Paramédical
Publié le 28 fév 2013Lecture 7 min
Fermeture percutanée de l’auricule gauche
L. LE FORESTIER, C. JAUNET (IDE), Nouvelles Cliniques Nantaises, Nantes
La fibrillation atriale (FA) est aujourd’hui l’arythmie la plus fréquente, fortement liée au vieillissement de la population. Ce n’est pas une maladie fatale en elle-même mais elle constitue un risque majeur d’accident vasculaire cérébral (AVC), multipliant ce risque par cinq.
La FA en quelques chiffres
• En France, la FA est responsable d’un AVC toutes les 20 minutes.
• 60 000 nouveaux cas par an en France sont répertoriés.
• Cette maladie atteint 4,5 millions de personnes en Europe et 5,1 millions aux État-Unis(1-2).
• Le nombre de personnes atteint de fibrillation atriale devrait doubler d’ici 2050(3).
• Environ 3 millions de personnes font un AVC lié à une fibrillation atriale chaque année(4-6).
La FA est caractérisée par un rythme cardiaque irrégulier et rapide. Elle peut être paroxystique, persistante ou chronique. La perte de systole en FA conduit à une diminution du débit cardiaque et à une stase du sang dans l’oreillette gauche, notamment dans l’auricule gauche, site privilégié de formation de thrombus. En effet, les AVC chez les patients atteints de FA sont essentiellement causés par des emboles provenant de l’auricule gauche.
Les facteurs de risque embolique chez les patients souffrant d’une FA, sans maladie valvulaire mitrale sont connus et évalués par le score CHA2DS2-VASc (tableau).
Une anticoagulation orale bien réglée constitue la prophylaxie de choix des accidents thromboemboliques chez les patients ayant un score CHA2DS2-VASc supérieur à 2.
Anatomie et localisation de l’auricule gauche
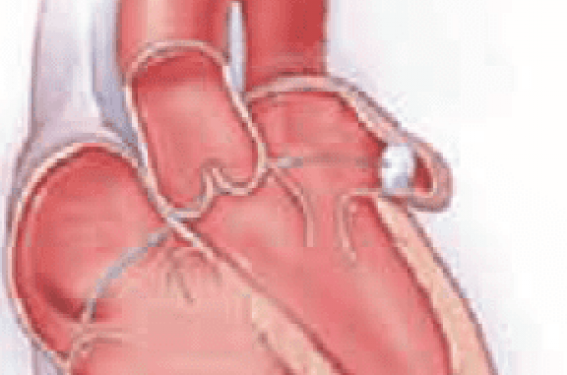
Généralement constituée de plusieurs lobes sans utilité connue, cette structure de forme complexe avec de nombreuses trabéculations (figure 1), est située entre la veine pulmonaire supérieure gauche et le ventricule gauche. L’orifice généralement ovalaire s’ouvre dans une zone convexe de la paroi auriculaire gauche. La partie proximale ou cervicale, de largeur et de longueur variables est connectée au corps de l’auricule gauche formé lui-même d’un ou plusieurs lobes avec une paroi d’épaisseur variable, parfois inférieure à 1 mm.
Figure 1. Auricules.
L’auricule est issu d’une rémanence de l’oreillette gauche embryonnaire primitive qui se développe durant la 3e semaine de gestation. La paroi lisse de l’oreillette se développe plus tard et est formée par l’accroissement des veines pulmonaires.
La branche circonflexe de l’artère coronaire gauche passe juste à côté de la base de l’appendice. L’orifice de l’appendice au niveau du corps de l’oreillette a un diamètre minimal de 0,5 à 2,7 cm tandis que le diamètre maximal est compris entre 1 et 4 cm. L’apex de l’auricule est plus contractile que son orifice. La morphologie et la taille de l’appendice sont très variables d’un patient à l’autre et sont influencées par la présence de pathologies annexes, telles que la FA, l’hypertension artérielle (HTA). La longueur de l’axe principal peut varier de 1,6 à 5 cm et son volume de 0,77 à 19,27 ml selon les pathologies associées.
Un peu d’histoire
Le premier système de fermeture chez l’homme a été utilisé en 2001 en Allemagne.
Le système de fermeture Watchman (figure 2 A), développé par Atritech et utilisé depuis 2002, est maintenant la propriété de Boston Scientific.
Depuis, d’autres systèmes sont arrivés sur le marché comme le système Amplatzer Cardiac Plug (St Jude Medical), disponible depuis 2009 (figure 2 B).
Figure 2. Système de fermeture Watchman (A) ; système Amplatzer Cardiac Plug (B).
Technique de fermeture
Cette technique de cathétérisme cardiaque s’adresse aux patients présentant un haut risque d’AVC lié à une fibrillation atriale, ayant une contre-indication au traitement anticoagulant oral (ACO), que ce soit par antivitamine K ou par les nouveaux anticoagulants oraux.
La fermeture percutanée de l’auricule gauche consiste à implanter une prothèse dans l’orifice de cette cavité cardiaque afin de prévenir la formation de thrombus dans cet auricule et d’éviter ainsi le risque d’AVC (figures 3 et 4). Une fois ce traitement réalisé, le patient pourra arrêter les ACO après un délai de traitement correspondant au temps d’endothélialisation de la prothèse.
Figure 3. Fermeture de l’auricule.
Figure 4. Mise en place sous radioscopie de la prothèse.
Dans notre centre, l’équipe en salle de cathétérisme est composée du cardiologue, d’un échographiste, de l’anesthésiste et de deux infirmières. La première est aide-opératoire et la seconde s’occupe, tout au long de la procédure, de contrôler les paramètres vitaux du patient, d’assurer le contrôle et la distribution du matériel utilisé.
Avant de commencer, les infirmières accueillent le patient, l’interrogent (check-list préopératoire), lui expliquent l’examen et le rassurent si besoin.
La procédure se fait sous anesthésie générale et sous échographie transœsophagienne (ETO) permettant :
- dans un premier temps, de vérifier l’absence de thrombus (auricule libre) ;
- dans un deuxième temps, d’effectuer une mesure précise du diamètre de l’auricule afin de choisir le matériel le plus approprié ;
- dans un troisième temps, de guider la ponction transseptale pour l’abord de l’oreillette gauche.
Les différentes étapes de notre pratique
- Ponction de la veine fémorale droite pour monter la gaine et l’aiguille qui permettront la ponction transseptale (figure 5), sécurisée par une mesure de la pression sanglante dans l’oreillette droite puis gauche, sous contrôle de la fluoroscopie et de l’ETO.
- Bolus d’héparine fait avant ou après la ponction transseptale selon l’opérateur, avec contrôle ACT (Activated Coagulation Time) en extemporané, fait à 20 minutes et 1 heure de l’injection pour vérifier l’efficacité de l’héparine (ACT souhaité entre 250 s et 350 s).
- Montée de la gaine d’accès sur un guide 0,035’’ de 260 cm, rigide de type Amplatz, qui est monté jusque dans l’oreillette gauche.
- Mise en place d’une sonde pigtail 5 F positionnée dans l’auricule et injection de produit de contraste permettant de confirmer le choix de la taille de la prothèse en fonction de la forme et la dimension de l’auricule.
- Montée de la gaine de pose purgée rigoureusement et choisie en fonction de la taille de l’implant.
- La prothèse est plongée dans du sérum physiologique hépariné afin d’évacuer l’air présent dans les mailles.
- Capture du dispositif dans le chargeur (selon les modèles). Ce montage, après purge rigoureuse de l’air dans le chargeur, est fixé à la gaine de pose et placé au niveau de l’orifice de l’auricule.
- Ouverture de la prothèse par retrait de la gaine de pose.
- Contrôle du positionnement de la prothèse sous fluoroscopie et ETO (en cas de mauvaise position de celle-ci, il est possible de recapturer la prothèse dans la gaine).
- Largage définitif de la prothèse.
- Retrait de la gaine et compression du point de ponction.
La totalité de l’ostium de l’auricule doit être obturée. La stabilité du dispositif implanté, élément de sécurité primordial, est facilitée par une taille de prothèse supérieure à la taille anatomique et par des crochets stabilisateurs situés tout autour de l’implant.
Le patient est toujours transféré après la procédure à l’Unité de soins intensifs de cardiologie (USIC), sa sortie est envisageable à J3 sous ACO (ou double antiagrégation plaquettaire en cas de contre-indication) pour une durée allant de 6 semaines à 3 mois.
Figure 5. Abord transseptal pour la fermeture de l’auricule gauche.
Risques et complications
- Hémopéricarde lié à la ponction transseptale.
- AVC perprocédure.
- Embolie gazeuse.
- Migration de la prothèse.
- Hématome au point de ponction lié à la taille des introducteurs (9 F, 10 F ou 13 F) ainsi qu’à l’héparinisation du patient.
Contre-indications
- Présence de thrombus dans l’oreillette ou l’auricule gauche.
- Diamètre de l’ostium de l’auricule < 10 mm ou > 30 mm.
Conclusion
Cette technique demande une très grande rigueur à chaque étape de la préparation du matériel, et nécessite un personnel médical et paramédical confirmé et formé à la technique. Le contrôle par l’infirmière des purges de chaque matériel est primordial tout comme l’accueil et l’installation du patient qu’elle assure. La présence de deux paramédicaux en salle permet d’effectuer une double vérification, donc assure plus de sécurité à chaque étape.
Dans la prévention du risque thromboembolique, ce traitement constitue probablement une alternative aux ACO au long cours, sous réserve de validation par les études en cours.
Ce dispositif médical n’est à ce jour pas remboursé en France (coût d’environ 5 000 euros), mais une demande de prise en charge est en cours pour les patients à haut risque embolique ayant une contre-indication aux ACO.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


