Échocardiographie
Publié le 14 nov 2016Lecture 10 min
Nouvelle approche dans l’exploration échographique transoesophagienne de la valve mitrale - Effets symbiotiques des techniques 3D virtuel et ultrasonore
S. LAFITTE*, A. QUESSARD**, *Unité médico-chirurgicale de valvulopathie et service des échocardiographies **Département de réanimation/anesthésie, Hôpital Cardiologique Haut Lévêque, CHU de Bordeaux
Cinq décennies d’évolutions technologiques prodigieuses dans le domaine des ultrasons ont permis une approche de plus en plus réaliste des représentations anatomiques du corps humain. Pour de nombreuses générations de médecins, jusqu’à maintenant, la réalité des structures organiques n’était que virtuelle, reconstruite, obtenue par l’interrogation parcellaire de l’espace investigué. Le mode TM a par exemple permis les premières descriptions du jeu valvulaire cardiaque, rapidement remplacé par le mode bidimensionnel, pour une meilleure compréhension des éléments visualisés. Les méthodes sont devenues systématisées, intégrant des plans de référence successifs afin de parfaire l’analyse morphologique de façon standardisée.
L’échographie transoesophagienne a démultiplié les capacités d’interrogation planaire de l’espace en introduisant les capteurs rotationnels, d’abord mécaniques puis électroniques. Les plans de coupes sont alors devenus infinis… et les difficultés à reconstruire cérébralement les volumes également… L’appréhension tridimensionnelle cardiaque, et a fortiori celle des structures complexes, non symétriques, comme par exemple la valve mitrale, n’en a pas été simplifiée, bien au contraire. Pire, faute de pouvoir reconstruire correctement ces structures dans nos aires sensorielles, faute de les comprendre, et en multipliant les modes d’imagerie, les outils, les vues et incidences, les durées d’examen en ont été allongées, préjudiciables en ETO, et a fortiori chez le patient vigile.
Or, ces dernières années, une conjoncture technologique favorable est en passe de modifier le paradigme actuel dans la façon de concevoir les connaissances, la pratique et l’enseignement de l’échocardiographie.
• Tout d’abord, les efforts en matière de simulation/modélisation ont enfin abouti. Les premiers mannequins de réalité virtuelle ont vu leur apparition, offrant la visualisation dynamique de l’anatomie fonctionnelle cardiaque, d’un réalisme exceptionnel. Une fois domptés, leur exploitation a permis de découvrir la structure de la valve mitrale en mouvement et son lien avec les éléments connexes, ce qui a autorisé la familiarisation de son environnement spatial, sa « géolocalisation » (figure 1).
• La mise en application in vivo de ces révélations a grandement été catalysée par la diffusion de la technologie 3D, et particulièrement en ETO. Retrouver, au cours de l’exploration ultrasonore, les images volumiques des mêmes structures cardiaques appréhendées virtuellement, a ouvert définitivement les portes d’une redéfinition de la façon de procéder l’examen ETO, en s’appuyant sur la complémentarité des modes 3D et multiplan.
Nous proposons tout d’abord de revisiter l’anatomie cardiaque centrée sur la valve mitrale, en précisant la localisation spatiale des différents éléments et leurs rapports, puis de définir les nouvelles approches descriptives durant l’examen échocardiographique transoesophagien avec la modalité 3D.
Figure 1. Représentation virtuelle tridimensionnelle de la valve mitrale en diastole (A) et en systole (B).
Anatomie dynamique de la valve mitrale
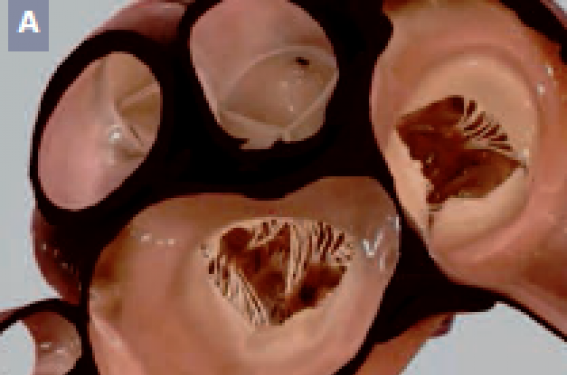
La valve mitrale, valve atrioventriculaire gauche, est une structure dynamique complexe comportant un anneau, deux feuillets (antérieur et postérieur), séparés par deux commissures (antéro-latérale ou externe, et postéro-médiane ou interne), et un appareil sous-valvulaire, composé de cordages et de deux piliers (antéro-latéral et postéromédian) (figure 2A).
L’anneau mitral est elliptique et possède une forme de selle de cheval, dont les portions creuses correspondent aux commissures valvulaires, et les portions les plus hautes aux zones médianes des feuillets mitraux (figure 2B). Les commissures sont situées plus bas que la ligne de coaptation des feuillets mitraux, et l’anneau fait saillie dans l’oreillette gauche sur les incidences échocardiographiques apicales 2 et 4 cavités, alors qu’il bombe vers le ventricule gauche en coupe parasternale gauche grand axe (ou ETO médio-oesophagien 120°).
Figure 2. A. Représentation schématique de la base du coeur montrant la face atriale de la valve mitrale, et permettant de révéler la proximité de son feuillet antérieur avec la valve aortique en position antérieure, la proximité de la zone 1 avec l’auricule gauche latéralement, la valve pulmonaire antérieurement, et celle de la zone 3 avec la valve tricuspide et les cavités droites. B. Représentation schématique de l’anneau mitral, elliptique, en forme de selle de cheval, et dont les portions creuses correspondent aux commissures valvulaires, et les portions les plus hautes aux zones médianes des feuillets mitraux. Le plan de l’anneau mitral désigné pour diagnostiquer les prolapsus est défini à partir de l’incidence médio-oesophagien 120° en ETO. C. Représentation schématique de la valve mitrale et de son appareil sous-valvulaire.
Le tiers antérieur de l’anneau mitral, qui correspond au bord d’insertion du feuillet antérieur, et qui est rattaché à l’anneau aortique par le trigone fibreux aorto-mitral, est relativement fixe. À l’opposé, les deux tiers postérieurs suivent la contraction ventriculaire, et jouent ainsi un rôle déterminant dans le maintien de l’étanchéité valvulaire en systole. La dilatation annulaire correspond le plus souvent à un étirement de cette zone postérieure. L’anneau mitral perd alors sa forme elliptique pour une forme circulaire. C’est donc son diamètre antéropostérieur médian qu’il est important de mesurer ; il est généralement inférieur à 40 mm, mais il existe des variabilités individuelles. En revanche, le rapport de ce diamètre avec la longueur du feuillet antérieur est plus constant, et normalement compris entre 1 et 1,2.
La valve mitrale comporte deux feuillets : un feuillet antérieur, de forme carrée et homogène, dont l’insertion mesure 30 mm (soit un tiers de la circonférence de l’anneau), pour une hauteur de 20 mm environ, et un feuillet postérieur, arciforme, subdivisé en 3 festons séparés par des indentations, et dont l’insertion, comparativement au feuillet antérieur, est plus longue (environ 55 mm, soit deux tiers de la circonférence de l’anneau mitral), et la hauteur plus réduite (environ 10 mm).
Malgré leurs formes différentes, les deux feuillets ont une surface équivalente.
L’appareil sous-valvulaire mitral comprend deux piliers, l’un antéro-latéral et l’autre postéromédian, situés à la verticale des commissures, et des cordages, rattachant le bord libre des feuillets mitraux aux piliers (figure 2C).
En systole, la contraction des piliers entraîne une traction des feuillets antérieur et postérieur, permettant ainsi de maintenir la valve mitrale fermée.
La description de la face atriale de la valve mitrale, qui correspond à la vue chirurgicale, est indispensable à connaître pour comprendre ses rapports anatomiques avec les structures adjacentes, et saisir les différentes informations fournies par les coupes échocardiographiques.
Il existe aujourd’hui un consensus entre échocardiographistes et chirurgiens pour segmenter la valve mitrale en trois zones (figure 2A) :
- la zone 1, antéro-latérale ou externe, où sont définis les segments A1 (feuillet antérieur), P1 (feuillet postérieur), et la commissure antéro-latérale (ou externe) ;
- la zone 2, médiane, avec A2 et P2 ;
- la zone 3, postéro-médiane ou interne, où l’on retrouve A3, P3, et la commissure postéromédiane (ou interne).
Sur une vue de la base du coeur, l’analyse de la face atriale de la valve mitrale révèle la proximité du feuillet antérieur mitral avec la valve aortique en position antérieure, celle de la zone 1 de la valve mitrale avec l’auricule gauche latéralement, et la valve pulmonaire antérieurement, et enfin, les rapports entre la zone 3 de la valve mitrale avec des structures anatomiques plus internes, que sont la valve tricuspide et les cavités droites.
Visualisation 3D de la mitrale
L’acquisition 3D doit être centrée sur la valve, afin de permettre le meilleur compromis entre la résolution spatiale et la résolution temporelle exprimée en volume par seconde (VPS). Un minimum de 10 VPS est nécessaire pour appréhender la dynamique de la structure dans le cycle cardiaque. Les systèmes actuels offrent une moyenne de 15 à 20 VPS en niveaux de gris, 10 VPS en 3D Doppler couleur. La représentation volumique de la valve mitrale permet une appréhension d’emblée globale, d’emblée anatomique, avec le positionnement des structures connexes (figure 3). Cette représentation visuelle 3D est d’abord rassurante car elle permet son intégration immédiate. Rapidement cependant, même si les anomalies patentes sont évidentes, l’oeil doit s’entraîner à l’analyse précise des différents reliefs et de leur dynamique. Toute une nouvelle sémiologie doit être décrite et domptée pour affiner les diagnostics.
Figure 3. Vue de la valve mitrale normale en ETO 3D en systole (A), et en diastole (B), qui permet la visualisation des indentations. CPM : commissure postéro-médiane, CAL : commissure antéro-latérale (cf. texte pour détails).
En pratique, l’acquisition volumique s’effectue en ETO au niveau oesophage moyen avec un recentrage/recadrage sur la structure permettant de s’affranchir des éléments proximaux. La valve mitrale est représentée en vue chirurgicale à partir de l’oreillette gauche avec l’aorte à 12 h, l’auricule à 9 h, la tricuspide à 3 h. On découvre la valvule mitrale antérieure sous le trigone aorto-mitral et celle postérieure de surface plus importante, et de gauche à droite, la commissure antérolatérale (externe), les feuillets A1P1, puis A2P2, A3P3 et enfin la commissure postéro-médiane (interne). La surface des 2 valvules est relativement lisse, avec peu de redondance, un léger bombement en systole. L’ouverture est harmonieuse, souple, avec une quasi-verticalisation des feuillets. On note au niveau postérieur et en diastole deux indentations plus ou moins profondes qui délimitent la zone 2 des zones 1 et 3. Cette vue permet d’appréhender qualitativement les prolapsus, les éversions de valves et ruptures de cordage. Plus spécifiquement, la localisation des lésions est efficiente. Le diagnostic des prolapsus commissuraux, difficilement identifiables en 2D, est ici grandement facilité (figure 4). On observe une ouverture limitée de l’orifice mitral en cas de restriction de jeu valvulaire avec la description de la dynamique de chacun des segments. L’identification de calcifications est néanmoins délicate. Le Doppler Couleur 3D aide à la compréhension des mécanismes de régurgitation, en prenant soin d’abaisser le plan de coupe supérieur au niveau de la zone de coaptation.
Figure 4. Exemple d’un prolapsus de commissure antéro-latérale et A1 avec rupture de cordage visualisé en ETO 3D. On note l’aspect de bombement en relief de la zone pathologique.
Acquisitions biplanaires sériées
Au-delà d’un rendu visuel réaliste et esthétique, le mode 3D n’est pas suffisant, particulièrement en vue du dessus, car les éléments proximaux sont occultants pour ceux sousjacents. Afin d’explorer les rapports des structures entre elles dans la profondeur du faisceau et de donner une dimension quantitative à la description, la deuxième phase est celle d’acquisitions sériées en mode bidimensionnel par la technique de balayage. Le mode bidimensionnel présente un avantage majeur sur le 3D par de plus hautes résolutions spatiales et temporelles, qui le rendent indispensable dans l’exploration fine des structures.
Le balayage transversal s’effectue directement par la manipulation de la sonde à partir de la coupe médio-œsophagienne 3 cavités (à 120° environ) (figure 5), par rotation de la poignée de la sonde, dans le sens horaire pour explorer la zone 3 et la commissure postéromédiane ou antihoraire pour la zone 1 et la commissure antéro-latérale. Après l’analyse de A2P2 en position centrale, il est conseillé de balayer des extérieurs vers l’intérieur pour une identification correcte des zones 1 et 3.
Figure 5. Exploration de la valve mitrale en ETO selon la méthode de balayage transversal effectué, à partir de la coupe médio-oesophagienne 3 cavités (B), par rotation de la poignée de la sonde, dans le sens horaire pour explorer la zone 3 et la commissure postéro-médiane (A) (les structures connexes étant la valve tricuspide (VT) et les cavités droites) ou antihoraire pour la zone 1 et la commissure antéro-latérale (C) (la structure connexe étant la valve pulmonaire [VP]).
Les sondes 3D matricielles permettent d’effectuer électroniquement ce balayage. L’outil biplan propose une image de référence à gauche de l’écran sur laquelle une ligne curseur peut être déplacée avec le « trackball » et dont le plan de coupe résultant à 90° se retrouve sur l’image de droite (figure 6). Le balayage de la ligne curseur est alors extrêmement précis, permettant d’additionner les plans de coupe sériés les uns après les autres telle une acquisition en scanner. La reconstruction cérébrale s’automatise presque naturellement et vient complémenter l’information 3D visualisée dans la première phase. Les acquisitions de cette deuxième phase s’effectuent en niveaux de gris et en Doppler couleur.
L’image de gauche est la vue bicommissurale, dégageant l’auricule gauche visualisé à l’écran à droite de la valve. Cette vue présente l’avantage de facilement discriminer les zones 1, 2, et 3 de la valve mitrale. Le curseur est alors placé en zone 2, permettant l’affichage sur l’image de droite de la vue des 3 cavités (ou LVOT pour left ventricular outflow tract) passant par A2P2. Le curseur est ensuite déplacé en zone 1, révélant à droite A1P1 et un peu plus loin la commissure antéro-latérale, puis en zone 3 pour dégager A3P3 et la commissure postéromédiane.
L’identification des zones 1 ou 3 se contrôle par la visualisation des structures connexes comme pour la zone 1, la valve et le tronc de l’artère pulmonaires, et pour la zone 3, le ventricule droit et la tricuspide.
La technique est reproduite en mode Doppler couleur pour une analyse précise de l’origine des régurgitations.
Grâce à la pénétration des ultrasons, les relations des éléments entre eux sont jaugées dans la profondeur, et mesurées le cas échéant, comme par exemple une hauteur de coaptation, un hiatus valvulaire, un abcès, une calcification, etc.
Figure 6. Exemple d’acquisition en mode biplan sur une valve mitrale en balayant les zones 1 à 3 sur l’image de gauche et en observant la résultante sur l’image de droite.
Reconstruction MPR (multiplanar reconstruction)
Enfin, la dernière phase s’appuie sur l’acquisition 3D initiale et applique la technique MPR (multiplanar reconstruction) sur la matrice volumique. L’objectif est la reconstruction de plans de coupe inédits, improbables, voire irréels en ultrasonographie conventionnelle. Pour exemple dans le cas du rétrécissement de la valve mitrale, nous irons chercher le plan au sommet de l’entonnoir dont l’orientation sera strictement parallèle au plan d’ouverture des 2 valves (figure 7). Cette phase est nécessaire à une approche quantitative de surface ou de distance, bien plus précise que la mesure sur les volumes. Il est à noter que malgré tout, cette méthode est limitée par la résolution spatiale de la technique d’acquisition, qui reste le mode 3D.
Figure 7. Acquisition en ETO 3D d’une valve mitrale sténosée (A) et application de la technique de reconstruction de coupe MPR (multiplanar reconstruction) afin d’effectuer une planimétrie de l’orifice (B).
En pratique
Une nouvelle ère dans l’exploration et la compréhension de la valve mitrale se dessine sous l’angle de l’intégration tridimensionnelle.
La visualisation volumique doit s’accompagner de plans bidimensionnels acquis en mode biplan ou par balayage selon une méthode systématique.
Plus rapide, plus efficace, elle permet de réduire les temps d’analyse et les erreurs d’interprétation.
Elle répond par ailleurs à une réelle nécessité d’adapter les techniques de corrections chirurgicales ou interventionnelles aux lésions observées.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :