Publié le 15 nov 2018Lecture 6 min
Échographie dans l’insuffisance cardiaque
Noumer NASSER, CCA, service du Pr S. Lafitte, Hôpital du Haut-Lévêque, Pessac
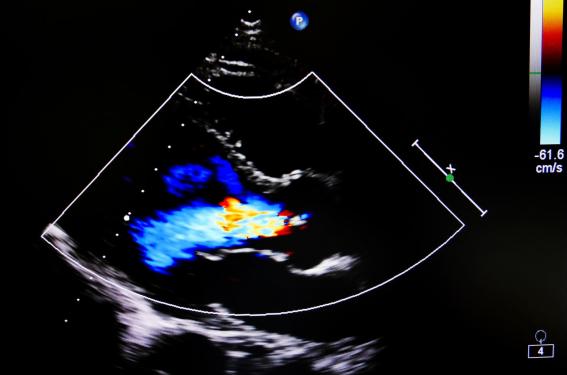
L’échocardiographie est l’outil de première ligne d’évaluation diagnostique et pronostique ou du suivi thérapeutique dans l’insuffisance cardiaque.
Quantification de la fonction systolique : approche multimodale
D’après Julien Ternacle, Paris
La fonction systolique du ventricule gauche est un paramètre indispensable de l’évaluation échocardiographique. Elle a un intérêt diagnostique, pronostique dans l’insuffisance cardiaque et permet de guider la thérapeutique. La fonction systolique VG peut être évaluée selon différentes modalités d’imagerie, dont il est nécessaire de connaître les avantages et les limites.
L’échographie
Facilement accessible, elle permet une évaluation de la FEVG par la méthode du Simpson biplan et par acquisition tridimensionnelle avec une bonne fiabilité chez un opérateur entraîné.
L’examen peut être complété par l’évaluation de la fonction systolique longitudinale par le strain global, notamment dans le suivi des chimiothérapies et de l’amylose cardiaque.
Le principal défaut est une tendance à la sous-évaluation des volumes télédiastolique et télésystolique par rapport à l’IRM. L’IRM cardiaque est le gold standard pour l’évaluation des volumes et de la fonction systolique ventriculaire gauche. La technique est limitée par une disponibilité disparate selon les centres et les contre-indications à l’examen, notamment chez les patients porteurs de matériel métallique.
Le scanner cardiaque
Il peut proposer des acquisitions pour l’évaluation de la fonction systolique ventriculaire gauche, avec une bonne fiabilité des volumes et de la FEVG en comparaison à l’IRM. La technique, outre son caractère irradiant, n’est à l’heure actuelle pas disponible dans tous les centres. Il est indispensable de savoir confronter les résultats des différentes techniques en cas de doute ou de discordance.
Évaluation de la fonction diastolique
D’après P. Lancellotti, Liège
L’augmentation des pressions de remplissage VG (PRVG) est reconnue comme facteur déterminant des symptômes cardiaques et du pronostic des patients insuffisants cardiaques chroniques, indépendamment de la fraction d’éjection. L’échographie cardiaque en permet une évaluation qualitative. Le principal paramètre jusqu’en 2016 était le rapport isolé E/e’. EURO-FILLING, étude incluant 159 patients, a permis de comparer différents paramètres échographiques d’estimations des PRVG à la pression télédiastolique VG obtenue par cathétérisme cardiaque. Les résultats ont confirmé l’intérêt des recommandations de 2016 de l’ASE et de l’ESC pour l’évaluation par des paramètres combinés des PRVG (figure), avec une fiabilité supérieure (sensibilité 75 %, spécificité 74 %, VPP 39 %, VPN 71 %) à la prise en compte isolée du E/e’.
Figure. Algorithme diagnostique d’une dysfonction diastolique ventriculaire gauche chez un patient à fraction d’éjection ventriculaire gauche normale selon les recommandations 2016 de l’ASE et de l’ESC.
Insuffisance cardiaque à FEVG préservée
D’après Erwan Donal, Rennes
Les recommandations de l’ESC distinguent trois types d’insuffisance cardiaque. L’insuffisance cardiaque à fraction d’éjection altérée se définit par une fraction d’éjection ventriculaire gauche (FEVG) inférieure à 40 %, l’insuffisance cardiaque à fraction d’éjection modérément altérée par une FEVG de 40 à 49 %, l’insuffisance cardiaque à fraction d’éjection préservée (ICFEP) par une FEVG supérieure ou égale à 50 %.
Le diagnostic d’insuffisance cardiaque à fraction d’éjection modérément altérée et l’ICFEP se fondent sur un tableau clinique d’insuffisance cardiaque, un taux de BNP élevé et des cr tères échographiques structuraux (volume de l’OG supérieure à 34 ml/m2 ou hypertrophie VG) ou fonctionnels (E/e’ > 13 et e’ moyenné < 9 cm/s).
En cas de diagnostic incertain, l’échographie d’effort peut orienter le cardiologue, en cas d’élévation des pressions pulmonaires à l’effort associée à un E/e’ moyen > 14 et un e’ septal < 7 cm/s.
Constriction péricardique
D’après Yannick Jobic, Brest
Le diagnostic échographique de péricardite chronique constrictive (PCC), et notamment sa distinction d’une cardiomyopathie restrictive est souvent complexe (CMR). Cette distinction est cependant nécessaire afin d’orienter le patient vers une thérapeutique adaptée (anti-inflammatoires ou péricardectomie dans la PCC, traitement spécifique selon l’étiologie de la CMR).
Rappelons les signes communs d’orientation aux deux pathologies : taille et fonction systolique ventriculaire gauche conservées, dilatation du massif atrial, profil de remplissage mitral restrictif, veine cave inférieure dilatée, non compliante et adiastolie sur le flux d’insuffisance pulmonaire.
Les signes échographiques en faveur d’une PCC sont la présence d’anomalies morphologiques du péricarde, une interdépendance VD-VG à l’origine d’un shift septal inspiratoire et de variations respiratoires des flux, des vitesses de Doppler tissulaire à l’anneau mitral conservées et parfois un e’ septal supérieur au e’ latéral (annulus inversus), un strain longitudinal global peu altéré.
Le diagnostic de PCC évoqué en échographie cardiaque doit être confronté à une IRM cardiaque, un cathétérisme cardiaque droit et gauche et/ou un scanner cardiaque.
Imageries multimodalités dans les cardiomyopathies restrictives
D’après Gilbert Habib, Marseille
Les cardiomyopathies restrictives (CMR) représentent la cause la moins fréquente des cardiomyopathies. Elles sont définies par une physiologie restrictive en présence de volumes ventriculaires normaux, d’une fonction systolique ventriculaire gauche normale et sans hypertrophie myocardique.
Les CMR constituent en fait un groupe hétérogène de cardiomyopathies expliquant les discordances même dans leurs classifications.
Selon leur mécanisme physiopathologique, elles peuvent être classées en cardiomyopathies infiltratives, comme l’amylose cardiaque, de surcharge, comme l’hémochromatose, ou endomyocardiques, comme la fibrose endomyocardique.
Une subdivision entre CMR génétiques ou non est également utile.
Dans tous les cas, les différentes techniques d’imagerie non invasive (échocardiographie, scanner, IRM) occupent une place fondamentale dans leur évaluation, tant au point de vue diagnostique que pronostique. Un document de consensus publié en 2017 rapporte le rôle de ces différentes techniques d’imagerie pour le diagnostic, l’évaluation pronostique et la prise en charge de ces patients.
L’imagerie peut être complétée dans certains cas par d’autres investigations comme la biopsie endomyocardique ou les analyses génétiques. Ces pathologies rares doivent être prises en charge dans des centres de référence spécialisés permettant une approche pluridisciplinaire.
Insuffisance cardiaque en oncologie
D’après Stéphane Ederhy, Paris
La dysfonction systolique VG est une complication fréquente des chimiothérapies dans le cadre du suivi du patient en oncologie, dont le mécanisme dépend de la molécule administrée.
Les anthracyclines (ATC) peuvent entraîner une dysfonction systolique VG, toxicité considérée dans la majorité des cas comme dépendante de la dose, cumulative et généralement irréversible. Le principal mécanisme de la toxicité cardiaque aux ATC est la génération et la majoration du stress oxydatif, entraînant une déstabilisation de la synthèse et la dégradation des protéines sarcomériques, une modification de l’homéostasie calcique et une diminution de la production d’ATP du cardiomyocyte.
L’incidence de la dysfonction systolique VG asymptomatique est de 18 %, l’incidence des patients symptomatiques de 6 %.
Le trastuzumab (Herceptine®) fait partie des thérapies moléculaires ciblées. Sa toxicité à l’origine d’une dysfonction systolique VG est habituellement réversible à l’arrêt de la chimiothérapie, sensible à l’introduction d’un traitement de l’insuffisance cardiaque, ce qui autorise en général la reprise de la chimiothérapie. L’incidence de sa toxicité hors administration contemporaine d’ATC est de 4,1 %.
Les immunothérapies sont prescrites dans la prise en charge des patients présentant un mélanome ou un cancer pulmonaire. La principale complication cardiaque est représentée par les myocardites dont l’incidence est faible, estimée à 0,19 %. Elles peuvent évoluer rapidement vers le choc cardiogénique et le décès dans 25 à 50 % des cas. Le traitement s’appuie principalement sur l’administration rapide et en urgence, dès la suspicion clinique de bolus de corticoïdes.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :