Publié le 25 mar 2008Lecture 8 min
L'échographie dans les complications aiguës de la chirurgie cardiaque
M. MICHEL-CHERQUI et Ph. DE LENTDECKER, hôpital Foch, Suresnes
Les Journées européennes de la SFC
La pratique de l’échocardiographie en postopératoire de chirurgie cardiaque s’avère systématiquement nécessaire quand des anomalies hémodynamiques (instabilité, hypotension voire choc ou collapsus), gazométriques (hypoxémie) ou électrocardiographiques (ischémie, troubles du rythme) ne répondent pas rapidement à un traitement médical bien conduit.
Les questions auxquelles le réanimateur doit répondre rapidement sont les suivantes :
• Une réintervention est-elle nécessaire en urgence ?
• Peut-on optimiser le traitement médical ?
• Y a-t-il une indication à mettre en place une assistance ?
L’examen échocardiographique transthoracique (ETT) et/ou transœsophagien (ETO) est l’outil de choix pour répondre à ces questions(1,2).
L’analyse hémodynamique conventionnelle est souvent insuffisante dans ces circonstances, et ceci a été démontré dans de nombreuses études. Chez les patients ayant bénéficié d’une ETO en urgence en postopératoire, dans plus de la moitié des cas l’examen échocardiographique permet de corriger le diagnostic et de modifier la prise en charge. Dans plus d’un tiers des cas, l’apport de l’ETO est jugé essentiel(3,4).
L’examen systématique permet l’analyse en imagerie et en Doppler des valves, parois et cavités. Il s’attache particulièrement à évaluer la qualité du geste chirurgical, surtout si un examen peropératoire n’a pas été pratiqué. Par ailleurs, il doit permettre l’évaluation de la précharge du ventricule gauche (VG), des fonctions ventriculaires gauche et droite et de la cinétique segmentaire. L’analyse de l’aorte est également systématique. Un foramen ovale perméable (PFO) doit être recherché en cas d’hypoxie. Enfin, l’analyse des plèvres et du parenchyme pulmonaire est recommandée.
L’examen peut être pratiqué en ETT dans un premier temps. Du fait de la ventilation artificielle, du décubitus dorsal, de la présence du pansement de sternotomie et des drains thoraciques, les fenêtres d’examens sont limitées et la qualité des images est souvent médiocre. Il est donc indispensable dans la majorité des cas d’effectuer un examen en ETO. Chez un patient sédaté, la sonde sera introduite au mieux sous contrôle laryngoscopique.
Complications nécessitant une réintervention en urgence
Les tamponnades
Elles sont au premier rang de ces complications et peuvent survenir quel que soit le type de chirurgie chez ± 5 % des opérés cardiaques. Elles sont en relation avec un saignement diffus ou localisé au site d’une anastomose ou exceptionnellement d’une plaie myocardique ou d’une dissection aortique.
Elles sont rares durant les 24 à 48 premières heures suivant la chirurgie car les drains permettent d’évacuer un saignement actif. Au-delà, le patient n’est plus drainé et un choc ou un tableau hémodynamique peu spécifique doit faire évoquer le diagnostic.
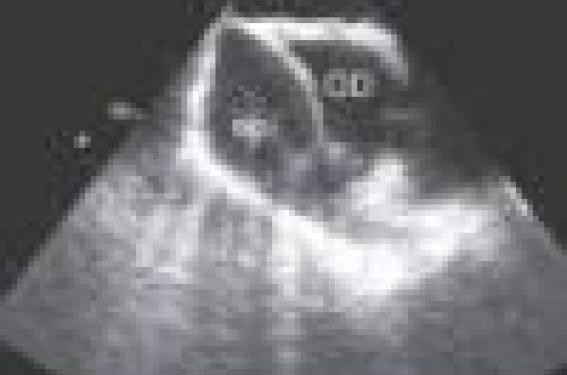
La tamponnade peut être circonférentielle, aisément visible en ETT. Une tamponnade localisée, comprimant la paroi postérieure ou électivement l’oreillette droite ou gauche est plus difficile à diagnostiquer ; elle nécessite fréquemment une approche par ETO (figure 1). La reprise chirurgicale s’impose pour décomprimer les cavités et réaliser l’hémostase.
Figure 1. Épanchement comprimant électivement l’oreillette droite. Ep : épanchement, OD : oreillette droite, OD : oreillette droite.
Les complications en rapport avec la CEC
Plus rares, elles peuvent également survenir quel que soit le type de chirurgie.
• Une dissection de l’aorte ascendante au site de canulation est une urgence chirurgicale.
• La canulation du sinus coronaire utilisée en cas de cardioplégie rétrograde peut être responsable d’un hématome du sinus ou plus rarement, d’un hématome de la paroi de l’oreillette gauche. Ces complications doivent être évaluées avec le chirurgien pour juger de l’opportunité d’une reprise.
La chirurgie valvulaire
Après chirurgie valvulaire, on recherchera une sténose iatrogène, une plastie valvulaire incomplète (fuite résiduelle > grade I), une thrombose de valve, une fuite paraprothétique pathologique (figure 2), une malposition de la valve, des mouvements anormaux des éléments mobiles d’une prothèse mécanique.
Figure 2. Fuite paraprothétique mitrale. F : fuite paraprothétique, OG : oreillette gauche.
En position aortique, une prothèse aortique mal positionnée peut entraîner l’obstruction des ostia coronaires et être responsable d’anomalies de la cinétique segmentaire ou d’un arrêt cardiaque brutal.
En position mitrale, du fait de la proximité anatomique entre l’anneau mitral, l’artère circonflexe et la valve aortique, une chirurgie mitrale (redux, calcifications) peut être responsable de complications exceptionnelles : la ligature accidentelle de l’artère circonflexe se manifeste par un trouble localisé de la cinétique segmentaire, la ligature accidentelle d’une sigmoïde aortique est responsable d’une fuite aortique majeure. Après plastie mitrale, un SAM (systolic anterior motion) peut classiquement être rencontré. Celui-ci est devenu exceptionnel, les chirurgiens utilisant des techniques permettant de le prévenir (plastie par glissement en cas d’excès tissulaire sur la petite valve par exemple) et l’ETO peropératoire étant pratiquement systématique lors de ces interventions. La survenue d’un collapsus dû à un SAM en réanimation se traite médicalement et une reprise chirurgicale est exceptionnelle.
La chirurgie coronaire
L’examen recherchera plus particulièrement une akinésie complète dans le territoire revascularisé (échec de plastie du tronc, thrombose précoce de pontage) imposant une reprise chirurgicale ou interventionnelle.
Analyse hémodynamique
Après avoir éliminé une complication aiguë relevant d’une reprise chirurgicale, l’examen ETO va permettre d’évaluer les fonctions ventriculaires droite et gauche et d’optimiser la prise en charge médicale. L’examen doit être rigoureux et systématique (une « routine » est recommandée), faire appel à des critères simples à obtenir et aisément reproductibles et être renouvelé afin d’apprécier de manière dynamique la réponse au remplissage et aux agents pharmacologiques(5). Il faut tenir compte du fait que les indices recueillis sont sensibles à des événements fréquents en postopératoire : troubles du rythme, bloc de branche, entraînement électrosystolique, ventilation en pression positive.
La fonction « pompe » du ventricule gauche est suivie sur la fraction de raccourcissement de surface ventriculaire gauche (coupe petit axe transgastrique) et la fraction d’éjection obtenue en coupe 2 cavités. La fonction ventriculaire droite est estimée sur l’analyse des rapports VD/VG en coupe transgastrique 2 cavités et en coupe 4 cavités. La courbure du septum est appréciée sur cette coupe, un index d’excentricité (diamètre antéro-postérieur/diamètre postero-latéral est estimé sur cette coupe.
Dysfonction ventriculaire
Une dysfonction ventriculaire (droite, gauche) sera prise en charge médicalement et le traitement (vasopresseurs, inotropes, NO) sera optimisé grâce au suivi échocardiographique. Il peut être parfois nécessaire de recourir à une assistance ventriculaire. L’échographie va alors permettre de contribuer au choix de l’assistance et de détecter les contre-indications à sa mise en place (insuffisance aortique, PFO, thrombus intracavitaire, etc.).
La cinétique segmentaire est appréciée au moins sur 4 coupes (petit axe transgastrique, 2 cavités, 4 cavités et 5 cavités) pour apprécier rapidement la contractilité dans les 3 principaux territoires.
Dysfonction segmentaire
En cas d’anomalies de cinétique segmentaire dans le territoire ponté, la pression de perfusion doit être optimisée, soit pharmacologiquement, soit grâce à une assistance ventriculaire. Le ballon de contre-pulsion intra-aortique est un moyen simple d’améliorer la perfusion myocardique. Sa mise en place peut être guidée par l’ETO.
La précharge et le « remplissage » du ventricule gauche sont globalement appréciés sur la mesure des surfaces télédiastolique et télésystolique du ventricule gauche. Les variations de diamètre des veines caves lors des cycles ventilatoires et l’analyse des Doppler mitraux (flux mitral et Doppler tissulaire de l’anneau) permettent d’apprécier l’éventuel bénéfice d’un remplissage.
Anomalies de la précharge
Une hypotension est le plus souvent la manifestation d’une précharge basse : hypovolémie vraie (hémorragie), vasoplégie (réchau-ffement, réaction inflammatoire, sepsis). Deux situations particulières doivent être recherchées :
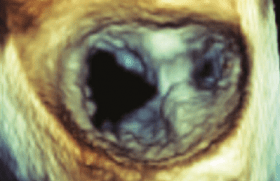
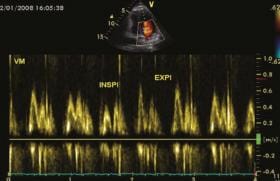
• une obstruction dynamique intraventriculaire gauche doit être suspectée devant un patient dont l’état hémodynamique s’aggrave sous inotropes. Les facteurs favorisant sa survenue sont l’excès tissulaire mitral (figure 3), l’hypertrophie ventriculaire gauche fréquente chez les hypertendus et les patients venant d’être opérés d’un remplacement valvulaire aortique pour rétrécissement aortique, l’existence d’une petite cavité, un bourrelet septal, une baisse de la postcharge. L’examen échographique objective l’accélération du flux en Doppler couleur dans la chambre de chasse, un enregistrement en Doppler continu à ce niveau montre des vitesses très accélérées (> 4 à 6 m/s), en cas d’excès tissulaire mitral, on visualise le mouvement de la grande valve en systole venant obstruer la chambre de chasse. Le traitement, dont les effets doivent être suivis en ETO, associe le remplissage, l’arrêt des inotropes, voire l’administration de bêtabloquants.
Figure 3. Examen réalisé lors d’un collapsus CV dans les suites d’une chirurgie coronaire : obstruction dynamique du ventricule gauche chez un patient présentant un excès tissulaire mitral. Le traitement associe un remplissage vasculaire, l’arrêt des inotropes puis l’administration de bêtabloquants. A. La grande valve mitrale obstrue en systole la chambre de chasse du ventricule gauche ; B. On enregistre en Doppler continu une vitesse à 5,5 ms en systole, témoin du gradient intraventriculaire gauche majeur.
• Le retentissement de la ventilation en pression positive sur l’hémodynamique doit être recherché. Celle-ci va avoir un effet sur la précharge ventriculaire gauche soit par l’intermédiaire du ventricule droit, soit directement chez les patients emphysémateux par un retentissement direct de la ventilation sur les cavités cardiaques, phénomène qualifié de tamponnade gazeuse. Une manœuvre de débranchement du respirateur sous contrôle échographique permet d’objectiver une amélioration tensionnelle, une augmentation significative de la surface télédiastolique ventriculaire gauche. Les paramètres du respirateur doivent ensuite être adaptés en fonction de cette manœuvre.
En cas d’hypoxémie, un PFO doit être systématiquement recherché en Doppler couleur, puis par injection de microbulles dans l’oreillette droite par le cathéter central habituellement en place. L’analyse des plèvres (ETO et ETT) et du parenchyme pulmonaire (ETT) conclut l’examen.
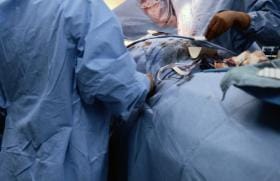
Enfin, la mise en place de voies veineuses centrales et d’abords artériels sous contrôle échographique accroît la sécurité de ces gestes (figure 4).
Figure 4. Pose échoguidée d’un cathéter veineux central : on visualise la jugulaire interne droite et la carotide chez un patient admis pour dissection aortique. C : carotide ; Fi : flap intimal ; JID : jugulaire interne droite.
En pratique
L’usage de l’échocardiographie est incontournable dans les services de réanimation après chirurgie cardio-thoracique. La formation des médecins doit se généraliser afin de prendre en charge les patients rapidement et de manière optimale.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :