Publié le 06 nov 2012Lecture 7 min
Les myocardiopathies hypertrophiques - Le traitement médical et les recommandations mixtes HAS et SFC
O. DUBOURG*, N. MANSENCAL* PH. CHARRON**, PH. BLANCHARD*** * hôpital Ambroise Paré, Boulogne-Billancourt ** hôpital de la Pitié-Salpêtrière, Paris *** Service des bonnes pratiques professionnelles à la Haute Autorité de Santé.
Les Journées françaises de l'insuffisance cardiaque
La CMH est la plus fréquente des maladies cardiaques d’origine génétique, caractérisée par une HVG qui touche le plus souvent le septum interventriculaire avec présence ou non d’un obstacle à l’éjection. Un élément essentiel du bilan est l’étude génétique car l’origine génétique et le dépistage des apparentés est fondamental dans cette maladie ; c’est pourquoi elle est recommandée.
Notre objectif(1) a été de mettre à disposition de tous les acteurs de santé des documents qui permettent la prise en charge optimale et décrivent le parcours de soins des patients atteints de CMH. Les recommandations recouvrent un protocole national de diagnostic et de soins, le PNDS, tiré d’un argumentaire scientifique détaillé qui s’accompagne d’une liste des actes et des prestations des affections longue durée de LAP. Ces documents sont consultables sur le site de l’HAS : www.has-sante.fr et sur le site de la SFC : www.sfcardio.fr. Des recommandations similaires communes ACC/AHA viennent d’être publiées simultanément, dont leur contenu ne diffère pas des recommandations françaises
rapportées ici(2).
Les formes familiales de CMH représentent plus de 50 % des cas et la maladie est en fait d’origine génétique dans la quasi-totalité des cas, avec une transmission autosomique dominante(3). Ceci justifie une stratégie de dépistage familial cardiologique (ECG et échocardiographie) ou mieux guidée par les résultats d’un test génétique prédictif. Cette démarche doit être faite en collaboration avec les généticiens dans des centres spécialisés(4).
Le médecin généraliste a un rôle essentiel dans la surveillance mais une consultation cardiologique est recommandée au moins une fois par an pour les patients asymptomatiques. Les autres examens spécialisés peuvent être réalisés en fonction du tableau clinique. Les patients symptomatiques seront suivis en fonction de l’avis du cardiologue et de la réponse au traitement.
Quelle surveillance, à quel rythme ?
En ce qui concerne les « porteurs sains », une surveillance régulière est nécessaire pendant une période estimée entre 1 et 3 ans en fonction de l’évolution de la maladie. Concernant les actes médicaux à réaliser par le cardiologue, on recommande : une consultation annuelle ou plus rapprochée selon l’état clinique pour le suivi et l’adaptation de la stratégie thérapeutique.
Les examens à réaliser systématiquement sont l’ECG et l’échocardiographie Doppler. Quand il existe un doute sur l’échocardiographie il peut être complété par une IRM cardiaque. Celle-ci est recommandée pour les patients avec une suspicion de forme apicale (parfois méconnue par l’échocardiographie) et peut être utile pour les autres phénotypes de CMH(5). Enfin, d’autres examens sont réalisables en fonction de la situation clinique (VO2, coronarographie) (tableau 1).
Sur le plan biologique, seul le test génétique est considéré comme systématique les autres examens sont faits en fonction du contexte clinique (CPK, BNP, pro-BNP, TSH).
Prédiction/prévention de la mort subite
La mort subite est la complication la plus redoutée de cette maladie. Le mécanisme principal retrouvé sur l’interrogation des défibrillateurs déjà implantés montre qu’il s’agit le plus souvent de TV ou de FV.
La mort subite survient chez des patients à haut risque et la recherche de facteurs de risque permet de cerner les patients les plus menacés(6). Toutefois le bilan est parfois insuffisant pour prédire/prévenir la mort subite.
Cinq facteurs de risque (FR) sont considérés comme majeurs
Leur mise en évidence repose sur :
• L’interrogatoire du patient à la recherche de syncope, particulièrement quand elle survient à l’effort et de façon répétitive ou bien chez un sujet jeune. Mais la valeur prédictive de la syncope comme signe précurseur d’une mort subite éventuelle est faible.
• L’interrogatoire du patient et de la famille à la recherche d’antécédents de mort subite prématurée (< 50 ans, surtout si survenue chez un apparenté au 1er degré et surtout si ≥ 2 cas).
La réalisation d’un Holter ECG (24 à 48 h) à la recherche de TV non soutenues (≥ 3 complexes à une fréquence supérieure à 120/min).
La réalisation d’une épreuve d’effort avec recherche d’une réponse anormale de la pression artérielle lors de celle-ci (sur tapis roulant ou sur un vélo). La réponse est pathologique en cas de réponse tensionnelle plate (PAS max – PAS repos < 20 ou 25 mmHg) ou de survenue d’une hypotension. La valeur prédictive a été montrée chez des patients avant 50 ans.
L’échographie cardiaque doit rechercher une épaisseur de la paroi VG > 30 mm.
On classe à part les facteurs de risque possibles ou mineurs tels : un début des symptômes dès l’enfance ;
- la présence d’une ischémie myocardique documentée ; une obstruction sous-aortique isolée ≥ 30 mmHg ;
- la découverte d’une mutation dite à haut risque (certaines mutations ou gènes ont été identifiés comme associés à un haut risque de mort subite : certaines mutation de la bêta myosine comme Arg719Gln et Arg403 Gln, et la plupart des mutations de la troponine T).
Le bilan d’évaluation du risque rythmique doit donc comporter systématiquement, outre l’échographie cardiaque, un Holter ECG (24 à 48 h), une épreuve d’effort avec profil tensionnel d’effort. La recherche de potentiels tardifs (ECG-HA) n’a pas d’intérêt. La réalisation d’une stimulation ventriculaire programmée a un intérêt faible et discuté, et n’est donc pas recommandée.
Quelle signification simple peut-on retenir pour les facteurs de risque (FR) ?
• Le sujet est considéré à haut risque rythmique en présence d’au moins 2 des FR majeurs et la mortalité annuelle est alors > 4 %. Ceci conduit habituellement à préconiser la pose d’un défibrillateur implantable.
• En présence d’un seul FR majeur, l’attitude varie selon les experts et certains discutent un défibrillateur. Chaque cas doit être envisagé individuellement.
• Le sujet est considéré comme à faible risque rythmique s’il ne présente aucun FR majeur. La présence de plusieurs facteurs de risque mineurs est probablement péjorative mais l’absence d’évaluation de cette situation ne permet pas de conclure de façon définitive ni de recommander une conduite particulière. Il n’y a pas traitement à visée anti-arythmique à préconiser. Les restrictions sportives et une surveillance annuelle restent indispensables.
Quel traitement proposer ?
Le traitement médical est à réserver aux patients symptomatiques car, en l’absence de facteurs de risque rythmique et de symptômes, il n’y a pas lieu de traiter ces malades en dehors des restrictions sportives ; la poursuite d’une surveillance régulière s’impose en revanche ; en présence de symptômes le traitement fait appel essentiellement aux bêtabloquants et parfois au vérapamil.
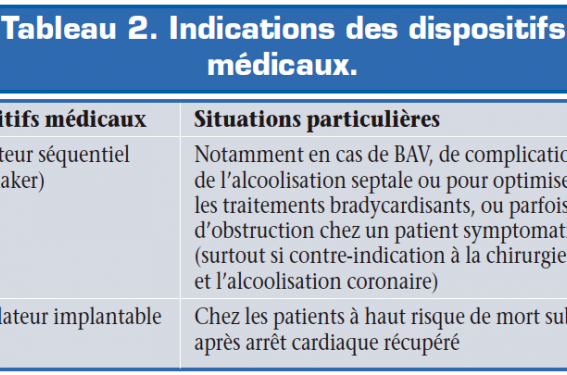
Concernant les dispositifs implantables : nous n’avons pas de données permettant d’établir de recommandation possible pour l’implantation d’un stimulateur cardiaque en dehors d’un trouble de conduction patent(7). L’implantation d’un défibrillateur est recommandée en prévention secondaire, chez tous les sujets ayant fait une mort subite récupérée et chez les patients avec TV soutenues mal tolérées(8). En prévention primaire, son indication passe par l’évaluation du risque de mort subite qui est essentielle chez les patients ayant une CMH (Cf. évaluation des facteurs de risques) (tableau 2).
En ce qui concerne la réduction septale, elle est réservée aux patients qui restent symptomatiques malgré un traitement optimal. On peut dans certains cas opérer ces patients pour réduire l’hypertrophie septale et c’est la méthode classique. Une nouvelle méthode de réduction de l’hypertrophie septale est apparue, il s’agit de l’alcoolisation intracoronaire du myocarde septal, qui est une alternative possible à l’intervention chirurgicale mais il s’agit là d’une technique en évaluation réservée à des centres hautement spécialisés (tableau 3).
Activité physique : laquelle autoriser et chez qui ?
L’activité physique doit être limitée en présence d’une CMH. Il existe un consensus pour interdire le sport en compétition afin de réduire le risque de mort subite. Il est nécessaire de dissuader les adolescents de s’orienter vers une carrière sportive.
Chez des patients asymptomatiques et sans critères de gravité, la pratique de la compétition pourra être autorisée exceptionnellement et après accord des spécialistes dans certains sports (à faible niveau de résistance et d’endurance tels que golf, tir à l’arc).
Chez les « porteurs sains », l’autorisation éventuelle à pratiquer un sport en compétition ne pourra être discutée que collégialement.
Concernant l’activité de loisir, les activités sportives intenses (provoquant un essoufflement significatif) et/ou avec phases d’accélération/décélération sont à prohiber (sprint, tennis, musculation). D’autres activités de loisir (la marche et le golf par exemple) peuvent être autorisées, au cas par cas selon le profil de risque du patient.
Les professions à caractère physique, ou engageant la sécurité en cas de syncope, sont habituellement récusées.
D’autres situations particulières sont envisagées dans le cadre de ces recommandations sur la CMH : insuffisance cardiaque, arythmie, grossesse, prévention d’une endocardite et seront retrouvées par le lecteur sur le site de l’HAS1, www.has-sante.fr, et ou de la SFC www.sfcardio.fr.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :