Focus-ShockWave
Publié le 30 déc 2020Lecture 8 min
Lithotripsie : présent & futur
Benjamin HONTON, Clinique Pasteur, Toulouse
Nous présentons un dossier sur la lithotripsie ou lithotritie intravasculaire en vue du traitement des lésions coronaires calcifiées et très calcifiées, notamment par la technique ShockWave. Cette mise au point est complétée de trucs et astuces et de cas cliniques.
Le présent
Les lésions coronaires calcifiées ont une incidence croissante dans la pratique quotidienne de l’angioplastie coronaire, au regard de l’explosion épidémiologique des facteurs les favorisant, en particulier le diabète. Par ailleurs, les lésions calcifiées sont d’une part sous-estimées en angiographie, mais également corrélées à une augmentation des complications angiographiques, ainsi qu’à un pronostic clinique plus défavorable(1).
Les techniques usuelles de préparation de la plaque calcifiée notamment par athérectomie rotative ont une pénétration faible en France (3 % des procédures) et sont associées à une augmentation des complications perprocédurales. De surcroît, leurs niveaux de preuve clinique d’efficacité restent faibles(2). Si la Société européenne de cardiologie rappelle dans ses dernières recommandations de bonnes pratiques l’importance de la préparation de la lésion avant l’implantation d’un stent sur le résultat à court et long terme de l’angioplastie, elle n’émet pas de recommandation spécifique sur l’utilisation des différents dispositifs (athérectomie, OPN, NC, scoring balloon, etc.), laissée à l’appréciation de l’opérateur(3).
Le cathéter de lithotripsie coronaire
Le cathéter de lithotripsie intravasculaire (IVL) ShockWave C2 développé par la société Schockwave Medical Inc utilise le principe de la lithotripsie pour entraîner des fractures dans la plaque calcique coronaire, afin d’augmenter la compliance du vaisseau et ainsi de faciliter la délivrance et le déploiement des endoprothèses coronaires. Le système ShockWave C2 comprend un cathéter d’angioplastie avec les deux émetteurs de lithotripsie intégrés dans un ballon d’angioplastie, un générateur et un connecteur (figure 1). Le cathéter est un ballon d’angioplastie semi-compliant dans lequel deux émetteurs de lithotripsie sont intégrés dans la section du ballon, qui mesure de façon standard 12 mm de longueur. Ce cathéter est compatible avec un guide monorail 0,014’’, avec une longueur de shaft de 138 cm. Il permet de délivrer des ondes acoustiques circonférentielles depuis les émetteurs sous l’effet d’une impulsion électrique délivrée par le générateur à raison de 1 impulsion par seconde. L’onde acoustique interagit avec les tissus de haute densité comme le calcium et exerce un équivalent de 50 atm sur la plaque calcifiée. Chaque cathéter est capable de délivrer jusqu’à 80 impulsions. Le diamètre des ballons varie de 2,5 à 4 mm avec une incrémentation de 0,5 mm. L’AMM a été obtenue le 18 avril 2017 pour le traitement des lésions coronariennes calcifiées, de novo, avant l’implantation d’un stent. Le générateur est configuré pour reconnaître et prendre en charge les différents types et tailles de cathéters connectés. Il ne peut, pour des raisons de sécurité, être connecté au secteur et au cathéter dans le même temps. Le câble du connecteur relie le générateur au cathéter et comprend un actionneur à distance utilisé pour activer la délivrance d’énergie du générateur au cathéter avec une activation simultanée des deux électrodes.
Figure 1. Cathéter ShockWave C2. Emission d’une onde acoustique par les électrodes de lithotripsie insérées dans le ballon d’angioplastie.
Les données de la littérature
Le programme de développement clinique dans le champ de la maladie coronaire est le programme DISRUPT CAD.
• DISRUPT CAD I
Il s’agit de l’étude pilote évaluant l’innocuité et l’efficacité du système ShockWave dans la préparation des lésions coronariennes calcifiées de novo, avant la pose d’endoprothèse, chez 60 sujets. La progression du cathéter au travers de la lésion a été faisable chez 98,5 % des patients avec un gain luminal immédiat avant endoprothèse de 1,7 mm. L’étude rapporte un faible niveau d’événements cardiovasculaires indésirables majeurs (MACE) de 5 %, uniquement représentés par des infarctus du myocarde sans onde Q à 30 jours. À 6 mois de suivi, 2 décès d’origine cardiovasculaire étaient enregistrés, et 91,5 % des patients ne présentaient aucun événement cardiovasculaire majeur(4).
• DISRUPT CAD II
C’est un registre postmarket évalué dans 15 sites européens(5). Ce registre de 120 sujets a confirmé la grande sécurité d’utilisation avec un taux de MACE hospitalier de 5,8 %, représentés uniquement par des infarctus périprocéduraux. Le critère primaire d’efficacité a été atteint chez 94 % des patients avec notamment un succès de délivrance du cathéter au site de lésion dans l’ensemble de la cohorte. Cependant, si les résultats en termes de sécurité sont indéniables dans cette population de patients avec des lésions complexes, les critères d’efficacité sont discutables car le critère principal retenu était la délivrance du stent avec une lésion résiduelle < 50 % post-stenting, loin de ce qui est attendu en pratique quotidienne.
• DISRUPT CAD III
Cette faiblesse a été partiellement compensée dans l’étude pivot FDA DISRUPT CAD I I I récemment publiée dans le Journal of the American College of Cardiology(6). Cette étude à l’échelle mondiale demandée par la Food and Drug Administration (FDA) a inclus 431 patients dans 47 centres. À la demande de la FDA en raison de l’absence de bras comparatif dans l’étude, les critères primaires d’efficacité (succès procédural) et de sécurité (MACE) ont été évalués à un objectif préspécifié (pre-specified performance goal, PPG) calculé sur les résultats de l’étude ORBIT II (predicate study). Le taux de MACE rapporté à 30 jours était de 7,8 % avec un succès procédural de 92,4 %, chaque critère dépassant très significativement l’objectif statistique préspécifié. Les investigateurs ont scindé la cohorte en deux groupes : le groupe « Roll-in » incluant les premiers cas de chaque centre (n = 47), comparé à la cohorte « Pivotal » (n = 381). L’absence de différence entre ces deux groupes concernant les critères primaires rappelle la facilité d’utilisation du cathéter de lithotripsie en comparaison au système d’athérectomie avec une courbe d’apprentissage rapide. Cette étude apporte également des éclaircissements sur les shocktopics, ces impulsions électriques avec capture ventriculaire visibles sur l’ECG de surface au moment de la délivrance de la thérapie acoustique (figure 2). Dans DISRUPT CAD III, elles ont été rapportées chez 171 patients sans aucune induction d’arythmies ventriculaires soutenues. On peut noter cependant un cas de fibrillation ventriculaire induite, récemment rapportée dans la littérature dans une indication off-label(7).
Figure 2. Activation électrique en ECG surface (IVL spikes) à l’origine d’une capture ventriculaire (VPB) ou shocktopics (© K. Dawkins).
• DISRUPT CAD IV
Cette étude réalisée dans la population japonaise est terminée et les résultats sont en attente de publication.
Les données OCT
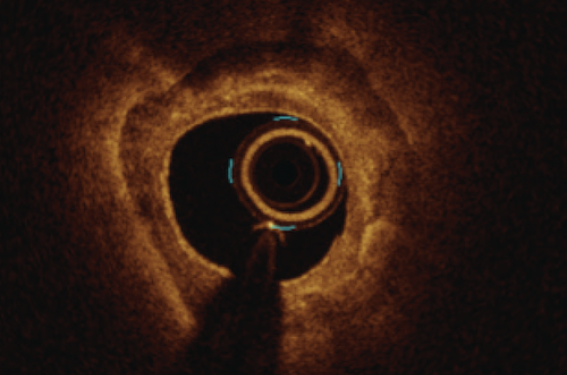
Les ondes acoustiques créent des fractures longitudinales dans la plaque calcique, bien visibles en OCT (figure 3). Dans la sous-étude OCT de DISRUPT CAD III (n = 97), 67 % des patients présentaient des fractures macroscopiques visibles en OCT, dont la largeur augmentait significativement après l’implantation du stent. De façon intéressante, il n’y avait pas de différence en termes de critère primaire entre les patients présentant ou non des fractures de plaque en OCT, confortant l’idée actuelle que la lithotripsie induit également des microfractures non visibles en OCT, comme démontré en micro CT (figure 4). L’absence de fracture macroscopiquement visible en OCT n’est donc pas un critère d’échec de la procédure.
Figure 3. Aspect typique de macrofracture induite par IVL en OCT se majorant après la mise en place des stents.
Figure 4. Aspect de microfractures visible sur artère fémorale superficielle cadavérique en histologie (à droite; A , B) et en micro CT (à gauche ; C, D) (© R. Virmani).
Le futur
Les données cliniques
Toutes les données cliniques publiées dans le programme DISRUPT CAD sont issues de patients très sélectionnés (angor stable, lésion < 40 mm, absence de lésion ostiale et/ou du tronc commun gauche, etc.) et ne reflètent pas notre pratique quotidienne. Plusieurs registres de prise en charge tout venants devraient démarrer en 2021, dont le registre FRANCE LILI, endossé par la Société francaise de cardiologie sous l’égide du GACI. Par ailleurs, persiste la problématique des lésions calcifiées excentriques normalement exclues du programme DISRUPT CAD. Une analyse poolée des patients de DISRUPT CAD I et II inclus avec une lésion calcifiée finalement considérée comme excentrée par un corelab indépendant a été récemment publiée, mettant en évidence un résultat procédural et de sécurité similaire aux lésions concentriques(8). Cependant, il s’agit d’une analyse post-hoc et évaluant un faible nombre de patients, qui nécessite d’être confirmée sur des études dédiées.
Malexpansion de stent
Une des applications potentielles de la lithotripsie est la sous-expansion de stent en rapport avec une préparation insuffisante de la plaque calcique (figure 5). Cette application off-label est maintenant rapportée dans la littérature dans de nombreux cas cliniques et de petites cohortes(9). Les critères de sécurité semblent bons, mais le taux d’efficacité rapporté est moindre que dans les lésions coronaires de novo. Par ailleurs, il existe beaucoup d’interrogations sur l’impact des ondes acoustiques sur le polymère et la structure métallique de l’endoprothèse, ainsi que sur la stratégie à appliquer sur le stent après la lithotripsie dans ces situations (ballons actifs/stents actifs).
Figure 5. Malexpansion de stent sur l’IVA proximale non levée malgré un ballon OPN de 4 x 15 mm, 30 atm (A). Après 80 pulses intrastent au ballon ShockWave 4 x 12 mm et postdilatation au ballon NC de 4 x 20 mm, 16 atm (B).
Les autres applications
L’utilisation de la lithotripsie endovasculaire est également possible dans tous les autres lits vasculaires avec le référencement du cathéter ShockWave M5 pour les axes iliofémoraux et du cathéter ShockWave S3 pour l’atteinte vasculaire jambière. Les caractéristiques techniques de ces cathéters sont différentes du cathéter coronaire C2 (tableau). Ils permettent, notamment pour le M5, de modifier notre prise en charge interventionnelle structurelle en autorisant des approches fémorales pour le TAVI ou les assistances ventriculaires gauches qui n’auraient pas été retenues initialement(10).
Conclusion
L’arrivée de la lithotripsie modifie considérablement le paysage de la prise en charge des lésions calcifiées, introduisant un outil très séduisant pour ces patients avec des lésions complexes.
La lithotripsie se caractérise sans nul doute par une excellente sécurité d’utilisation, avec cependant des données cliniques d’efficacité qui restent à confirmer, notamment dans les populations de patients « tout venant » et dans les malexpansions de stent sur plaque calcifiée.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


