Valvulopathies
Publié le 01 avr 2019Lecture 10 min
Diagnostic et suivi d’une bicuspidie aortique : voir et prévoir
Jean-Luc MONIN, Emmanuel LANSAC, Institut des maladies valvulaires/Montsouris, Paris
La bicuspidie est la malformation congénitale cardiaque la plus fréquente, avec une prévalence estimée entre 1 et 2 % de la population générale et une forte prédominance masculine (3 hommes pour une femme). Cette malformation touche à la fois la valve aortique et l’aorte initiale, qui est dilatée dans la majorité des cas avec un risque significatif d’évolution vers un anévrisme et un sur-risque de dissection aortique. Une bicuspidie doit être recherchée essentiellement dans trois circonstances :
– souffle aortique systolique ou diastolique chez un sujet jeune (en pratique avant 60 ans) ;
– dépistage familial chez les apparentés au premier degré d’un patient porteur d’une bicuspidie, chez qui la prévalence de la bicuspidie est 10 fois plus élevée que dans la population générale ;
– bilan d’un anévrisme de l’aorte initiale, associé ou non à une valvulopathie aortique.
Forme typique/atypique/formes rares
La forme typique de bicuspidie (70 % des cas, figure 1) et liée à un défaut de séparation in utero de la commissure entre les deux sigmoïdes coronaires (bicuspidie droite/gauche), elle est fréquemment associée à une dilatation de l’aorte initiale et plus rarement à une coarctation isthmique. Le raphé peut être complet ou partiel, source de difficultés diagnostiques. La forme atypique de bicuspidie (15 % des cas) comporte un raphé entre les sigmoïdes non coronaire et coronaire droite (bicuspidie droite/non coronaire) (figure 2).
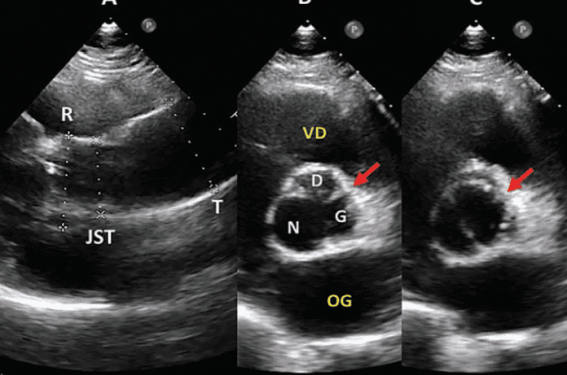
Figure 1. Bicuspidie typique (échographie transthoracique). A.Déformation de l’aorte initiale en incidence parasternale transverse : dilatation modérée de l’aorte tubulaire (diamètre = 41 mm) ; la racine aortique est de diamètre normal à 32 mm. B. Incidence transverse en diastole, noter l’asymétrie entre les trois sigmoïdes avec une sigmoïde non coronaire plus développée. Le raphé entre les sigmoïdes coronaires (flèche rouge) apparaît plus dense qu’une commissure normale. C. Incidence transverse en systole, noter l’ouverture incomplète, arrondie en regard du raphé (flèche rouge). D : sigmoïde coronaire droite ; G : sigmoïde coronaire gauche ; JST : jonction sino-tubulaire ; N : sigmoïde non coronaire ; OG : oreillette gauche ; R : racine aortique ; T : aorte tubulaire ; VD : ventricule droit.
Figure 2. Bicuspidie atypique (échographie transthoracique). Incidence parasternale transverse en diastole (A) et en systole (B). Le raphé (flèche jaune) entre les sigmoïdes non coronaire et coronaire droite est bien visible en diastole et systole. Abréviations : idem figure 1.
Parmi les formes rares de bicuspidie, on peut citer les formes symétriques avec une orientation commissurale proche de 180°, où les 2 sigmoïdes fonctionnelles sont de taille équivalente (type 0 de Sievers, figure 3) ; l’examen attenti f de ces valves notamment lors de la chirurgie révèle le plus souvent un fin raphé sur l’une des sigmoïdes.
Figure 3. Bicuspidie symétrique (type 0 de Sievers) en échographie transthoracique, incidence parasternale transverse en diastole (A) et systole (B). Les deux sigmoïdes fonctionnels sont de taille très proche avec une ouverture commissurale à 180°. Noter la discrète encoche (flèche rouge) correspondant à un raphé très probable, invisible en ETT. Abréviations : idem figure 1.
La classification de Sievers(1) décrite en 2007 reste assez utilisée, elle comporte cependant 2 limites essentielles :
– les bicuspidies de type 0, malgré leur dénomination, comportent un raphé dans la plupart des cas ;
– les bicuspidies de type 2, qui associent généralement un raphé droite/non coronaire et un raphé droite/gauche (figure 4), sont en fait des valves unicuspides dont les risques évolutifs et les possibilités chirurgicales sont très différentes des valves bicuspides. En effet, l’évolutivité valvulaire plus rapide des valves unicuspides amène fréquemment les patients à la chirurgie entre 40 et 50 ans, voire plus tôt. De plus, la fréquence des calcifications valvulaires réduit significativement les possibilités de préservation valvulaire par rapport aux valves bicuspides.
Figure 4. Valve unicuspide, échographie transœsophagienne en diastole (A), et systole selon deux plans de coupe différents (B et C). A. Les trois sinus de Valsalva sont nettement identifiables en diastole. B. Plan de coupe proche du bord libre des sigmoïdes, ouverture valvulaire arrondie et excentrée avec 2 raphés bien visibles (flèches rouges) entre les sigmoïdes droites/non coronaire, d’une part, et droite/gauche, d’autre part. C. Sur un plan de coupe plus proche de la base des sigmoïdes, les raphés sont nettement moins visibles mais l’ouverture valvulaire arrondie est évocatrice d’une valve unicuspide. Abréviations : idem figure 1.
Les éléments du diagnostic
Le diagnostic de bicuspidie repose essentiellement sur l’échocardiographie transthoracique. Ce diagnostic est fortement suspecté sur l’incidence parasternale longitudinale : épaississement anormal des sigmoïdes, ouverture asymétrique avec inversion de courbure « en dôme », fréquemment accompagnée d’une déformation caractéristique de l’aorte initiale (figure 1). L’incidence parasternale transverse permet un examen attentif de la valve aortique sur une vue « en face » : la valve doit être examinée en diastole et en systole, afin d’identifier le ou les raphés, de préciser l’orientation commissurale et la présence d’éventuelles calcifications valvulaires. En cas de doute sur un raphé incomplet, les éléments en faveur d’une bicuspidie sont :
– l’épaississement anormal d’une commissure en diastole (figure 5) ;
– une asymétrie entre les 3 sigmoïdes aortiques : les 2 sigmoïdes intéressées par le raphé (sigmoïde conjointe) étant généralement moins développées que la 3e sigmoïde (figure 1) ;
– une ouverture valvulaire arrondie en regard du raphé, par opposition à l’angle aigu formé par une commissure complètement ouverte (figure 5).
Figure 5. Bicuspidie typique en échographie transthoracique, incidence parasternale transverse avec zoom en diastole (A) et systole (B). Noter l’épaississement du raphé entre les deux sigmoïdes coronaires (flèches rouges) bien visible en diastole et systole avec ouverture arrondie de la sigmoïde conjointe en systole. Abréviations : idem figure 1.
Tous les segments de l’aorte initiale sont généralement dilatés en cas de bicuspidie :
– anneau aortique large, > 25 mm de diamètre chez l’homme ou > 23-24 mm de diamètre chez la femme ;
– la dilatation aortique (> 38 mm ou > 21 mm/m2) prédomine typiquement sur la portion tubulaire ou ascendante (figure 1), liée en partie aux anomalies génétiques des composantes de la paroi et en partie à la lésion de jet du flux d’éjection aortique ;
– plus rarement, on observe une dilatation prédominant sur les sinus de Valsalva (racine aortique) ou une hypoplasie de l’aorte initiale.
La recherche d’une coarctation isthmique par voie suprasternale doit être systématique, notamment dans les bicuspidies droite/gauche qui sont plus volontiers associées à une coarctation.
En cas d’insuffisance aortique pure chez un sujet jeune, associée ou non à une dilatation de l’aorte initiale, l’échographie transœsophagienne est indispensable pour évaluer la possibilité d’une éventuelle chirurgie valvulaire aortique conservatrice.
Le dépistage familial est-il justifié ?
La prévalence élevée de bicuspidie et/ou dilatation de l’aorte initiale chez les apparentés au premier degré d’un patient porteur de bicuspidie a été confirmée par une étude espagnole récente : parmi 724 apparentés de 256 patients, la prévalence de bicuspidie était de 6,4 % (9,2 % chez les hommes et 3,5 % chez les femmes)(2). De plus, une dilatation isolée de l’aorte initiale sans bicuspidie était présente chez 9,6 % des apparentés, prédominant la plupart du temps sur l’aorte tubulaire. D’autres études ont retrouvé une prévalence bicuspidie jusqu’à 10 % chez les apparentés au premier degré, soit 5 à 10 fois plus que dans la population générale. Le dépistage familial est donc justifié en cas de bicuspidie, ceci d’autant plus que le patient et sa famille sont demandeurs. En pratique, il semble logique de dépister les enfants à partir de 10 ou 15 ans, compte tenu d’un diagnostic échographique plus facile à cet âge et d’un pronostic globalement favorable. Le dépistage des ascendants est également logique.
Quels risques évolutifs ?
Deux études contemporaines nord-américaines regroupant au total plus de 1 000 patients permettent de délivrer à nos patients une information globalement rassurante sur les risques évolutifs d’une bicuspidie(3,4).
• Premièrement, l’espérance de vie en cas de bicuspidie est la même que pour la population générale issue de la même région.
• Deuxièmement, le principal risque évolutif est la nécessité d’une chirurgie programmée sur la valve aortique ou sur l’aorte ascendante. La cohorte de la Mayo Clinic regroupe 416 patients diagnostiqués en moyenne à l’âge de 35 ans : après 25 ans de suivi, un patient sur deux nécessite une chirurgie valvulaire aortique et un patient sur quatre une chirurgie de l’aorte initiale(3). L’étude canadienne de Toronto donne des résultats concordants : parmi 642 patients, une chirurgie valvulaire programmée a été pratiquée dans 22 % des cas après un suivi moyen de 9 ans(4). En dernier lieu, la cohorte de la Mayo Clinic a montré que le risque de dissection aortique est multiplié par 8 en cas de bicuspidie, par rapport à la population générale et après 16 ans de suivi en moyenne(3). Le sur-risque de dissection est donc significatif mais il est très éloigné du risque observé dans les « vraies » maladies génétiques comme la maladie de Marfan (risque multiplié par 100). Bien entendu, ces données rassurantes sont sous réserve d’un diagnostic précis et d’une surveillance conforme aux recommandations en cours.
Surveillance clinique/Imagerie
Le rythme de surveillance dépend de la sévérité de l’atteinte valvulaire aortique et de la présence éventuelle d’un anévrisme de l’aorte thoracique. En l’absence de valvulopathie aortique significative ou d’anévrisme aortique, un suivi clinique et échographique tous les 2 ans semble raisonnable. En cas de valvulopathie aortique modérée, les recommandations actuelles sont en faveur d’un suivi clinique et échocardiographique annuel(5). Il en est de même en cas d’anévrisme aortique, défini par un diamètre maximal > 45 mm. En cas de valvulopathie sévère et asymptomatique, un suivi semestriel est recommandé, notamment pour le rétrécissement aortique(5).
Les points clés de la surveillance sont :
– la recherche lors de chaque consultation de symptômes à l’effort, potentiellement liés à la valvulopathie aortique ;
– la recherche répétée d’antécédents familiaux de dissection aortique ou de mort subite inexpliquée avant l’âge de 60 ans ;
– l’écho-Doppler cardiaque est l’examen d’imagerie de première intention, qui permet d’évaluer précisément la sévérité hémodynamique et le retentissement d’une valvulopathie aortique et de mesurer des diamètres de l’aorte initiale dans la plupart des cas ;
– en cas de discordance entre les données échocardiographiques ou en cas d’échogénicité insuffisante (aorte ascendante visualisée sur moins de 4 cm à partir du plan de l’anneau aortique), l’IRM cardiaque est l’examen privilégié, de par son caractère non irradiant et sa précision diagnostique. En effet, l’IRM est actuellement la méthode de référence pour la mesure des volumes et de la fraction d’éjection ventriculaire gauche. Elle permet également un calcul fiable de la fraction de régurgitation aortique en cas d’insuffisance aortique et des mesures précises des diamètres de l’aorte thoracique ;
– compte tenu de son caractère irradiant, l’angioscanner ne doit pas être prescrit de manière répétée, pour éviter un sur-risque de cancer, notamment chez les patients jeunes. L’angioscanner cardiaque est aortique garde sa place lorsque les diamètres aortiques sont proches des seuils justifiant une intervention chirurgicale et dans le cadre d’un bilan préopératoire.
Indications opératoires
En cas de valvulopathie aortique sévère, les indications opératoires sont globalement les mêmes, que la valve soit bicuspide ou tricuspide.
Les recommandations actuelles insistent sur l’importance du test d’effort (ECG d’effort) qui doit être réalisé à intervalle régulier, notamment chez les patients actifs, afin d’objectiver l’absence de symptôme à l’effort et de quantifier l’adaptation cardiovasculaire (augmentation de la pression artérielle systolique à l’effort)(5).
Rappelons que l’échographie d’effort n’a plus d’indication en pratique courante pour la surveillance des patients asymptomatiques compte tenu du peu d’études disponibles actuellement, dont les résultats sont contradictoires(5). En cas d’anévrisme de l’aorte initiale sans indication de chirurgie valvulaire aortique, la chirurgie l’aorte est indiquée si le diamètre maximal > 55 mm chez les hommes de gabarit standard(5). Ce chiffre est probablement à moduler chez les patients de petit gabarit, notamment les femmes, bien qu’aucun seuil ni aucune valeur indexée à la surface corporelle ou à la taille ne figure dans les recommandations sur ce point, à l’exception du syndrome de Turner (indication opératoire en cas de diamètre aortique > 25 mm/m2, notamment en cas de bicuspidie associée). Le seuil chirurgical est abaissé à 50 mm chez les hommes en cas d’anévrisme sur bicuspidie associé à d’autres facteurs de risque de dissection, notamment les antécédents familiaux de dissection ou mort subite inexpliquée, l’hypertension artérielle et la coarctation isthmique(5). En cas d’indication opératoire sur la valve aortique, un remplacement de l’aorte initiale est indiqué sur les segments dont le diamètre dépasse 45 mm(5).
Chirurgie valvulaire aortique conservatrice
En cas d’insuffisance aortique isolée chez un patient jeune (en pratique jusqu’à 60-65 ans), plusieurs études récentes sont en faveur d’une meilleure qualité de vie et d’une meilleure survie à moyen terme en cas de chirurgie conservatrice valvulaire aortique par comparaison au remplacement valvulaire prothétique(6,7). Plus précisément, les patients susceptibles de bénéficier de ce type d’intervention doivent avoir une insuffisance aortique pure, associée ou non à un anévrisme de la racine aortique, sans rétraction ni calcification valvulaire. Les recommandations européennes de 2017 recommandent d’adresser ce type de patient dans un centre expert médico-chirurgical susceptible de réaliser une chirurgie conservatrice valvulaire aortique(5).
En pratique
Une valve aortique bicuspide comporte un unique raphé, plus ou moins complet, située le plus souvent entre les 2 sigmoïdes coronaires : on parle de bicuspidie typique ou bicuspidie droite/gauche (70 % des cas). La forme atypique de bicuspidie comporte un raphé entre les sigmoïdes coronaire droite et non coronaire (15 % des cas). Les formes rares comportent essentiellement les valves symétriques, avec orientation commissurale proche de 180° (ancien type 0 de Sievers) et les exceptionnels raphés gauche/non coronaire.
En présence de 2 raphés, il s’agit d’une valve unicuspide dont le potentiel évolutif et les possibilités chirurgicales sont très différentes par rapport aux valves bicuspides. Le diagnostic positif et la surveillance des patients ayant une bicuspidie reposent essentiellement sur l’examen clinique et l’écho-Doppler cardiaque. En cas de données échographiques discordantes de visualisation insuffisante de l’aorte ascendante, l’IRM cardiaque doit être privilégiée compte tenu de son caractère non irradiant. L’angioscanner cardiaque et aortique est généralement réservé au bilan préopératoire.
En l’absence d’indication valvulaire aortique, un remplacement chirurgical de l’aorte ascendante est indiqué en cas d’anévrisme > 55 mm de diamètre pour les hommes de gabarit standard. Le seuil est abaissé à 50 mm en cas de bicuspidie associée à d’autres facteurs de risque : antécédents familiaux de dissection ou mort subite inexpliquée, HTA ou coarctation. Des seuils plus bas doivent être considérés chez les femmes ou en cas de petit gabarit.
Les patients jeunes ayant une insuffisance aortique isolée, associée ou non à un anévrisme de l’aorte initiale, doivent être adressés de préférence à un centre expert médico-chirurgical afin de pouvoir éventuellement bénéficier d’une chirurgie valvulaire aortique conservatrice.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :







