Publié le 16 fév 2018Lecture 13 min
Cardiomyopathies aux anthracyclines : prévention et traitement
Pierre GIBELIN, CHU de Nice

L’action antitumorale des anticancéreux exercent des effets secondaires sur les tissus sains de l’organisme. Si certains effets délétères sont communs à la plupart des antimitotiques (nausées, vomissements, aplasie médullaire, alopécie), les effets indésirables au niveau cardiaque sont souvent l’apanage de quelques agents, notamment les anthracyclines.
La cardiotoxicité liée à la chimiothérapie est en augmentation du fait, d’une part, du vieillissement de la population, d’où une association plus fréquente de cancer et de maladies cardiovasculaires, d’autre part, d’une meilleure efficacité du traitement anticancéreux.
En effet, les survivants à un traitement de tumeurs solides ou hémopathies ont augmenté très fortement depuis 20 ans. Ainsi les atteintes cardiaques ont augmenté parallèlement. De même, de nombreux traitements associés de traitements adjuvants favorisent l’atteinte cardiaque, ainsi que la radiothérapie associée.
Le problème est important et on conçoit l’intérêt du bilan cardiologique dont l’objectif est la recherche d’une dysfonction myocardique avant le traitement (détection des sujets à risque) pendant la chimiothérapie et à distance du traitement pour assurer une prise en charge spécialisée aussi optimale que possible.
Définition de l’atteinte cardiaque
Il n’y a pas de définition universelle. L’European Association of Cardiovascular Imaging et l’ASE retiennent une chute de 10 % de la FEVG avec une FEVG < 50 %. Mais Cardiac Review and Evaluation Commitee retiennent une chute de 5 % avec une FEVG < 55 % si signes cliniques et 10 % sans signes cliniques ; enfin la FDA est plus exigeante et propose une chute de 20 % si la FEVG de départ est normale et de 10 % si elle est < 53 %.
Fréquence
Les incidences sont très variables selon les études et les doses. En effet, l’incidence varie de 3 à 48 % pour la doxorubicine : 3 à 5 % pour 400 mg/m2, 7 à 26 % pour 550 mg/m2 et 18 à 48 % pour 700 mg/m2 (dose cumulative totale, DCT, conseillée 550 mg/m2), de 1 à 11 % pour l’épirubicine (DCT conseillée 900 mg/m2), de 5 à 18 % pour l’idarubicine (DCT conseillée 90 mg/m2) et 2 % pour l’anthracycline liposomale (dose > 900 mg/m2).
Cardinale et coll. (Circulation 2015) nous renseignent de manière plus précise : sur une étude portant sur 2 625 patients traités par anthracyclines suivis tous les 3 mois pendant 1 an, puis tous les 6 mois pendant 4 ans, puis tous les ans, l’incidence était de 9 %(9,7 % cancer du sein ; 6,2 % autres) dont 81 % en classe I/II NYHA. Au total, 98 % des atteintes se produisaient dans la première année (temps moyen entre début chimiothérapie et CMD : 3,5 mois).
Prévention
Détection des patients à risque
(tableau)
Facteurs de risque liés aux malades
• L’âge : les sujets jeunes semblent plus vulnérables de même que les personnes âgées.
• Le sexe féminin : à dose cumulée identique, les femmes sont plus à risque que les hommes.
• Les facteurs génétiques : probable mutation concernant le métabolisme du fer par exemple. Les sujets trisomiques 21 et les Noirs américains sont à risque accru.
• La durée du suivi : les effets du temps écoulé depuis l’arrêt du traitement constituent un facteur de risque essentiel.
• Des antécédents cardiovasculaires : la préexistence de maladie cardiaque est sous-estimé.
Dans une étude observationnelle monocentrique, Schmidinger et coll. ont étudié les patients programmés pour une chimiothérapie. Ils ont analysé les facteurs de risque de la maladie coronarienne, les antécédents cardiovasculaires, les troubles du rythme, l‘HTA et les signes ou antécédents d’insuffisance cardiaque.
Les auteurs retrouvent des antécédents cardiovasculaires dans 9,3 % des cas avec 5,8 % d’infarctus du myocarde, 7 % d’insuffisance cardiaque, 3,5 % des troubles du rythme et 3,5 % d’HTA non contrôlée. De nombreux patients ont des facteurs de risque cardiovasculaire : HTA (48,8 %), une hypercholestérolémie (26,7 %), un diabète (22 %), une hypertriglycéridémie (12,8 %).
Ainsi il faut insister sur la détection des patients à risque avant chimiothérapie à savoir :
– les patients avec une FEVG < 50 % asymptomatiques ;
– insuffisance cardiaque à FE altérée ou conservée ;
– coronaropathie : antécédent d’infarctus, d’angor, de pontage, de stent ;
– valvulopathie modérée à sévère ;
– antécédents d’AVC ou d’AIT ;
– antécédents de thromboembolie ;
– HTA répondant mal aux traitements et/ou avec HVG ;
– troubles du rythme sévère ;
– cardiomyopathie hypertrophique, restrictive dilatée ;
– facteurs de risque : diabète, hypercholestérolémie, tabac, obesité, alcool.
De tels patients ont un risque élevé de développer une cardiotoxicité.
L’évaluation du profil cardiovasculaire par le cardiologue doit être pris en considération par l’oncologue afin de décider du type de thérapeutique et du mode d’administration individualisé : dose administrée lors de chaque session, la dose cumulée, les horaires, le mode d’administration, l’association de plusieurs médicaments et un suivi optimal (par exemple : évaluation de la FEVG : 2 à 4 semaines, 3 ou 4 mois, et à 6 mois après le début du traitement et la fin de la cure). Un registre national a été mis en place par le groupe insuffisance cardiaque de la SFC pour déterminer la fréquence des cardiopathies et facteurs de risque chez les patients devant avoir un traitement par les anthracyclines et/ou trastutumab (ce registre a débuté en juin 2017).
Facteurs de risque liés aux traitements
• Dose totale cumulée : en effet, il existe une augmentation exponentielle de l’incidence de la cardiopathie toxique avec l’augmentation de la dose cumulée.
Si la probabilité d’apparition est inférieure à 10 % pour des doses cumulées en deçà de 550 mg/m2 le risque croît considérablement pour des doses supérieures. Ces données ont conduit à considérer la dose de 550 mg/m2 de doxorubicine comme la limite supérieure à ne pas dépasser. L’épirubicine parait moins toxique. La tendance actuelle des oncologues est d’utiliser des doses bien moindres d’anthracycline.
Il existe une grande variation inter individuelle quant à la sensibilité cardiaque aux anthracyclines.
• Mode d’administration : il est préférable de faire des perfusions de produit sur une période prolongée.
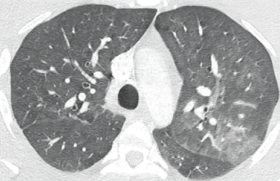
• Irradiation médiastinale : cette association peut majorer la toxicité cardiaque aux anthracyclines, de même que l’association avec d’autres anticancéreux : mitoxantrone, mitomycine, cyclophosphamide, melphalan, vincristine, actinomycine, bléomycine, trastuzumab.
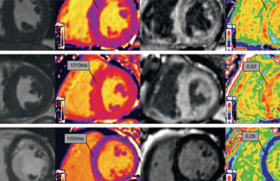
Détection précoce de la dysfonction VG
Monitoring de la fraction d’éjection
C’est de loin le paramètre le plus utilisé. Celle-ci est habituellement évaluée par l’échocardiographie. La FEVG est le meilleur facteur pronostique. La fréquence et la méthode d’évaluation de la FEVG (échocardiographie, scintigraphie, IRM…) n’est pas clairement précisé dans les recommandations internationales.
Cependant cette méthode a montré une mauvaise sensibilité diagnostique et une faible valeur prédictive pour les formes paucisymptomatique.
Toutes les modalités de l’échocardiographie pour l’évaluation de la FEVG doivent être utilisé : 2D simpson, 3D, contraste, écho de stress.
Autres indicateurs échocardiographies
• Paramètres diastoliques
L’altération des paramètres diastoliques survient avant l’atteinte de la fonction systolique évaluée par la FEVG. De nombreuses études ont montré que les anthracyclines altèrent les paramètres diastoliques mesurées en échographie tel que le rapport E/A, le temps de décélération de l’onde E (TDE) et la relaxation isovolumétrique. D’autres études ont montré des résultats identiques avec le DTI avec la mesure de E’ et du rapport E/E’. Toutefois, une atteinte précoce de la fonction diastolique n’a pas de valeur prédictive du développement ultérieur d’une cardiotoxicité avec altération de la fonction systolique. Sawaya et coll. (2011) sur un suivi de 6 mois n’a pas pu montrer une valeur prédictive d’une atteinte de la fonction systolique.
• Strain et strainrate
Cette technique permet d’évaluer les déformations longitudinale, radiale et circonférentielle ; la plus étudiée étant la déformation longitudinale. La FE ou FR évalue la fonction ventriculaire gauche globale. Il peut être important d’étudier la dysfonction régionale qui peut précéder la déformation globale. De plus, la FE dépend de la pré- et de la postcharge.
Les paramètres de déformation sont moins sensibles aux variations de charge. Sawaya en 2011 et 2012 a démontré que le strain longitudinal prédit le développement d’une cardiotoxicité chez les patients traités par les anthracyclines et trastuzumab.
On retiendra avec les recommandations de l’ESC 2016 une réduction relative de la déformation longitudinale globale (GLS) > 15 % par rapport à la déformation de base. Ces résultats restent à confirmer car il existe une grande variation de la norme en fonction des appareils utilisés pour la mesure.
• Biomarqueurs
• Troponines (Tn) : deux grandes études ont montré l’intérêt du dosage de la troponine I effectuées par l’équipe de Cardinale. La plus récente a étudié 703 patients pour évaluer l’impact pronostique de l’élévation des troponines. Les résultats sont les suivants :
– patients qui ont leur Tn I normale après chaque cure et après la fin du traitement (n = 495) (1 mois après) ont un risque très faible d’événement cardiovasculaire (< 1 %) ;
– patients qui ont une élévation de la Tn I après chaque cure et à la fin du traitement (n = 63) ont un risque élevé d’événement cardiovasculaire (84 %) ;
– patients qui ont une élévation de la Tn I après chaque cure mais qui revient normale à la fin de la cure de chimiothérapie ont un risque intermédiaire (37 %).
Des résultats voisins sont retrouvés avec le trastuzumab.
• BNP/NT-proBNP : les natriurétiques ont été utilisés comme biomarqueurs, leur intérêt dans la détection précoce de la toxicité cardiaque des chimiothérapies est en cours d’évaluation avec des résultats contradictoires.
Au total, même si les biomarqueurs ont montré des résultats contradictoires, ils ont également montré leur potentiel à prédire une cardiotoxicité. Leur valeur prédictive négative est importante. L’élévation de la troponine peut prédire l’évolution vers une dysfonction VG, sélectionne les patients pouvant bénéficier d’un traitement préventif et définit un groupe à surveillance rapproché et prolongé.
Traitement préventif
La meilleure prise en charge de tel patient consiste en la prévention de l’atteinte cardiaque. Diverses approches ont été réalisées avec des résultats contrastés.
Administration des anthracyclines
• Discussion onco-cardiologique.
• Réduction de la dose cumulée.
• Durée et fréquence d’administration : perfusion en continu > 6 h, 3 fois par semaine, avec préférence pour l’épirubicine.
• Forme liposomale : encapsulation de l’anthracycline dans le liposome.
• Traitement alternatif.
• Traitement séquentiel pour l’association avec le trastuzumab.
Traitement médicamenteux
Actuellement, les résultats les plus intéressants, du moins chez l’enfant, sont ceux obtenus avec la dexrazoxane (Cardioxane®) chélateur intracellulaire du fer. Combiné le traitement par anthracycline et dexrazoxane peut être particulièrement utile chez l’enfant. Parmi les enfants traités pour sarcome, Wexler et coll. Ont trouvé une meilleure tolérance cardiaque quand les deux sont associés, et ceci permet d’utiliser des doses cumulatives plus élevées sans effet secondaire (410 vs 310 mg/m2). Néanmoins ce traitement a des effets secondaires : infection, fièvre, plus grande incidence de la myélosuppression.
L’indication actuelle concerne les adultes présentant un cancer du sein avancé ou avec métastases qui a déjà reçu des doses de doxorubicine de 300 mg/m2 ou 540 mg/m2 d’épirubicine et qui doit bénéficier d’une nouvelle cure d’anthracyclines.
• + IEC
L’étude de Cardinale a montré l’effet préventif d’un traitement systématique par les IEC chez les patients à risque, à savoir ceux qui reçoivent une forte dose d’anthracycline et dont le taux de troponine s’est élevé pendant les cures de chimiothérapie.
L’étude a porté sur 114 patients divisés en 2 groupes : l’un traité par les IEC (enalapril 20 mg/j ; n = 56) et l’autre non traité par IEC (n = 58).
Le début du traitement s’est fait 1 mois après la première cure de chimiothérapie et a été poursuivi pendant 1 an. On note une diminution significative de la FEVG dans le groupe non traité alors que celle-ci ne bouge pas dans le groupe traité et l’incidence du critère primaire (chute de plus de 10 % de la FE) est plus élevée dans le groupe non traité (43 vs 0 % ; p < 0,001).
• + Bêtabloquants
La même année, l’équipe de Kaley a étudié l’effet d’un traitement systématique par les bêtabloquants sur un petit nombre de patients traités par les anthracyclines.
Vingt-cinq patients étaient mis sous carvedilol (12,5 mg/j pendant 6 mois) contre 25 patients non traités. À 6 mois, les résultats sont parlants :
– dans le groupe carvedilol, la FEVG était similaire (70 vs 69 % avant et 6 mois après traitement) alors qu’elle était diminuée dans le groupe non traité (68,9 vs 52,3 % ; p < 0,001). Des résultats identiques ont été obtenus pour le diamètre VG et la fonction diastolique.
D’autres études ont été faites mais toujours sur de petits échantillons. Ainsi ces résultats doivent être confirmés.
• + IEC et bêtabloquants
Récemment, l’étude OVERCOME a étudié 90 patients présentant une hémopathie maligne traités par anthracyclines (36 leucémies aiguës et 54 autres hémopathies malignes). Tous les patients avaient une FEVG normale avant chimiothérapie. Ces patients ont été divisés en 2 groupes randomisés : un groupe traité par enalapril 8,5 ± 5,6 mg/j plus carvedilol à 23,8 mg/j à la fin de l’étude. L’âge des patients était de 50 ans avec 43 % de femmes. Après 6 mois de surveillance échocardiographique, les auteurs n’ont pas constaté de différence significative de la FEVG dans le groupe traité alors qu’ils ont constaté une diminution significative dans le groupe non traité : -3,1 % pour l’ensemble (p = 0,03) et -6,3 % (p < 0,01) pour les leucémies (plus d’anthracyclines).
Ces traitements ont donc fait leurs preuves, en particulier pour les IEC chez les patients à haut risque, mais il reste à prouver leur intérêt à titre systématique.
De nombreux autres traitements ont été utilisés : statines, aspirine, amlodipine, sildenafil, ARA 2.
Traitement
Le traitement de la cardiomyopathie toxique en tant que telle repose sur les mêmes principes que celui des insuffisances cardiaques chroniques « classiques » : IEC, bêtabloquants, antagoniste des récepteurs de l’aldostérone. Le pronostic péjoratif attaché à la cardiopathie toxique aux anthracyclines s’est amélioré grâce à l’utilisation de ces classes thérapeutiques.
L’équipe de Cardinale a publié un important travail sur le traitement des cardiomyopathies aux anthracyclines. Ils ont inclus 201 patients consécutifs avec une FE < 45 % due à une cardiomyopathie aux anthracyclines. Une dose progressive d’enalapril (2,5 à 20 mg/j) et chaque fois que possible carvedilol (3,12 à 25 mg 2/fois par jour) a été mise en place aussitôt que la détection de la dysfonction ventriculaire gauche a été constatée. La FEVG a été mesurée avant le traitement puis tous les mois pendant 3 mois et tous les 3 mois pendant 2 ans et tous les 6 mois par la suite (suivi moyen 36 ± 27 mois). Les patients ont été considérés comme répondeurs quand la FE a augmenté au-dessus de 50 %, répondeurs partiels quand la FEVG a augmenté de plus de 10 % mais sans atteindre les 50 % pendant le suivi et non répondeur quand la FEVG augmente de moins de 10 % et n’atteint pas les 50 %.
Au total, 85 patients (42 %) sont répondeurs, 26 patients (13 %) sont répondeurs partiels et 90 patients sont non répondeurs (45 %) ; ainsi une récupération complète ou partielle est survenue chez plus de la moitié des patients.
Le pourcentage de répondeurs décroît progressivement avec l’augmentation du temps entre la fin de chimiothérapie et le début du traitement.
L’analyse multivariée montre que seul (avec la classe NYHA) le temps entre fin de cure et début du traitement est un facteur indépendant prédictif d’une récupération complète de la FE (OR : 3,9, IC95% : 2,7-5,7 ; p < 0,0001 pour chaque doublement du temps).
Les auteurs retrouvent une diminution de chance de récupération de la FE multipliée par 4 pour chaque doublement du temps entre fin de cure et début du traitement.
Le pourcentage de patients avec une récupération complète de la FE est de 64 % chez ceux traités dans les 2 premiers mois après la fin de la cure. Ce pourcentage décroît progressivement avec le temps et dévient nul 6 mois après. Après 12 mois, la possibilité d’une récupération même partielle de la FEVG est nulle.
Ces résultats soulignent l’importance de débuter un traitement le plus précocement possible après la détection de l’atteinte myocardique. Ainsi les auteurs insistent sur l’importance d’une détection précoce de la dysfonction systolique même chez les patients asymptomatiques.
Oncologue et cardiologue doivent travailler en collaboration étroite.
Ces résultats ont été confirmés par une étude plus récente et plus large déjà citée plus haut (Circulation 2015) sur les 2 625 pts traités par anthracyclines suivis pendant 3 mois pendant chimiothérapie et pendant la 1re année, tous les 6 mois pendant 4 ans puis tous les ans.
La définition de la toxicité était une diminution de FE de 10 points avec une FE < 50 % (début du TRT) et la définition de la récupération était :
– partielle : augmentation de la FE de 5 points et > 50 % ;
– totale : FE retrouve la FE de départ.
Les patients bénéficiant du traitement par IEC ± bêtabloquants ont une récupération de 82 % (temps moyen 8 mois) avec 11 % de récupération complète et 71 % récupération partielle.
Les patients qui ne récupèrent pas ont une NYHA plus élevée, une intolérance au traitement et plus d’événements cardiovasculaires. L’analyse multivariée de non-récupération retrouve la FEVG en fin de chimiothérapie et la dose cumulée d’anthracyclines.
Des recommandations ont été publiées en 2012 par le groupe de travail ESMO clinical practice guideline.
Ces recommandations pour les anthracyclines sont basées sur la surveillance ou non par la troponine (on sent l’influence de l’équipe de Cardinale dans ces recommandations). En effet si le dosage de la troponine est faite à chaque cycle quand celle-ci devient positive un traitement par les IEC est recommandé (symptomatique ou non). Par contre, si celle-ci n’est pas pratiquée, une surveillance échocardiographique est faite tous les 3 mois et si la FEVG est atteinte (< 50 %), le traitement par la bithérapie IEC et bêtabloquants est proposé.
Pour la surveillance, les recommandations ESC 2016 propose de faire une échocardiographie toute les 50 mg/m2 ou au-delà de 240 mg/m2 et une surveillance biologique à chaque cycle. Elles proposent un traitement par IEC + bêtabloquants si patients symptomatiques et laissent un point d’interrogation si asymptomatique.
Enfin il faut souligner l’importance grandissante dans les recommandations de la pratique d’exercice en cours de chimiothérapie.
En pratique
La fréquence d’une atteinte cardiaque avant chimiothérapie (patients de plus en plus âgés) reste à évaluer (registre national).
L’importance de la détection des patients à risque : bilan cardiologiqueobligatoire en pré-chimiothérapie : clinique, troponine, échocardiographie avec 2D strain si possible.
L’importance d’une décision conjointe onco-cardiologique pour : évaluer bénéfice/risque, mettre en place une action préventive oncologique (alternative, mode d’administration, forme d’anthracycline, dose cumulée).
Et une action cardiologique : prise en charge des facteurs de risque, traitement préventif ? Traitement dysfonction VG/insuffisance cardiaque, encourager l’exercice physique, faire une surveillance rapprochée.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :