Publié le 04 jan 2021Lecture 6 min
Une cardiopathie hypertrophique pas comme les autres…
Tanios AKIKI, C. CHAMANDI, V. TEA, É. PUYMIRAT, département de cardiologie, USIC, HEGP, Paris
Nous rapportons le cas d’un patient de 39 ans, sans antécédents connus, présentant depuis plusieurs mois une dyspnée d’effort (NYHA II). Il se présente aux urgences pour une hémoptysie de faible abondance (un demi-verre) survenue quelques heures auparavant.
Au moment de la prise en charge, le patient ne montre pas de signe de gravité. Il n’a pas récidivé. L’interrogatoire ne rapporte pas d’étiologie évidente. Le patient pratique le culturisme professionnel depuis cinq ans. Il n’a pas de consommation alcoolotabagique, pas de voyage récent. L’examen clinique est sans particularités.
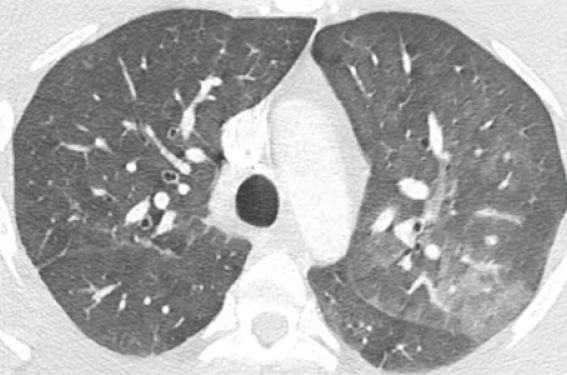
Un scanner thoracique injecté est réalisé retrouvant une image de verre dépoli bilatéral prédominant à gauche (figure 1). L’hypothèse d’une hémorragie intra-alvéolaire motive une admission en pneumologie où est réalisée une fibroscopie bronchique. À l’examen macroscopique, aucun saignement n’est retrouvé. L’analyse du lavage broncho-alvéolaire ne retrouve également aucun stigmate cytologique d’hémorragie intra-alvéolaire récente (ou ancienne) dans le territoire exploré.
Figure 1. TDM thoracique.
Un bilan complémentaire est réalisé, comprenant :
– un bilan auto-immun (FAN, AAN, ANCA) : négatif ;
– un bilan rénal : rapport protéinurie/ créatininurie à 0,101 g/ mmol sans insuffisance rénale ni hématurie associée ;
– et une échographie thoracique devant un aspect d’hypertrophie ventriculaire à l’ECG retrouvant un VG hypertrophié, une FEVG 40 % avec une hypokinésie globale (figures 2 et 3).
Figure 2. ECG.
Figure 3. Résultats de l’échocardiographie. Un ventricule gauche non dilaté (DTDVG 64 mm soit 27 mm/m2), hypertrophié (SIV 15 mm, PP 15 mm) avec une fraction d’éjection FEVG à 40 % sur une hypokinésie globale modérée. L’aorte initiale est non dilatée. La valve mitrale est fine non sténosante présentant une fuite minime. L’oreillette gauche est modérément dilatée, mais les pressions de remplissage ventriculaire gauche sont non augmentées. La valve aortique est tricuspide, non fuyante, non sténosante. Le débit cardiaque préservé 7 l/min soit 3 /min/m2. Les cavités droites sont de dimensions normales avec une bonne fonction systolique longitudinale du ventricule droit.
Le patient est alors transféré en cardiologie pour le bilan de cette probable cardiopathie hypertrophique du sportif.
En reprenant l’interrogatoire, le patient ne rapporte pas de mort subite dans sa famille ou de personne suivie pour une cardiopathie. Il avoue en revanche prendre des substances « non autorisées » pour augmenter sa masse musculaire. Il s’agit de stéroïdes anabolisants pris de manière intermittence (2 mois - 3 fois par an) associant :
– trenbolone (75 mg 3 fois par semaine) ;
– propionate (100 mg 4 fois par semaine) ;
– drostanolone (100 mg 3 fois par semaine) ;
– clenbutérol (entre 80 et 200 mg par jour selon son planning).
Une IRM cardiaque est réalisée et confirme la présence d’une cardiopathie hypertrophique majeure non obstructive (CMHNO) avec une masse non indexée de plus de 400 g, un rapport masse sur volume > 2, et une masse indexée à 170 g/m2. L’atteinte est homogène. Il n’y a pas d’argument pour une maladie de Fabry ou une amylose (absence de rehaussement tardif) (figure 4).
Figure 4. Résultats de l’IRM cardiaque. La présence de cardiopathie hypertrophique majeure avec une masse non indexée de plus de 400 g, un rapport masse sur volume > 2, et une masse indexée 170 g/m2. L’atteinte est homogène. Il est important de vérifier l’absence de maladie de Fabry ou d’une amylose. Cette dernière est cependant peu probable, car il ne semble pas exister de rehaussement tardif.
Le bilan a été complété par le dosage enzymatique de l’alpha galactosidase, électrophorèse des protéines sériques et les chaînes légères, le dosage de la cortisolémie à jeun, une cortisolurie des 24 h et un test au tétracosactide (Synacthène®) à visée étiologique (résultats non concluants).
Le coroscanner est normal. Enfin, l’échocardiographie d’effort confirme une CMHNO au repos et à l’effort avec une FEVG à 50 %. Absence d’argument pour une ischémie et pour une hyperexcitabilité auriculaire et ventriculaire. Le profil d’effort est adapté.
Au cours de son hospitalisation, la télémétrie n’a pas révélé de troubles du rythme.
Le diagnostic final retenu est celui d’une CMH secondaire à la prise de stéroïdes anabolisants.
L’arrêt des stéroïdes anabolisants et de la pratique du culturisme lui a été recommandé et une prise en charge psychologique lui a été proposée. Un traitement antiarythmique par bêtabloquants lui a été prescrit. Après discussion, nous n’avons pas retenu l’indication à la pose d’un défibrillateur, notamment en raison du caractère potentiellement réversible de ces lésions cardiaques. Une IRM de contrôle est prévue dans 6 mois.
Toxicité des stéroïdes anabolisants
Les stéroïdes anabolisants androgènes (SAA) sont des dérivés synthétiques de la testostérone qui ont été initialement développés à la fin des années 1930. Ils sont approuvés pour traiter le syndrome de dépérissement dans l’infection par le virus de l’immunodéficience humaine, l’hypogonadisme, anémie accompagnant une insuffisance rénale et médullaire, l’endométriose et le cancer.
Les SAA sont également utilisés comme produit dopant chez les sportifs et ont été associés au décès d’athlètes professionnels célèbres. Les SAA les plus utilisés sont le décanoate de nandrolone, la méthandiénone, le stanozolol, l’androstérone et l’androstane.
Les SAA sont utilisés illégalement par certains athlètes en raison de leurs propriétés anabolisantes. En plus de l’accroissement de la masse musculaire, certains stéroïdes comme la nandrolone sont réputés pour améliorer la confiance en soi, exacerber l’agressivité, et diminuer les douleurs articulaires liées à l’entraînement intensif.
Toutes les grandes organisations sportives professionnelles interdisent l’utilisation des SAA.
La toxicité des SAA dépend de la molécule utilisée, de la dose et de la durée d’exposition. Bien que les effets secondaires soient rares aux doses thérapeutiques, les « athlètes » utilisent généralement 5 à 15 fois les doses cliniques recommandées de SAA dans le but de majorer leurs effets sur la masse musculaire et la performance athlétique. À ces doses, les effets indésirables comprennent la suppression dose-dépendante de la fonction testiculaire, la gynécomastie, et l’hépatotoxicité. Les effets cardiaques et métaboliques sont peu clairs, bien qu’il y ait des rapports alarmants de morbidité et de mortalité cardiovasculaires. De plus, les athlètes abusent souvent du SAA pendant des années, aggravant ainsi le potentiel des effets secondaires.
Les anabolisants augmentent la synthèse des protéines, l’assimilation des protéines alimentaires et la masse musculaire en association avec l’entraînement. Ils ont des effets secondaires hydroioniques, hématologiques, métaboliques et myocardiques. Ils aboutissent à une activation du métabolisme lipidique : augmentation du cholestérol total, du LDL, des triglycérides et diminution du HDL.
Au niveau myocardique, les anabolisants mènent à une désorganisation des myofibrilles, gonflement mitochondrial, lésions structurelles focalisées de nécrose et de fibrose. L’effet d’hypertrophie myocardique est encore controversé.
Il est important de noter que les récepteurs myocardiques à la testostérone sont nombreux. Le récepteur spécifique aux androgènes permet à la testostérone de médier la trophicité des cardiomyocytes à l’état physiologique et probablement aussi dans l’hypertrophie adaptatrice. Ce qui peut expliquer l’apparition d’hypertrophie ventriculaire dans les surdosages aux anabolisants.
L’utilisation à long terme des SAA semble être associée à une hypertrophie myocardique, à une athérosclérose coronarienne accélérée et à une altération du VG au strain longitudinal global (GLS), suggérant un dysfonctionnement systolique cardiaque infraclinique des années après l’arrêt des SAA. Ces formes de phénotypes cardiovasculaires indésirables associés au SAA pourraient représenter un problème de santé publique auparavant méconnu.
Chaque cardiologue est concerné par les substances dopantes et leurs effets ; à tout moment de sa pratique, il peut être confronté à l’effet secondaire cardiaque d’un produit dopant dont la prise ne sera pas forcément avouée.
La découverte d’une cardiopathie hypertrophique chez un sujet jeune sportif doit faire évoquer une prise d’anabolisants qu’il faut éliminer dans le cadre de la recherche étiologique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :