Publié le 20 sep 2016Lecture 10 min
Thrombophilie et maladie thromboembolique veineuse
M. CAZAUBON, Secrétaire générale de la SFA, Paris
La maladie thromboembolique veineuse résulte de l’interaction de plusieurs facteurs, connus depuis R. Virchow(1) : lésion de la paroi veineuse, stase sanguine et anomalies de la coagulation.
Définitions
La maladie thromboembolique veineuse résulte de l’interaction de plusieurs facteurs, connus depuis R. Virchow(1) : lésion de la paroi veineuse, stase sanguine et anomalies de la coagulation.
Ces dernières ont été particulièrement mises en lumière au cours du siècle dernier, avec une coopération dynamique entre médecins cardiovasculaires et hémostasiens.
Le terme de thrombophilie biologique regroupe les anomalies constitutionnelles ou acquises de la coagulation qui induisent un état d’hypercoagulabilité et prédisposent à la maladie thromboembolique veineuse (MTEV). Nous limiterons cette mise au point aux thrombophilies biologiques constitutionnelles :
• déficits en inhibiteurs de la coagulation : antithrombine (AT) protéine C et protéine S (PC et PS) ;
• polymorphismes génétiques : facteur V (facteur V Leiden, FVL), prothrombine (facteur II G20210A).
Quant à l’entité maladie thromboembolique veineuse, elle regroupe la thrombose profonde et superficielle des membres supérieurs et/ou inférieurs et l’embolie pulmonaire.
Prévalence des principales thrombophilies biologiques et risque relatif de MTEV
Le tableau 1 reprend la prévalence des thrombophilies dans la population générale et chez les patients avec un épisode de MTEV ainsi que le risque relatif de premier accident thromboembolique veineux et de récidive(2).
Le polymorphisme du facteur VL est le plus fréquent des facteurs de risque génétique de MTEV avec une prévalence de 2 à 10 % dans la population générale (moins fréquent dans les pays du Sud) et de 20 % chez les patients avec un premier épisode de MTEV. La forme hétérozygote est nettement plus fréquente que l’homozygote, avec un risque relatif de MTEV nettement moindre (7 vs 80).
Le tableau 1 révèle aussi que le risque de récidive après un premier épisode de MTEV chez les porteurs d’une thrombophilie est relativement modéré, données qui se sont constituées au fil des années depuis les premières recherches de thrombophilie et qui vont influencer notre conduite à tenir.
Le risque relatif d’accident thromboembolique veineux chez les porteurs d’une anomalie acquise de la coagulation dépend aussi du contexte clinique et des facteurs de risque thromboembolique associés. Il est particulièrement majoré chez la femme enceinte ou en postpartum et lors de la prise d’un traitement estroprogestatif ou TSH.
L’association de plusieurs anomalies génétiques augmente aussi le risque relatif (tableau 2)(3).
D’après ces données on peut donc répondre aux indications de la recherche d’une anomalie biologique de la coagulation.
Tableau 1. Prévalence et risque relatif de MTEV (1er épisode et récidive).
Tableau 2. Risque relatif de METV.
TSH : traitement substitutif hormonal. FVL : mutation du facteur V Leiden.
Quand rechercher une anomalie génétique de la coagulation ?
En prévention primaire ?
La question a souvent été posée chez la femme jeune sans antécédent de MTEV avant la prescription d’un traitement estroprogestatif. Les recommandations de la HAS 2015 sont claires et nettes :
Pas de dépistage systématique de la thrombophilie avant une primo-prescription de contraception hormonale combinée (CHC)(4).
Cette affirmation repose sur la faible incidence de la MTEV chez les femmes sous CHC (de 5 à 12 pour 10 000 femmes par an, selon le type de contraception utilisée), sur le rapport bénéfice/risque de la CHC qui reste positif, et sur l’absence d’études de haut grade portant sur le dépistage systématique de la thrombophilie avant prescription de CHC.
En revanche, chez les femmes sans antécédent de MTEV mais avec antécédents familiaux (parents, fratrie ou enfants) de thrombose veineuse ou de thrombophilie confirmée, une recherche de thrombophilie avant prescription de CHC peut être envisagée au cas par cas(4).
En cas de découverte d’une thrombophilie, la contraception est contre-indiquée et une consultation associant le gynécologue et l’hémostasien est hautement justifiée pour trouver la méthode contraceptive à adopter.
Chez la femme enceinte sans antécédent de MTEV mais avec antécédents familiaux de MTEV ou de thrombophilie, la recherche de thrombophilie est discutable s’il s’agit de FVL ou FII20201A hétérozygotes (avec un grade C dans (5)). Elle est recommandée (grade B) dans les autres thrombophilies (déficit en AT, PS, PC, ou FVL et FII20201A homozygotes ou associés), car elle modifie la conduite à tenir pendant la grossesse et surtout en postpartum (voir plus bas).
En prévention secondaire, après un premier épisode de MTEV
Premier impératif : savoir si la thrombose veineuse est idiopathique (non provoquée) ou pas. Le Groupe d’étude sur l’hémostase et la thrombose (GEHT) et la Société française de médecine vasculaire (CFMV)(5) proposent cette classification des circonstances déclenchantes :
• Circonstances déclenchantes majeures : immobilisation plâtrée ou fracture du membre inférieur ou alitement pendant plus de 3 jours, survenus dans les 3 mois précédents ou cancer actif dans les 2 ans précédents.
• Circonstances déclenchantes modérées ou mineures : grossesse et postpartum, contraception estroprogestative ou traitement hormonal substitutif en cours, voyage en avion (de plus de 6 heures).
En dehors de ces situations on parle de thrombose idiopathique.
À retenir : le caractère non provoqué est un facteur de risque confirmé de récidive (RR : 2,8).
En cas de premier épisode de MTEV non provoquée, il est recommandé d’effectuer une recherche de thrombophilie (grade C)(5). Elle se fera avant, si possible, ou après l’arrêt du traitement anticoagulant. Il est recommandé de restreindre les explorations de laboratoire au diagnostic de déficits en inhibiteurs (AT.PC.PS), aux polymorphismes génétiques FVL et FIIG20210A (grade C) et au diagnostic du syndrome des antiphospholipides (SAPL).
La notion d’âge intervient : selon les recommandations françaises, en cas de premier épisode de MTEV survenant après 60 ans, il est recommandé de ne pas effectuer de recherche de thrombophilie (grade B).
La notion de grossesse intervient aussi mais on ne dispose pas d’études randomisées et contrôlées permettant de donner des recommandations de haut grade. C’est donc au cas par cas et en équipe (gynécologue, hémostasien, angéiologue) que se prendront les décisions de prescrire ou non un traitement antithrombotique prophylaxique.
Pour illustrer ces recommandations, voici quelques observations cliniques.
CAS CLINIQUES : MTEV grossesse et thrombophilie
Premier cas
Une jeune femme de 30 ans se présente avec un antécédent de thrombose surale gauche survenue il y a 3 ans après un voyage en avion (6 heures) alors qu’elle était sous pilule. Il n’y a pas de notion de bilan de l’hémostase à la recherche d’une anomalie biologique de la coagulation (thrombophilie biologique). Dans les antécédents familiaux, on ne retrouve pas de notion de thrombophilie clinique ( MTEV) ou biologique.
Actuellement, elle est enceinte de 5 mois, et se plaint de douleurs des deux membres inférieurs justifiant la consultation angéiologique. L’examen écho-Doppler est normal, aucune séquelle de la thrombose gauche en particulier.
• Quelle est la conduite à tenir ?
Doit-on prescrire un traitement anticoagulant par HBPM à dose préventive ? À partir de quand et jusqu’à quand ? Est-ce que la recherche d’une thrombophilie biologique modifie cette attitude thérapeutique ? Le résultat de l’écho-Doppler et en particulier l’existence – ou non – de séquelles de thrombose veineuse profonde et/ou superficielle modifie-t-il la conduite à tenir ?
• Réponses
1. Chez cette jeune femme, l’antécédent thrombotique sous pilule justifie la mise en route d’un traitement anticoagulant prophylaxique par héparine de bas poids moléculaire (HBPM).
2. Il aurait pu être instauré dès les premiers mois.
3. Il doit donc être débuté dès ce jour et sera poursuivi au moins 2 mois en postpartum(7).
4. Associé à la compression médicale par chaussettes, bas ou collants (recommandation de classe A ).
5. La recherche d’une thrombophilie biologique ne se justifie pas car la mise en évidence d’une anomalie de la coagulation ne changerait rien à la conduite à tenir(7).
6. S’il existait des séquelles échographiques du premier accident thrombotique veineux, a fortiori siégeant sur des veines profondes proximales, poplitée, fémorales et iliaques, cela viendrait renforcer la décision de prescrire un traitement par HBPM préventif, même en l’absence de recommandation formelle dans ce contexte. Ce paramètre est de plus en plus étudié.
C’est dire l’importance d’un bilan échographique réalisé par un médecin vasculaire chez la femme enceinte avec antécédent de MTEV.
S’il n’y avait pas d’antécédent de MTEV, mais la notion d’un facteur VL hétérozygote, le risque de MTEV est considéré comme modéré : on peut retarder la mise au traitement par HBPM à dose prophylaxique et ne le commencer qu’en postpartum, pour une durée de 6 semaines. Cela repose sur les recommandations 2012 de l’ACP(6).
Deuxième cas
Il s’agit d’une femme enceinte sans antécédent personnel de MTEV, mais porteuse du FVL ou FII20210A homozygote, et avec antécédents familiaux de MTEV.
Il existe selon Bates et al. (6), une recommandation de grade 2B :
– pour une prophylaxie pendant la grossesse avec HBPM à dose préventive ou intermédiaire ;
– et pour une prophylaxie en postpartum pendant 6 semaines à dose préventive ou intermédiaire (ou AVK avec INR entre 2 et 3).
S’il n’existe pas d’antécédent familial de MTEV, la surveillance clinique s’impose pendant la grossesse, mais le traitement prophylaxique reprend sa place dans les 6 semaines suivant l’accouchement (grade 2 B).
En cas de FVL ou FII20210A hétérozygote, la surveillance angéiologique s’impose pendant toute la grossesse, en particulier s’il existe des facteurs de risque de la MTEV (immobilité, obésité, âge de plus de 35 ans, maladie veineuse chronique sévère).
Place des antécédents familiaux de MTEV et/ou de thrombophilie constitutionnelle
On a vu qu’ils guidaient la conduite à tenir mais avec la nécessité de respecter plusieurs règles :
• être certain de l’antécédent de MTEV, ce qui n’est pas toujours évident en l’absence de documents ;
• connaître avec précision et certitude le type de thrombophilie (ne pas se contenter d’un « je crois qu’il existe une anomalie génétique »…) ;
• ne prendre en compte que les antécédents familiaux de premier degré (enfants, parents, fratrie).
Utilité de la recherche d’une thrombophilie génétique en cas de thrombose veineuse superficielle
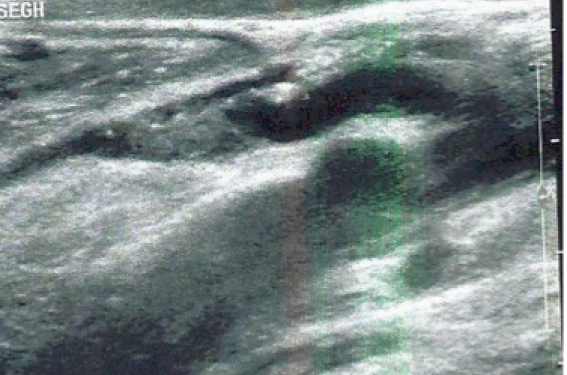
La question se pose principalement si la thrombose veineuse superficielle survient sur des veines saines (non variqueuses, VNV) (figures 1 et 2) ou sur veines variqueuses (VV).
Dans la série de J.-L. Gillet(8), la fréquence des thrombophilies, et en particulier de la mutation hétérozygote du facteur V Leiden, est de 50 % dans le groupe des VNV versus 15 % dans celui des VV. Leur prévalence n’était pas plus grande dans le groupe avec TVS associée à une TVP que dans les TVS isolées.
Mais il existe peu d’études, donc pas de recommandations de haut grade en faveur de la recherche d’une anomalie génétique de la coagulation et aucune donnée permettant de décider du traitement (durée, posologie) en fonction de l’existence ou non d’une thrombophilie (5).
Figure 1. Thrombose de la petite saphène (veine saine) sur tout son trajet.
Figure 2. Limite supérieure de la thrombose de la veine petite saphène (TVS sur veine saine).
La survenue d’une thrombose superficielle au décours d’un traitement endoveineux (sclérothérapie ou laser) peut inciter à la recherche d’une thrombophilie. Ceci pourrait avoir en particulier un intérêt chez la femme jeune souhaitant une grossesse, et a fortiori si elle a des antécédents familiaux thrombotiques ou thrombophiliques (voir plus haut).
Les pièges du bilan d’hémostase
Cliniques
• pas de certitude sur les antécédents familiaux de MTEV ou de thrombophilie
• pas de certitude sur l’existence d’une MTEV chez le patient
Laboratoire
• Pendant un épisode de MTEV aigu : s’attendre à une diminution de l’AT, PC et PS
• Sous héparine : s’attendre à une diminution de l’antithrombine
• Sous antivitamine K : s’attendre à une diminution des PC et PS
• Idem avec les anticoagulants oraux directs
• Chez la femme enceinte : diminution de la PS
Conclusion
• Pas de recherche de thrombophilie chez la femme enceinte, au cours d’un épisode TEV aigu ou lors d’un traitement anticoagulant par héparine ou AVK
• Attendre 2 à 4 semaines après l’arrêt du traitement anticoagulant.
Conclusion
Après un engouement et une recherche quasi systématique d’anomalies biologiques de la coagulation devant tout épisode de maladie thrombo-embolique veineuse et/ou chez les membres d’une famille de patients porteurs d’une anomalie biologique de la coagulation, les études menées conjointement entre épidémiologistes, cliniciens, médecins cardiovasculaires et spécialistes de l’hémostase ont conduit à une attitude beaucoup plus raisonnable et raisonnée.
Chez un patient présentant une thrombose veineuse profonde des membres inférieurs, non provoquée, la demande d’explorations de la coagulation vient après l’interrogatoire personnel et familial, l’examen clinique et les explorations vasculaires, en pesant au cas par cas le rapport bénéfice/risque de la découverte d’une éventuelle anomalie génétique. C’est chez la femme jeune enceinte ou en souhait de grossesse, a fortiori si elle a ou si elle a eu une thrombose veineuse, que l’existence d’une thrombophilie intervient le plus sur la conduite à tenir.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :