Publié le 31 déc 2014Lecture 13 min
Diagnostic et prise en charge de la cardiomyopathie hypertrophique - Les recommandations 2014 de la SEC
A. HAGÈGE, Département de cardiologie, HEGP, Paris
Les précédentes recommandations concernant la cardiomyopathie hypertrophique (CMH) datent de 2003 (ACC/ESC) et de 2011 (ACC/AHA). Depuis, les progrès de la génétique et de l’imagerie ont rendu nécessaire la rédaction de ces nouvelles recommandations, révolutionnaires pour certaines d’entre elles, notamment en ce qui concerne la prise en charge du risque de mort subite. Elles sont accessibles en ligne sur http://eurheartj.oxfordjournals.org/lookup/ doi/10.1093/eurheartj/ehu284.
Définition : HVG inexpliquée en imagerie de coupes
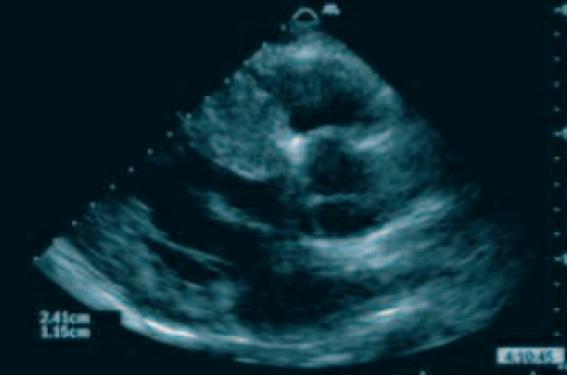
Chez l’adulte, la CMH est définie par la présence d’une augmentation de l’épaisseur pariétale d’au moins un segment myocardique ventriculaire gauche ≥ 15 mm, mise en évidence par n’importe quelle technique d’imagerie (échographie, IRM ou scanner), et non expliquée uniquement par les conditions de charge cardiaque.
L’épaisseur maximale en diastole de la paroi du ventriculaire gauche doit être mesurée sur des coupes bidimensionnelles à la base, en médioventriculaire et à l’apex.
Pour le dépistage familial chez l’adulte, un seuil ≥ 13 mm est exigé. Chez l’enfant, un épaississement pariétal ventriculaire gauche ≥ 2 déviations standards au-dessus de la moyenne prédite par l’âge, le sexe, la taille et le poids permettent le diagnostic.
Étiologies : sarcomériques supposées ou démontrées, mais pas seulement
La CMH est le plus souvent due à une mutation morbide sur un gène codant pour une protéine du sarcomère cardiaque, mutation retrouvée par l’analyse génétique (40-60 %) ou seulement suspectée sans preuve biologique (25-30 %).
La grande majorité des mutations est située sur les gènes codant pour la protéine C ou la bétamyosine cardiaques.
Dans 5 à 10 % des cas, d’autres étiologies sont retrouvées, avec notamment chez l’adulte des causes génétiques rares (maladie de Fabry, maladie mitochondriale, amylose familiale à transthyrétine [ATTR]), ou non génétiques (amylose sénile, amylose à chaînes légères secondaire à un myélome).
Bilan initial : rechercher les signes évocateurs de maladie de surcharge ou infiltrative
Le bilan initial doit comporter un arbre généalogique, un interrogatoire, un examen clinique, un ECG, des éléments d’imagerie cardiaque et des examens de laboratoire.
L’ensemble permet de faire émerger des signes d’alertes pour une cause non sarcomérique qui va entraîner des examens plus spécialisés. Dans le cas contraire, le dépistage génétique à la recherche d’une mutation morbide sur un des gènes codant pour une des protéines du sarcomère cardiaque, devrait être systématique.
Les signes d’alertes sont les suivants :
Symptômes ou signes cliniques
- anomalies neurosensorielles, orientant vers une maladie mitochondriale ou une maladie de Fabry ;
- atteintes visuelles, orientant vers une maladie mitochondriale, une amylose ATTR ou une maladie de Fabry ;
- syndrome du canal carpien, notamment bilatéral chez l’homme, orientant vers une amylose ATTR ;
- faiblesse musculaire, orientant vers une maladie mitochondriale ;
- ptosis palpébral, orientant vers une maladie mitochondriale ;
- angiokératomes ou hypohydrose, orientant vers une maladie de Fabry.
ECG
- PR court, orientant vers une maladie mitochondriale ou une maladie de Fabry ;
- BAV complet, orientant vers les mêmes étiologies mais aussi l’amylose ;
- microvoltage, retrouvé chez près de 50 % des patients avec amylose AL et 20 % des patients avec amylose ATTR.
Échographie
- HVG concentrique, orientant vers une amylose, une maladie de Fabry ;
- hypokinésie ventriculaire gauche, avec ou sans dilatation cavitaire, orientant vers une maladie mitochondriale, une amylose ATTR, une maladie de Fabry ;
- épanchement péricardique, orientant vers une amylose ;
- hypertrophie du ventricule droit, orientant vers une amylose, une maladie de Fabry ;
- aspect granité du myocarde septal, orientant vers une amylose.
Biologie
Certains dosages biologiques doivent être systématiques, liés à la sévérité de la maladie ou aggravant les symptômes :
- NFS, à la recherche d’une anémie ;
- élévation du BNP ou du NTproBNP ou de la troponine T, de mauvais pronostic ;
- dysthyroïdie ;
- insuffisance rénale.
D’autres peuvent orienter vers une étiologie spécifique :
- dysfonction rénale avec protéinurie (amylose, Fabry, maladie mitochondriale) ;
- cytolyse hépatique (maladie mitochondriale) ;
- élévation des CPK (maladie mitochondriale) ;
- pic monoclonal ou une protéinurie (amylose) ;
- hyperglycémie (maladie mitochondriale) ;
- augmentation des lactates (maladie mitochondriale) ;
- dosage systématique de l’activité intraleucocytaire alphagalactosidase A à la recherche d’une maladie de Fabry chez l’homme de plus de 30 ans (chez la femme, le test n’est pas sensible et la génétique est préférée).
Imagerie et examens complémentaires
Recherche systématique d’une obstruction de repos ou provoquée
L’obstruction intraventriculaire gauche est présente chez environ 60-70 % des patients, soit au repos, soit provoquée. Les tests de provocation doivent inclure la manoeuvre de Valsalva, éventuellement le passage de la position accroupie à la position debout et le test d’effort.
L’obstruction est considérée comme présente si ≥ 30 mmHg et comme cliniquement significative si ≥ 50 mmHg. Il est capital que le mécanisme de l’obstruction (sous-aortique due au SAM, due à une membrane sous-aortique, à des anomalies mitrales, ou médioventriculaire) soit au mieux précisé. Tous les patients doivent avoir systématiquement une échographie Doppler de repos et après manœuvre de Valsalva, voire debout si aucun gradient n’est provoqué par les manœuvres antérieures. Chez les patients symptomatiques chez lesquels le gradient spontané ou provoqué par les manœuvres précédentes reste < 50 mmHg, une échographie d’effort est recommandée afin de dépister un gradient d’effort.
Évaluation systématique de la fonction diastolique à l’échographie
Une évaluation systématique de la fonction diastolique ventriculaire gauche est recommandée : Doppler pulsé transmitral, DTI à l’anneau mitral, flux veineux pulmonaire, pression artérielle pulmonaire systolique, taille de l’oreillette gauche.
IRM cardiaque, conseillée sans être obligatoire
L’IRM cardiaque doit être réalisée par des équipes habituées à ce genre de cardiopathie, et est recommandée dans tous les cas lorsque l’échographie n’est pas optimale. Elle devra aussi être envisagée même chez les patients ayant une échographie de bonne qualité afin de mieux évaluer l’anatomie, la fonction ventriculaire et l’étendue de la fibrose myocardique (clichés tardifs après injection de gadolinium).
L’IRM devrait aussi être envisagée chez les patients ayant une suspicion d’hypertrophie ou d’anévrisme apical, ou suspects d’amylose cardiaque, et peut être aussi prescrite avant thérapeutique invasive (ablation par alcool ou chirurgie).
Scintigraphie osseuse, en cas de suspicion d’amylose
La prescription d’une scintigraphie osseuse est recommandée en cas de suspicion d’amylose ATTR, ces patients fixant de manière très anormale le traceur (99mTC-DPD) au niveau myocardique, de manière très spécifique.
Scanner cardiaque, d’intérêt limité
Le scanner cardiaque n’a d’intérêt qu’en cas d’échographie peu satisfaisante ou de contre-indication à l’IRM.
Holter ECG, de préférence sur 48 heures
Il permet de vérifier l’existence d’arythmies auriculaires ou ventriculaires.
Tests d’effort, avec évaluation de la réponse tensionnelle
L’évaluation à l’effort se fait au mieux par test d’effort cardiopulmonaire (VO2), recommandé dans tous les cas chez les patients sévèrement symptomatiques lorsqu’une thérapeutique agressive (transplantation cardiaque, assistance) est prévue.
Elle devrait également être envisagée chez tous les patients pour évaluer la sévérité le mécanisme de l’intolérance à l’effort, ou avant ablation septale.
En cas d’impossibilité, le test d’effort classique (ECG sur tapis roulant ou bicyclette) peut être utilisé.
Dans tous les cas, il faut mesurer la pression artérielle à l’effort, une élévation anormale (≤ 20 mmHg) ou une chute tensionnelle (≥ 20 mmHg) ayant avant 40 ans une valeur pronostique (mort subite).
Prise en charge des symptômes en cas de CMH obstructive : d’abord les médicaments
La conduite à tenir est basée sur la démonstration d’une obstruction sous-aortique ≥ 50 mmHg, soit au repos, soit à défaut après manœuvre de Valsalva, sinon après passage de la position accroupie à la position debout, ou en dernier recours chez le patient symptomatique par échographie d’effort.
Médicaments
Lorsque le seuil de 50 mmHg est dépassé, les bêtabloquants doivent être prescrits en première intention à la dose maximale tolérée pour améliorer les symptômes chez les patients symptomatiques.
En cas d’intolérance ou de contre-indication le vérapamil à la dose maximale tolérée peut être utilisé.
Le disopyramide à la dose maximale tolérée est recommandé en association au bêtabloquant (ou au vérapamil si ce n’est pas possible) en cas de symptômes persistants.
En cas d’intolérance aux bêtabloquants et au vérapamil, le diltiazem à la dose maximale tolérée peut être utilisé chez les patients symptomatiques.
Chez les patients asymptomatiques ou chez l’enfant, bêtabloquant ou vérapamil peuvent être utilisés lorsque l’obstruction est significative pour réduire les pressions de remplissage ventriculaire gauche.
Les vasodilatateurs artériels et/ou veineux sont contre-indiqués en cas d’obstruction, notamment les dérivés nitrés et les inhibiteurs des phosphodiestérases (sildénafil). La digoxine n’est pas recommandée. Les diurétiques de l’anse ou thiazidiques peuvent être utilisés avec précaution pour améliorer la dyspnée d’effort. Le disopyramide devrait être évité chez les patients avec QT corrigé > 480 ms, glaucome ou adénome prostatique, ou encore traitement concomitant par les drogues augmentant le QT (amiodarone, sotalol), et chez les patients en fibrillation atriale (risque d’augmentation de la fréquence cardiaque).
Ablation septale (alcoolisation, myectomie)
Il ne faut jamais envisager de thérapeutiques invasives chez les patients asymptomatiques, quelle que soit la sévérité de l’obstruction sous-aortique.
Les équipes médico-chirurgicales qui prennent en charge ces patients doivent exercer dans un centre entraîné et travailler en équipe multidisciplinaire.
Avant d’envisager ces thérapeutiques invasives, il faut :
- restaurer le rythme sinusal ou ralentir la fréquence cardiaque en cas de FA ;
- éliminer d’autres causes contribuant/causant la dyspnée (obésité, maladie respiratoire, coronaropathie, anémie, dysthyroïdie, arythmie, effets secondaires des drogues, etc.) ;
- analyser l’anatomie et la fonction de la valve mitrale, notamment à la recherche d’un prolapsus mitral ou d’autres anomalies intrinsèques valvulaires et préciser que le mécanisme de l’obstruction est bien lié au SAM (et non à une obstruction médioventriculaire, une membrane sous-aortique, une sténose aortique, une anomalie d’insertion de pilier mitral, la présence de tissu mitral valvulaire accessoire) ;
- évaluer la distribution et la sévérité de l’hypertrophie, le seuil minimal d’HVG requis pour envisager une ablation étant de ≥ 17 mm.
Ainsi, une ablation septale n’est envisageable que si :
- dyspnée d’effort sévère (NYHA III/IV) (voire syncopes d’effort itératives) sous traitement médical maximal ;
- obstruction sous-aortique de repos ou provoquée ≥ 50 mmHg avec HVG septale haute ≥ 17 mm. La myectomie est préférée à l’alcoolisation septale lorsqu’une autre lésion, notamment valvulaire (mitrale ou des piliers), requiert un geste chirurgical. La plastie mitrale ou le remplacement valvulaire mitral sont à envisager lorsqu’il existe une fuite mitrale modérée à sévère qui n’est pas due au SAM seul, ou lorsque l’épaisseur septale est ≤ 16 mm au niveau du contact SAM-septum.
Pacemaker DDD
La mise en place d’un pacemaker DDD peut être envisagée chez des patients sélectionnés avec gradient de repos ou provoqué ≥ 50 mmHg, en rythme sinusal, sous traitement médical maximal, en cas de contre-indication à l’ablation ou de risque élevé de BAV complet après ablation, ou encore en cas d’indication à la mise en place d’un défibrillateur cardiaque.
Prise en charge des symptômes en cas de CMH non obstructive : tout est basé sur la FEVG
Il s’agit des patients symptomatiques sans obstruction sous-aortique significative, spontanée ou provoquée (< 50 mmHg) :
- en cas de fibrillation atriale, il faut en première intention, soit ramener le rythme sinusal, soit ralentir le rythme cardiaque (éventuellement en utilisant de faibles doses de digoxine) ;
- en l’absence d’arythmie, tout dépend de la fraction d’éjection ventriculaire gauche (FEVG) :
• FEVG ≥ 50 % : le traitement est celui des formes obstructives (bêtabloquant, vérapamil, diltiazem, diurétique à faible dose),
• FEVG < 50 % : le traitement est celui de l’insuffisance cardiaque systolique (bêtabloquant, IEC, antialdostérone, diurétique à faible dose), complété éventuellement par la mise en place d’une resynchronisation ventriculaire en cas de bloc de branche gauche avec QRS large ≥ 120 mm ;
- quelle que soit la FEVG, chez les patients très symptomatiques, la transplantation cardiaque peut être envisagée.
Prise en charge des arythmies atriales : anticoagulant au long cours dans tous les cas
• L’utilisation du score CHA2DS2-VASC pour calculer le risque thromboembolique, toujours élevé en cas de CMH, n’est pas recommandée.
• La mise sous anticoagulant par voie orale (AVK, INR cible 2-3) est recommandée même en cas de FA paroxystique, même lorsque le rythme sinusal est restauré.
• Lorsque les AVK ne peuvent pas être utilisés (INR instable, impossibilité de faire des INR, effets secondaires des AVK), un anticoagulant oral direct (ou AOD) est recommandé.
• La restauration du rythme sinusal par choc électrique ou drogue doit être envisagée chez les patients ayant une FA récente.
• L’amiodarone doit être envisagée pour maintenir le rythme sinusal après cardioversion.
• Bêtabloquant, vérapamil ou diltiazem sont recommandés pour contrôler le rythme cardiaque des patients restant en FA.
• L’association aspirine et clopidogrel devrait être envisagée lorsque les patients refusent de prendre un anticoagulant oral.
• L’ablation de la FA devrait être envisagée chez les patients qui n’ont pas de dilatation atriale importante, qui ont des symptômes dus à la FA résistante au traitement ou en cas d’impossibilité de prendre des drogues antiarythmiques.
Prévention de la mort subite : calculer en ligne le risque à 5 ans
La prévention secondaire, après mort subite récupérée, par implantation d’un défibrillateur cardiaque automatique (DAI) est systématique après arrêt cardiaque par TV ou FV, ou après TV soutenue spontanée mal tolérée, lorsque l’espérance de vie dépasse 1 an.
En prévention secondaire, l’estimation du risque de mort subite à 5 ans doit être basée sur un index pronostique. Le calcul de ce score est possible en ligne sur le site de l’ESC (http://www.doc2 do.com/hcm/webHCM.html) et inclut l’âge (en années), les antécédents familiaux de mort subite cardiaque (soit avant 40 ans chez un collatéral du premier degré, soit à tout âge s’il s’agit d’une mort subite due à une CMH), l’existence de tachycardies ventriculaires non soutenues (TVNS) au Holter ECG (de préférence sur 48 h), les antécédents de syncope inexpliquée (particulièrement chez les sujets jeunes et dans un délai de 6 mois-1 an avant évaluation) et des paramètres échographiques, dont l’épaisseur maximale de la paroi du ventricule gauche (en mm), la taille de l’oreillette gauche antéro-postérieure (en mm), et le gradient sous-aortique en mm (le plus élevé au repos ou après Valsalva).
Cet algorithme a été établi sur une cohorte d’environ 2 000 patients (109 morts subitement) puis validé sur une cohorte d’environ 1 600 patients (avec 89 morts subites ou chocs appropriés par DAI).
Cette équation ne doit pas être utilisée lorsque l’espérance de vie es t de moins d’un an, avant 16 ans, chez l’athlète de compétition, et chez les patients ayant une cardiopathie hypertrophique d’origine métabolique ou infiltrative.
Le risque de mort subite à 5 ans doit être calculé à l’évaluation initiale, puis tous les 1 à 2 ans.
• En cas de risque faible (< 4 % à 5 ans), le DAI n’est généralement pas indiqué. Cependant, lorsque d’autres facteurs sont présents (fibrose extensive en IRM, chute tensionnelle à l’effort, autres paramètres), il peut être envisagé.
• En cas de risque intermédiaire (4-6 % à 5 ans) le défibrillateur peut être envisagé.
• En cas de risque élevé (≥ 6 %), le défibrillateur doit être envisagé.
En utilisant un seuil de 4 %, un patient est sauvé tous les 5 ans pour 16 défibrillateurs implantés ; pour un seuil de 6 %, il faut implanter 11 défibrillateurs pour sauver une vie à 5 ans.
Génétique : test recommandé chez tous les patients
Chez les sujets atteints :
- le test génétique est recommandé chez les patients chez lesquels on a fait le diagnostic de CMH ;
- il doit être réalisé dans des laboratoires spécialisés dans la maladie ;
- en cas de diagnostic incertain, le test génétique ne doit être réalisé qu’après évaluation spécialisée.
Chez les apparentés du premier degré :
- le dépistage génétique en cascade est recommandé ;
- en cas de dépistage négatif (pas de mutation identique chez le patient), un suivi n’est pas nécessaire sauf en cas d’apparition de symptôme ;
- lorsque le dépistage n’est pas souhaité ou n’est pas possible, évaluation clinique avec ECG et écho doivent être répétées tous les 2 à 5 ans chez les patients n’ayant pas d’anomalie clinique, ECG ou en imagerie.
Chez l’enfant :
- le dépistage doit être réalisé après l’âge de 10 ans par des équipes spécialisées lorsqu’une mutation a été identifiée chez les parents ;
- lorsque le statut génétique n’est pas connu une évaluation ECG écho doit être envisagée tous les 1 à 2 ans entre 10 et 20 ans puis tous les 2 à 5 ans ;
- lorsqu’il y a des antécédents familiaux malins dans l’enfance (mort subite) ou en cas de révélation précoce de la maladie ou encore en cas de symptômes ou lorsque l’enfant pratique des activités physiques inhabituelles, il peut être envisagé avant l’âge de 10 ans.
Suivi : mieux standardisé
• Il doit inclure ECG et échographie tous les 12-24 mois chez les patients stables, et à chaque fois qu’il y a une modification de la symptomatologie.
• Un Holter de 48 h est recommandé tous les 12-24 mois chez les patients stables, tous les 6-12 mois chez les patients en rythme sinusal avec oreillette gauche dilatée ≥ 45 mm, et en cas de palpitations.
• Une IRM peut être envisagée tous les 5 ans chez les patients stables ou tous les 2-3 ans en cas de progression de la maladie.
• Un test d’effort doit être envisagé tous les 2-3 ans chez les patients stables ou tous les ans chez les patients avec aggravation.
• Un test d’effort cardiopulmonaire doit être envisagé tous les 2-3 ans chez les patients stables ou tous les ans chez les patients avec aggravation.
La prise en charge de la femme enceinte, la contraception, ainsi que les conseils généraux de vie au patient sont aussi amplement détaillés.
Figure 1. Prise en charge en fonction du gradient spontané/provoqué.
Figure 2. Algorithme de prévention primaire du risque de mort subite cardiaque (MSC). HVG maximale correspond à l’épaisseur maximale mesurée en imagerie de coupes au niveau de la paroi du ventricule gauche. Sur fond rouge, classe de recommandation et niveau de preuves ; IIa : devrait être envisagé ; IIb : peut être envisagé ; III : n’est pas recommandé ; B : données issues de larges études non randomisées.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :