Testé pour vous
Publié le 31 mai 2011Lecture 7 min
Agrastat® (tirofiban HCL) : nouveau RCP
P. BARRAGAN, Polyclinique les Fleurs, Ollioules
La société HAC Pharma et Iroko nous informe de la modification de l’autorisation de mise sur le marché (AMM) d’Agrastat® (tirofiban HCL) en janvier dernier incluant, en sus des anciennes posologies, la posologie bolus de haute dose pour les patients bénéficiant d’une intervention coronaire percutanée. Par ailleurs, la Société Européenne de Cardiologie a précisé à la fin de l’année 2010 les indications recommandées des antagonistes des récepteurs IIb/IIIa plaquettaires.
Les indications actuelles de la Société Européenne de Cardiologie
IDM ST+
Seule l’utilisation d’un anti- GPIIb/IIIa chez des patients présentant un large thrombus intracoronaire est suggérée (classe IIa pour l’abciximab et l’eptifibatide, IIb pour le tirofiban). Par contre, l’utilisation systématique de ces molécules avant l’hospitalisation et la coronarographie n’est pas recommandée (classe III).
IDM ST-
De même, toute utilisation en amont d’une coronarographie est classée en classe III et seule la mise en évidence d’un caillot angiographique justifie leur indication (classe I pour l’abciximab et IIa pour le tirofiban et l’eptifibatide).
La non-recommandation de l’utilisation préhospitalière dans les STEMI est-elle fondée ?
La métaanalyse de De Luca(1), forte de 13 essais randomisés (de janvier 1990 à décembre 2004) colligeant plus de 27000 patients (dont 47 % dans le groupe abciximab) retrouvait une réduction significative de la mortalité à 1 an chez les patients traités par angioplastie. Deux études plus récentes FINESSE(2) et BRAVE-3(3) dont le design était centré sur l’intérêt d’une administration préhospitalière précoce d’abciximab ont toutes deux échoué à démontrer le bénéfice espéré. Une des critiques majeures formulées à ces deux études, réside dans l’administration tardive d’abciximab, en moyenne plus de 165 minutes après le début des symptômes dans FINESSE (recrutant des STEMI jusqu’à la 6e heure) et 200 minutes dans BRAVE III (incluant des infarctus jusqu’à la 24e heure), le bénéfice éventuellement obtenu par cette recanalisation antiplaquettaire étant largement dépassé par ses effets délétères hémorragiques.
L’essai randomisé en double aveugle On-TIME 2(4) a évalué l’utilisation préhospitalière du tirofiban. Le délai moyen entre le début de la douleur et le début du traitement était de 77 minutes (contre 165 et 200 respectivement dans FINESSE et BRAVE-3).
L’objectif primaire (sus-décalage ST à l’heure) était atteint (p = 0,001) avec un bénéfice clinique net à 1 mois (décès, IDM, revascularisation en urgence, AVC, hémorragies majeures) également en faveur du tirofiban (p = 0,024) et une forte tendance à une moindre mortalité à 1 an (p = 0,051) dans le groupe traité par tirofiban en préhospitalier.
Par ailleurs, le bénéfice du tirofiban a été plus marqué chez les sujets âgés de plus de 65 ans, ceux avec un score Killip ≥ 2 et ceux dont l’infarctus avait été pris en charge très précocement (< 75 min après début des symptômes). On ne peut s’empêcher de penser qu’il existe encore de bonnes indications d’utilisation d’un anti-GPIIb/IIIa en préhospitalier chez des patients vus précocement.
Anti-GPIIb/IIIa après mise en évidence d’un caillot intracoronaire
L’utilisation d’anti-GPIIb/IIIa dans le cadre des syndromes coronaires aigus (ST+ ou ST-) en présence d’un large thrombus intracoronaire, jugée pourtant plus que raisonnable par nos experts européens (classe I ou II), n’a par contre jamais été validée par un essai bien conduit.
À ce jour, seule la technique de thromboaspiration coronaire évaluée dans l’essai randomisé TAPAS(5) a, sans conteste, démontré une réduction significative de la mortalité à 1 an (p = 0,04). Dans cette étude, plus de 90 % des patients des deux groupes, recevaient également des anti-GPIIb/IIIa. Ces deux traitements sont donc nécessairement synergiques et toute utilisation de la thromboaspiration devrait logiquement être associée à l’administration d’un anti-GPIIb/IIIa.
Cette synergie est confirmée par la méta-analyse ATTEMPT(6) montrant que la survie était améliorée uniquement chez les patients traités par anti- GPIIb/IIIa (p = 0,045).
Nouvelle posologie Agrastat® pour les patients bénéficiant d’une angioplastie
L’étude randomisée ouverte, EVEREST(7), concernant des NSTEMI à haut risque a comparé une dose de charge de 0,4 μg/kg/min d’Agrastat® instaurée en amont dès l’unité de soins intensifs, avec un bolus de 25 μg/kg débuté 10 minutes avant l’angioplastie et relayé par une perfusion de 0,15 μg/kg/min.
Un troisième bras bénéficiait d’un bolus de 25 μg/kg d’abciximab débuté également 10 minutes avant l’angioplastie et suivi d’une perfusion d’entretien de 0,125 μg/kg/min.
L’un des deux critères primaires de l’essai, l’incidence de l’élévation des troponines I cardiaques en postprocédure a été significativement réduit chez les patients traités en amont par du tirofiban par rapport aux deux autres bras (figure 1).
En ce qui concerne l’autre critère primaire, la perfusion tissulaire évaluée, entre autres, par échographie de contraste myocardique, a montré un bénéfice meilleur dans le premier bras d’amont par rapport aux deux autres (figure 2).
Cette nouvelle posologie est désormais celle à utiliser exclusivement dans le cadre de l’angioplastie coronaire.
Figure 1. Tous les patients inclus dans EVEREST avaient des taux de Tnlc perprocédure élevés. Les taux de Tnlc après angioplastie étaient significativement plus bas dans le groupe ayant reçu Agrastat® en amont comparativement au groupe Agrastat® en bolus à haute dose (3,8 ± 4,1 vs 7,2 ± 12 ; p = 0,015) et abciximab (3,8 ± 4,1 vs 9,0 ± 13,8 ; p = 0,0002).
Figure 2. Le score à l’ECM était plus élevé dans le groupe ayant reçu Agrastat® en amont comparativement au groupe Agrastat® en bolus à haute dose et abciximab. L’analyse par patient a montré que les patients traités par Agrastat® en amont avaient plus fréquemment un taux de perfusion cellulaire normal à l’ECM que ceux recevant Agrastat® en bolus ou l’abciximab.
Cas clinique
Monsieur K, 29 ans, est directement acheminé par le Samu 83 en salle interventionnelle pour un IDM avec sus-décalage du ST apicolatéral avec miroir inférieur. La douleur, d’abord fluctuante, est permanente depuis 2 heures.
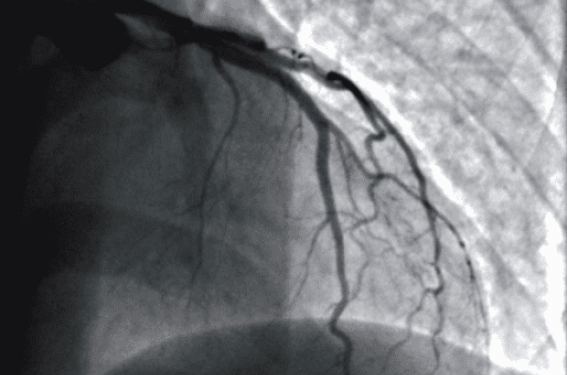
Une coronarographie effectuée 1 an auparavant était normale (photo 1) et avait été motivée par un IDM antérieur inaugural rudimentaire mis en évidence par IRM. L’angiographie coronaire d’urgence retrouve un thrombus occlusif sur le tronc commun (photo 2) et une coronaire droite dominante avec existence d’une circulation collatérale vers l’IVA (photo 3). Le patient est au stade Killip 3.
Une recanalisation est immédiatement démarrée associant une perfusion IV d’Agrastat® (tirofiban HCL) en bolus de 25 μg/kg suivie d’une perfusion de 0,15 μg/kg/min et une thromboaspiration par cathéter Export® (Medtronic).
Le guide 0,014’’ ne peut être positionné que dans le réseau circonflexe. La thromboaspiration ramène de nombreux et volumineux caillots frais. L’impossibilité de franchissement de l’IVA ostiale suggère l’existence d’une occlusion chronique (de moins d’1 an) de l’IVA ostiale ou d’une plaque disséquée de cette dernière. Un stent nu court de 9 mm x 3,5 mm est implanté sur une lésion focale du tronc gauche distal, avec passage en flux TIMI 3 (photo 4).
Une contre-pulsion est mise en place par voie fémorale droite et retirée après 72 heures.
L’évolution hémodynamique est bonne et le patient quitte l’hôpital 1 semaine après son admission avec une FE échographique mesurée à 38 %.
Photo 1. Coronarographie « normale » de mars 2010 après IDM antérieur rudimentaire.
Photo 2. Coronarographie d’urgence en avril 2011 retrouvant un thrombus occlusif sur le tronc commun (flux TIMI 0).
Photo 3. Coronaire droite dominante avec existence d’une circulation collatérale vers l’IVA.
Photo 4. Après thromboaspiration TCG/CX, un stent nu court de 9 mm x 3,5 mm est implanté sur une lésion focale du tronc gauche distal, avec passage en flux TIMI 3. L’IVA ne peut pas être recanalisée.
Testé pour vous
Cette rubrique vise à vous informer sur les matériels les plus récents. L’industriel choisit l’expert qui teste le matériel et la rédaction de CATH’LAB n’intervient pas sur l’information délivrée. Il ne s’agit pour autant pas d’un publi-rédactionnel, l’auteur ayant toute liberté pour s’exprimer.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


