Publié le 26 oct 2004Lecture 7 min
Cardiologie interventionnelle - Une domination des stents actifs
P. COSTE, Hôpital cardiologique, université de Bordeaux 2, Pessac
Le « millésime 2004 » du Congrès Européen de Cardiologie confirme la montée en puissance des stents actifs en cardiologie interventionnelle ; l’extension de leurs indications progresse rapidement. Malgré l’enthousiasme général, certains exigent encore une surveillance à long terme pour dépister un processus de resténose ou de thrombose tardive.
Les nouvelles recommandations de l’ESC pour l’angioplastie seront bientôt publiées ; elles lui donnent une place majeure dans la prise en charge des syndromes coronariens aigus.
Stents à libération de drogues
Les stents à libération de drogues sont toujours dans la course pour prévenir la resténose. Les opérateurs s’enhardissent sur des indications plus complexes, comme les lésions du tronc commun ou les lésions ostiales. Les résultats préliminaires sont acceptables avec des chiffres de resténose entre 20 et 25 % des cas (Colombo 178, 179). On attend maintenant des études comparatives avec la chirurgie cardiaque…
Avec un recul de 300 jours, l’expérience du registre RESEARCH à Rotterdam suggère que l’utilisation du stent actif au sirolimus est possible dans les syndromes coronaires aigus. Il n’y a pas eu d’excès d’événements cardiaques dans les 30 premiers jours qui suivent l’implantation. On observe, en revanche, un effet bénéfique sur le risque de nouvelles revascularisations sur le vaisseau cible (– 79 % pour les infarctus).
Le risque de thrombose précoce est estimé à environ 1,5 % dans les registres communiqués (Goy 1770, Colombo 1779). Néanmoins, certains orateurs ont souligné la fréquence des occlusions tardives au-delà de 6 mois, associées à une inflammation prononcée au niveau des mailles de la prothèse avec parfois un défaut de recouvrement par la néo-intima (van Beseukom 3344). Cette complication inhabituelle avec les stents classiques n’est pas sans rappeler l’expérience malheureuse de la brachythérapie (Virmani).
Quoi qu’il en soit, l’étude européenne E-SIRIUS avoue une bonne évolution à moyen terme pour les 175 patients du bras sirolimus. À 2 ans, il n’y a pas de différence significative entre les deux groupes en termes de mortalité (2,3 vs 2,8 % pour les stents témoins), ou de réintervention après la période des 9 mois qui suivent l’angioplastie.
Enfin et surtout, l’étude ISAR-DESIRE a définitivement validé les stents actifs (sirolimus et paclitaxel) en les comparant au simple ballon pour traiter la resténose intrastent. Le taux de resténoses à 6 mois est de respectivement 14 et 22 % dans les groupes sirolimus et paclitaxel et de 45 % dans le groupe ballon. La différence entre les deux prothèses actives pourrait s’expliquer par le hasard ou par un gain initial plus grand pour le groupe sirolimus. Les auteurs ont donc conclu prudemment que l’étude REALITY apportera prochainement une réponse à cette question (Kastrati).
Autres stratégies de prévention de la resténose intrastent
Les autres stents au revêtement passif sont-ils efficaces sur la resténose ?
Le recouvrement au carbone (étude PREVENT 3839, 3842) semble inefficace dans deux études randomisées ; seul le titane recouvert de monoxyde d’azote aurait un bénéfice à confirmer par d’autres travaux (Billinger 3843).
Traitement pharmacologique par voie générale ?
Suite aux travaux récents de l’équipe de Munich (étude OSIRIS publiée récemment dans Circulation), l’approche associant un stent nu et un traitement oral fait son chemin.
L’équipe italienne de Cernigliaro (1412) confirme la diminution de la prolifération intimale par le sirolimus administré pendant 30 jours par voie orale.
L’étude IMPRESS2, réalisée avec la prednisolone, montre aussi une certaine efficacité (Ribichini 1411), mais à condition de sélectionner les patients ayant une nette réaction inflammatoire 48 h après le stenting (C-reactive protein > 3 mg/l).
Ces stratégies devront cependant être comparées à l’implantation d’une prothèse recouverte du même agent antiprolifératif.
Angioplastie chez le multitronculaire : stent classique ou stent actif ?
Les données à 5 ans de l’étude ARTS-1, qui comparait la chirurgie de pontage à l’angioplastie, montrent que les taux cumulés de mortalité, d’infarctus du myocarde et d’accidents vasculaires cérébraux ne sont pas différents entre les deux groupes (respectivement 4,9 % en chirurgie contre 8,2 % en angioplastie, p = 0,14). Cependant, on remarque une augmentation du taux de réinterventions dans le groupe angioplastie (8,8 % en chirurgie contre 30,3 % en angioplastie, p < 0,0001).
L’étude ARTS-2, réalisée avec le stent au sirolimus, retrouve un bon résultat clinique à 30 jours, et surtout un taux de thromboses précoces de 1,2 % par patient, proche de celui des stents classiques (Serruys P1771).
Angioplastie chez le diabétique : quoi de neuf ?
À la phase aiguë de l’infarctus, il n’y pas d’avantage à implanter systématiquement une endoprothèse classique chez les sujets diabétiques (Timmer 3828).
Néanmoins, en 2004, une étude avec les stents actifs est souhaitable dans cette population à haut risque de resténose et de thrombose. Curieusement, le diabétique traité par insuline aurait un plus mauvais pronostic avec les stents actifs (Paya 3829). De même, le registre français EVASTENT retrouve une mortalité plus importante chez le diabétique avec atteinte multitronculaire après implantation de stent actif au sirolimus. La thrombose de stent serait également plus fréquente dans cette population (Machecourt 2131, 3830).
Heureusement, une analyse rétrospective des études TAXUS vient nous rassurer en confirmant l’intérêt du paclitaxel pour prévenir la resténose des diabétiques, et ce, quelle que soit la longueur du stent (Dawkins).
Les antiagrégants en cardiologie interventionnelle
Nouveautés sur le clopidogrel
La dose de charge de 600 mg a été étudiée et fait l’objet de plusieurs communications.
Dans l’étude de F. J. Neuman, l’effet antiagrégant est acquis dès la 2e heure. On remarque également l’énorme variabilité individuelle de la réponse sur un collectif de près de 1 000 patients (Hochlolzer 2777). L’intérêt d’augmenter la posologie serait d’obtenir une action plus rapide en augmentant la concentration plasmatique du métabolite actif qui est corrélée au degré d’inhibition de l’agrégation plaquettaire (Taubert 2776).
Recommandations 2004 de la Société Européenne de Cardiologie pour la prise en charge de l’infarctus du myocarde avec élévation persistante du segment ST (STEMI : IDM avec sus-décalage de ST ; ACP : angioplastie coronaire percutanée).
Infarctus du myocarde : confirmation de l’abciximab
L’administration d’abciximab dans l’environnement de l’angioplastie primaire fait partie des recommandations de l’ESC (Silber). L’importance d’une administration précoce avant l’intervention est suggérée par deux métaanalyses (Borentain 312, Flather 2400). Néanmoins, des études portant sur des grands effectifs sont encore nécessaires avant d’envisager une administration régulière en préhospitalier. Le délai de prise en charge repositionne l’angioplastie et la fibrinolyse dans les recommandations de l’ESC (figure). Plusieurs communications ont rappelé l’importance du délai d’acheminement du patient au centre de cardiologie interventionnelle (Fernandez-Aviles 304, Masotti Centol 309).
Nouvelles recommandations sur l’angioplastie SCA
Les recommandations 2004 sur l’angioplastie se font un peu attendre. Silber n’a livré que la partie concernant les syndromes coronariens aigus (SCA).
Dans les SCA sans sus-décalage persistant du segment ST, la prescription précoce du clopidogrel devrait être confiée aux médecins en préhospitalier et les héparines de bas poids moléculaires données en première intention dès l’arrivée à l’hôpital. La distinction entre les SCA à haut risque et à bas risque est toujours d’actualité, mais la prise en charge diffère selon la présence ou l’absence d’une structure de cardiologie interventionnelle. La coronarographie doit être faite le plus vite possible en cas de haut risque (< 48 h), mais si l’angioplastie est faite moins de 2,5 heures après les premiers symptômes, l’administration des agents anti-GPII/IIIa — abciximab ou eptifibatide — est proposée uniquement avant l’intervention. Dans le cas contraire, on suggère la perfusion d’agents anti-GPIIb/IIIa en préalable à la coronarographie.
Pour les SCA avec sus décalage persistant, l’angioplastie est le traitement de l’infarctus chaque fois qu’elle est possible dans les 12 premières heures. Lorsqu’on ne dispose pas de l’angioplastie dans un délai de moins de 3 heures, il faut privilégier la fibrinolyse, sauf contre-indication. Au-delà de la 3e heure, le transfert vers l’angioplastie sans fibrinolyse est légitime (figure). Après fibrinolyse, il faut faire une coronarographie dans les 24 heures. Au-delà, la prise en charge sera guidée par l’ischémie myocardique résiduelle évaluée par des examens non invasifs.
La stratégie invasive dans les syndromes coronariens aigus est-elle remise en question ?
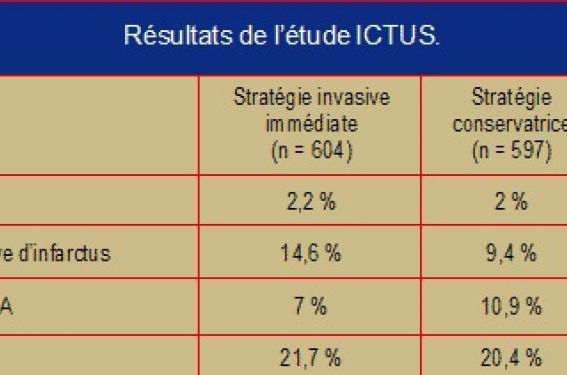
L’étude hollandaise ICTUS ne montre pas de bénéfice à réaliser précocement une angioplastie percutanée ou un pontage chez des patients à haut risque qui présentent un SCA sans sus-décalage persistant du segment ST ; 1 200 patients ont été répartis dans deux bras : revascularisation immédiate (< 24-48 h pour l’angioplastie) ou attitude conservatrice avec stabilisation par un traitement médical moderne, puis coronarographie avec revascularisation seulement en cas de récidive ou d’ischémie à l’épreuve d’effort. Le critère principal, évalué à 1 an, associait décès, infarctus ou réhospitalisation pour SCA.
Globalement, les deux attitudes ne donnent pas de résultats bien départagés avec, dans cette étude, un taux de mortalité à 1 an aux environs de 2 %. Il y a un excès d’infarctus avec la stratégie invasive (14,6 vs 9,4 % ; p = 0,006) et en contrepartie une augmentation du risque de réhospitalisations avec la stratégie différée (10,9 vs 7 % ; p = 0,017). Il est nécessaire, mais aussi urgent, de confirmer ce travail par d’autres études afin d’affiner les critères de définition des sujets « à haut risque ». Curieusement, cet essai comparatif va dans le même sens qu’une métaanalyse récente (Cramer 2030).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :