Rythmologie et rythmo interventionnelle
Publié le 19 avr 2005Lecture 6 min
Présent et futur dans la sélection des patients pour la resynchronisation de l'insuffisance cardiaque
S. GARRIGUE, clinique Saint-Augustin, Bordeaux
Les Journées européennes de la SFC
Pour les cardiologues stimulistes, les années 1990-95 symbolisent l’âge d’or de la stimulation double-chambre (DDD) dans l’insuffisance cardiaque. Que le délai auriculo-ventriculaire soit programmé court ou qu’il soit optimisé pour chaque patient présentant un intervalle PR long, la stimulation DDD permet de réduire l’asynchronisme auriculo-ventriculaire, de diminuer le degré de fuite mitrale dans certains cas (plus spécifiquement en supprimant la part diastolique de la fuite) et de diminuer la précharge en optimisant le temps de remplissage ventriculaire gauche (VG). Cependant, la stimulation DDD conventionnelle présente une limite majeure, celle du site d’excitation ventriculaire situé, dans la grande majorité des cas à l’apex du ventricule droit : l’activation électrique et mécanique VG rétrograde est bien connue pour s’avérer délétère sur le plan hémodynamique aussi bien à court qu’à long terme.
Parallèlement à ces travaux, S. Cazeau et coll. rapportaient en 1994 pour la première fois le bénéfice à court terme d’une stimulation biventriculaire chez des patients en insuffisance cardiaque sévère et bloc de branche gauche (BBG).
Le concept de resynchronisation était de pallier le retard de conduction ventriculaire gauche hémodynamiquement délétère, phénomène que la stimulation ventriculaire droite conventionnelle ne pouvait modifier, voire, dans certains cas pouvait aggraver. Les premières études aiguës objectivèrent des résultats cliniques très encourageants alors que peu d’éléments pouvaient encore préciser le mécanisme exact responsable de l’amélioration observée. Alors, où en sommes-nous aujourd’hui et quels seront les outils de demain ?
De l’électricité vers l’électromécanique
La stimulation biventriculaire a concerné, en tout premier lieu, les patients en insuffisance cardiaque réfractaire au traitement médical et présentant un BBG particulièrement important (QRS > 130 ms). En effet, il existe une corrélation positive entre le temps de régurgitation mitrale, la durée du complexe QRS et l’altération de la dP/dt VG, à tel point que plus le complexe QRS est large, plus la survie est compromise (figure 1).
Figure 1. Courbe de survie de patients insuffisants cardiaques en fonction de la largeur du QRS.
Dès 1992, Xiao et al. ont suggéré que si la largeur des complexes QRS pouvait être réduite, notamment par une solution appropriée de stimulation, on pourrait obtenir une amélioration hémodynamique significative. En produisant deux sources de courant sur les ventricules, Cazeau et coll. ont vérifié cette hypothèse puisqu’ils ont pu affiner la largeur du complexe QRS et améliorer la fraction d’éjection VG.
Ce nouveau concept fut confirmé par des études randomisées multicentriques (MUSTIC, PATH-CHF, MIRACLE, et plus récemment COMPANION). Pourtant, la proportion de patients dits « non-répondeurs » à la nouvelle thérapie électrique fluctue entre 15 et 30 %, avec un effet placebo (stimulateur implanté mais stimulation inactive) pouvant atteindre 38 % d’après l’étude MIRACLE.
Ces derniers résultats amènent une question de poids : pourquoi certains patients à complexes QRS larges ne sont pas améliorés par la stimulation biventriculaire alors que les QRS sont affinés ?
La place de l’échocardiographie
Un bloc de branche gauche suppose un retard électrique conséquent entre l’activation du ventricule droit (VD) et celle du VG. Il a été démontré échocardiographiquement qu’en stimulant simultanément les deux ventricules, le délai électromécanique interventriculaire était significativement réduit (figure 2). Cette observation illustrerait le premier rôle de la stimulation biventriculaire mais peut-être pas le plus important. En effet, trois études récentes, l’une scintigraphique, les deux autres échocardiographiques, rapportent que l’asynchronisme électromécanique intra-VG (figure 3) et non pas interventriculaire, est un facteur de risque indépendant de morbi-mortalité chez les patients insuffisants cardiaques, quelle que soit la largeur du complexe QRS (figure 4). Par conséquent, on peut en déduire que si la stimulation biventriculaire peut réduire l’asynchronisme intra-VG, elle serait bénéfique aussi bien sur les symptômes que sur la mortalité. Si l’on se réfère aux deux études échographiques, celles-ci affirment bien qu’il existe une corrélation significative, certes, mais modérée (r = 0,44 ; p < 0,05) entre la largeur du complexe QRS et la présence d’un asynchronisme intra-VG mais seulement si la largeur du QRS est > à 140 ms. Autre point intéressant est qu’une faible proportion (9–15 %) des patients avec QRS larges ne présentait pas d’asynchronisme intra-VG, cela pouvant expliquer au moins en partie, le pourcentage de non-répondeurs à la stimulation biventriculaire (tableau). Chez les patients insuffisants cardiaques avec des complexes QRS < 120 ms, la présence d’asynchronisme intra-VG fluctue entre 35 et 54 %.
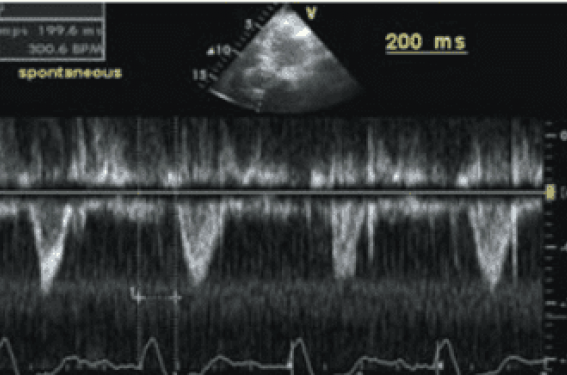
Figure 2. Le délai interventriculaire est la différence entre le temps de prééjection aortique (intervalle entre le début du QRS et le début de l’éjection aortique en mode écho-Doppler) et le temps de prééjection pulmonaire. Dans cet exemple, le délai interventriculaire est de 117 ms avant resynchronisation contre 45 ms après resynchronisation cardiaque (réduction de 260 %).
Figure 3. Exemple de calcul d'asynchronisme intra-VG par échocardiographie (mode TM) entre les pics de contraction systolique des parois septale et latérale. L'asynchronisme est ici considérable (196 ms), la normale étant tolérée jusqu'à 130 ms selon Pitzalis (J Am Coll Cardiol 2002 ; 40 : 1615-22).
Figure 4. Courbe de survenue d'événements cardiaques en fonction du temps chez les patients insuffisants cardiaques (FEVG inférieure ou égale à 45 %) avec et sans asynchronisme intra-VG.
Une équipe italienne a resynchronisé ces mêmes patients à QRS fins et avec asynchronisme intra-VG objectivé à l’échocardiographie. Le résultat est éloquent puisque tous ont été améliorés malgré un élargissement net du QRS (110 ± 11 vs 120 ± 13 ms).
Cependant, sélectionner un patient avec asynchronisme intra-VG plutôt qu’un complexe QRS large ne solutionne pas tout, hélas. Le site de stimulation VG paraît tout aussi important. En 2001, une étude rapporte le fait qu’il existe une amélioration hémodynamique significativement supérieure de la stimulation VG en regard du bord libre en comparaison à la stimulation antérieure. En revanche, les séquences hémodynamiques (dP/dt max VG) consistaient en 6 complexes ventriculaires stimulés, et la différence (en termes de dP/dt VG max) entre stimulation VG-bord libre versus stimulation VG-paroi antérieure était de 7 %. Il paraît difficile de rester catégorique sur la position idéale de la sonde VG comme étant en regard de la paroi libre VG, en se basant sur ces données, certes, encourageantes mais pas décisives. De plus, Ansalone a clairement démontré que l’amélioration la plus significative en termes hémodynamiques, était obtenue en plaçant la sonde VG au niveau de la paroi présentant le délai électromécanique le plus long.
La polémique ne s’arrête pas là puisque deux études récentes viennent compliquer davantage le concept. En effet, pour un même aspect, sur l’ECG de surface de bloc de branche gauche complet, il existe différentes localisations de bloc de conduction fonctionnel selon les patients en insuffisance cardiaque. Certains décrivent un bloc antérieur d’autres sur le bord libre du VG, et enfin en regard de la paroi postérieure VG. Ainsi, un complexe QRS large avec aspect de retard gauche ne présagerait en rien du site du bloc de conduction.
Au-delà de cette analyse, Lambiase et al. suggèrent que stimuler le VG dans une zone de conduction lente crée un « néo-asynchronisme » intra-VG dû à la stimulation épicardique VG, indépendamment de la paroi stimulée.
En somme, il paraît difficile d’être idéalement placé (pour une stimulation biventriculaire optimale sur le plan hémodynamique) si l’on s’en tient uniquement à la stimulation de la paroi libre du VG chez tous les patients. Hélas, il n’y a pas encore de « recette » pratique et universelle, et les méthodes non invasives de localisation de bloc de conduction intra-VG nous font actuellement défaut. Il est sûr en tout cas que des initiatives comme celles de Rudy et coll. sur la cartographie électrique du front d’activation VG à partir d’un ECG de surface à multiples électrodes présagent d’un avenir passionnant et déterminant pour le traitement électrique de nos patients insuffisants cardiaques.
Intérêt de la programmation du délai de stimulation VD-VG dans un pacemaker triple-chambre
Récemment, plusieurs études ont montré que la préexcitation du VG ou du VD dans le cadre d’une stimulation biventriculaire pouvait améliorer davantage la fonction myocardique en comparaison avec la stimulation simultanée des deux ventricules. Seul point délicat, chaque patient doit être individuellement évalué par échocardiographie afin de déterminer le délai de stimulation interventriculaire optimal (figure 5). Cette nouvelle fonction (non encore disponible sur tous les PM triple-chambre), en préexcitant soit le VG, soit le VD, pourrait pallier un site non optimal d’implantation de sonde VG et ainsi réduire davantage le pourcentage de patients non-répondeurs à la stimulation biventriculaire.
Figure 5. Configuration optimale de stimulation multisite ventriculaire en fonction de critères hémodynamiques (débit cardiaque, degré d’insuffisance mitrale). On peut remarquer que la stimulation biventriculaire simultanée était optimale chez seulement 4 patients sur 35.
Conclusion
Les altérations électromécaniques secondaires à la défaillance myocardique ne sont pas superposables aux altérations électriques visibles sur l’ECG de surface. Ainsi, des patients insuffisants cardiaques à QRS larges peuvent ne présenter aucun asynchronisme électromécanique important et donc ne pas répondre à la stimulation biventriculaire qui a pour rôle premier de réduire l’asynchronisme intra-VG, facteur de risque indépendant de morbi-mortalité. Ainsi, l’échocardiographie pèse de plus en plus lourd dans l’évaluation et dans la sélection d’un patient candidat à la resynchronisation cardiaque. C’est elle qui, dans un très proche avenir, évaluera, quantifiera en routine l’asynchronisme intra-VG et finalement déterminera le patient répondeur à la thérapie électrique, indépendamment de la largeur du QRS.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :