Publié le 15 avr 2022Lecture 6 min
Lipides : que peut-on attendre des études en cours ?
Franck BOCCARA, service de cardiologie, Hôpital Saint-Antoine, Sorbonne Universités, Inserm UMR_S938, Centre de Recherche Saint-Antoine, Paris
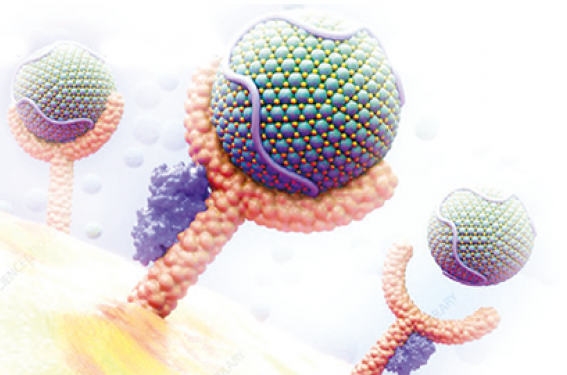
De nouveaux traitements hypolipémiants sont en train d’émerger, en particulier les traitements nés de la biothérapie utilisant des techniques de « mise en silence génétique ». Ces nouvelles molécules sont soit des oligonucléotides anti-sens, soit des petits ARN interférents permettant de dégrader l’ARN messager transcrit pour réduire la production protéique et ainsi réduire le niveau plasmatique de la lipoprotéine cible.
Je parlerai ici de trois cibles lipides qui sont en évaluation par l’intermédiaire de ces nouvelles thérapeutiques. Il s’agit toujours du LDL-cholestérol (LDL-C) via proprotein convertase subtilisin/kexin type 9 (PCSK9), de la lipoprotéine(a) [Lp(a)] et des triglycérides qui sont tous associés à l’augmentation du risque cardiovasculaire.
Le taux circulant de ces lipoprotéines peut être réduit en utilisant cette technique de « mise en silence génétique » en ciblant les protéines qui ont un rôle important dans la production de ces lipoprotéines (par exemple PCSK9, Lp(a) et apolipoprotéines B ou C3).
En utilisant cette nouvelle technologie, le taux plasmatique de ces lipoprotéines peut être réduit de 50 à 90 % grâce à 2 à 12 injections sous-cutanées par an. Des études de phase III sont en cours pour montrer que cette réduction très importante du taux circulant de la lipoprotéine est associée à une réduction de l’incidence des événements cardiovasculaires athérosclérotiques. Ces nouvelles drogues sont délivrées de façon plus efficace en particulier au niveau du foie et des cellules hépatiques, permettant ainsi de réduire les doses de drogues utilisées et in fine de réduire les effets indésirables.
Nous reverrons dans cette mini-revue en particulier des nouveaux traitements ayant pour cible PCSK9, la Lp(a) et les triglycérides (tableau 1).
• Nouveautés dans l’inhibition de PCSK9
Depuis la découverte de l’anomalie génétique gain de fonction du gène de PCSK9 en 2003, de nouvelles thérapies ciblant PCSK9 par des anticorps monoclonaux (alirocumab et évolocumab), ont permis de réduire de 50 à 60 % le taux circulant de LDL-C. De plus, dans les essais cliniques de phase III ODYSSEY et FOURIER, il a été montré une réduction des événements cardiovasculaires en prévention secondaire de 15 % en adjonction au traitement par statine ± ézétimibe.
Ces traitements par anticorps monoclonaux sont injectables et se donnent tous les 15 jours (évolocumab et alirocumab) ou tous les mois (alirocumab).
L’inclisiran (laboratoires Novartis) utilise une nouvelle technique de « mise en silence » de l’ARN messager grâce à l’utilisation de petits ARN interférents. Cette nouvelle technologie de biothérapie utilise un double bras d’ARN messager qui est enrobé dans un carbohydrate — la N-acétylgalactosamine (Gal- NAc) — qui permet d’atteindre le foie et la cible PCSK9 à la surface des cellules hépatiques. Après internationalisation dans le cytoplasme, ce petit ARN interférent est capturé par une machinerie intracytoplasmique intitulée RISC (RNA-induced silencing complex) qui au final va permettre de dégrader l’ARN messager de PCSK9 dans le cytosol et de réduire ainsi la production protéique de PCSK9. Il en résulte une augmentation à la surface des hépatocytes du récepteur au LDL-C et donc une augmentation de la capture intrahépatique du LDL circulant. L’inclisiran injecté par voie sous-cutanée à un mois, 3 mois puis tous les 6 mois permet de réduire d’environ 50 % le taux circulant de LDL-C. Actuellement, une étude de phase III (randomisée en double aveugle), ORION 4, est en cours et a inclus 15 000 patients présentant une maladie athérosclérotique stable (antécédents d’infarctus du myocarde ou d’AVC ou d’artériopathie des membres inférieurs). Cette étude évalue l’effet de l’inclisiran 300 mg par voie sous-cutanée injecté à la randomisation, à 3 mois puis tous les 6 mois versus placebo. Le dernier patient sera suivi jusqu’en juillet 2026. Le critère de jugement principal est un critère combiné associant l’infarctus du myocarde fatal et non fatal, l’AVC et une revascularisation coronaire urgente. Enfin une autre étude de phase III est en cours, l’étude VICTORION-2-PREVENT, qui va aussi inclure des patients présentant une maladie athérosclérotique (infarctus du myocarde, AVC ou artériopathie des membres inférieurs) avec un LDL-C > 0,7 g/l lors de la randomisation sous statine à dose maximale tolérée. Le critère de jugement principal est un critère à 3 points MACE : décès cardiovasculaire, infarctus du myo- carde non fatal et AVC non fatal. Cette étude va durer 6 ans et le dernier patient suivi le sera jusqu’en 2027.
Ces deux études permettront de prouver qu’au-delà de l’efficacité biologique et de la bonne tolérance de l’inclisiran, ce traitement permet une réduction des événements cardiovasculaires en prévention secondaire. Si les deux études sont positives, on passera d’un traitement par voie orale quotidien par statine à des traitements injectables tous les 15 jours à un nouveau traitement injectable tous les 6 mois toujours en association au traitement par statine et ézétimibe.
• Cible thérapeutique la lipoprotéine(a)
Concernant cette cible thérapeutique, il n’existe pas actuellement de traitement spécifique. Seules les anticorps monoclonaux anti-PCSK9 (alirocumab et évolocumab) peuvent réduire de 20 % le taux circulant de Lp(a). Deux molécules sont en cours de développement : l’une en phase II l’olpasiran (laboratoires Amgen) et l‘autre le pélacarsen (laboratoires Novartis) en phase III.
L’olpasiran est une molécule utilisant la technique là encore de petits ARN interférents et permet une réduction importante du taux circulant de Lp(a). Actuellement l’olpasiran est en développement en phase II dans une étude en double aveugle randomisée contre placebo pour réévaluer l’efficacité, la sécurité et la tolérance de ce traitement chez des sujets ayant une élévation de la Lp(a) circulante.
Le pélacarsen utilise la technique d’oligonucléotide anti-sens et est également injecté par voie sous-cutanée. Il cible l’ARN messager de la Lp(a) hépatique, réduisant ainsi la production hépatique de celle-ci. De façon identique à l’inclisiran, pour atteindre le foie, on utilise encore la technique de liaison GalNAc qui sert de ligand pour un récepteur glycoprotéique au niveau des hépatocytes et permet d’internaliser spécifiquement cette molécule dans le foie conjugué au pélacarsen. Cet oligonucléotide anti-sens est ensuite délivré au niveau du noyau, ce qui permet un clivage de l’ARN messager codant pour la Lp(a). Il en résulte ainsi une franche diminution de la production de Lp(a) circulante. Le pélacarsen après un développement de phase II ayant démontré une réduction d’environ 80 % de la baisse de Lp(a) vient de terminer les inclusions d’une étude de phase III (étude HORIZON) qui est une étude randomisée en double aveugle contre placebo évaluant l’efficacité et la tolérance du pélacarsen injectable (voie sous-cutanée) tous les mois chez des patients ayant présenté un infarctus du myocarde ou un AVC ou une artériopathie symptomatique des membres inférieurs. Cette étude HORIZON de phase III répondra dans environ 4 ans à la question du bénéfice cardiovasculaire en prévention secondaire de cette réduction importante de la Lp(a). Enfin l’étude de phase III avec l’olpasiran (étude de réduction des événements cardiovas- culaires) devrait démarrer au dernier trimestre 2021 incluant là encore des patients avec une élévation de la Lp(a) et présentant un infarctus du myocarde.
• Étude évaluant un traitement ayant pour cible des triglycérides
L’évinacumab qui est un anti-corps monoclonal contre ANGPTL3 (laboratoires Regeneron) est en cours d’évaluation chez les patients atteints d’hypertriglycéridémie sévère dans la prévention des récidives de pancréatites aiguës et dans un autre essai de phase III chez les enfants atteints d’hypercholestérolémie familiale. Une étude de phase III randomisée contre placebo a évalué ce nouveau traitement chez des patients atteints d’hypercholestérolémie familiale homozygote. Cette molécule a permis une baisse additive du LDL-C d’environ 50 % après 6 mois de traitement. Une autre étude de phase II en double aveugle contre placebo étudiant l’évinacumab chez des patients présentant une hypercholestérolémie réfractaire, c’est-à-dire des patients ayant ou non une hypercholestérolémie familiale hétérozygote avec un LDL-C > 0,7 g/l, a montré un bénéfice biologique avec une réduction du LDL-C à 4 mois par rapport au placebo d’environ 50 % à la dose maximum de la drogue. Une autre étude présentée à l’ACC en 2021 a montré que l’utilisation de cet anticorps monoclonal a permis chez 51 patients avec une hypertriglycéridémie sévère (triglycéridémie à jeun > 5 g l) de baisser le taux médian de triglycérides d’environ 70 %. Cette drogue pourrait être utilisée chez des patients ayant présenté un premier épisode de pancréatite aiguë secondaire à des hypertriglycéridémies importantes, mais son coût est encore très important et nécessite des études en cours de coût/efficacité.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :