Rythmologie et rythmo interventionnelle
Publié le 15 jan 2021Lecture 6 min
Stimulation cardiaque : quelles nouveautés ?
Romain ESCHALIER, service de cardiologie, CHU de Clermont-Ferrand
Depuis les premières implantations de stimulateurs cardiaques externes puis endovasculaires dans les années 1950-1960, cette discipline a connu de nombreux progrès dans des domaines très variés : compréhensions physiopathologiques, technologiques, techniques d’implantation, algorithmiques. Cependant, certains de ces progrès sont maintenant anciens, et même si la sécurité de ces implantations est excellente, il reste des domaines dans lesquels nous nous devons d’être plus performants.
Nous sommes depuis quelques années dans une période de transition enthousiasmante. Nous vivons en effet une rupture technologique, mais aussi dans certains cas, des changements de paradigme. J’ai fait le choix arbitraire et forcément discutable de discuter la stimulation cardiaque sans sonde et de son évolution vers la synchronisation atrio-ventriculaire ; de la stimulation hissienne qui nous apporte une vision nouvelle et enfin des évolutions dans la stimulation biventriculaire. Les étapes futures consisteront probablement en une fusion/association de ces différentes techniques/approches.
La stimulation cardiaque sans sonde avec synchronisation atrio-ventriculaire
Les premières descriptions de stimulation cardiaque sans sonde datent de 1970(1), mais n’ont pas connu à cette époque-là d’essor du fait de difficultés technologiques.
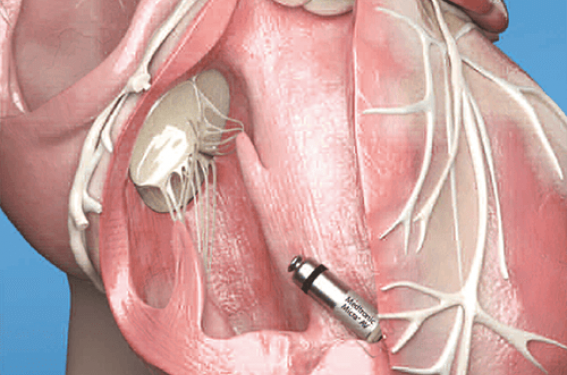
Cependant le concept était né avec de nombreux avantages potentiels, comme l’absence de boîtier sous-cutané, de sonde intravasculaire ou intracardiaque, l’endothélialisation du système… Il a ensuite fallu attendre le début des années 2010 pour voir réapparaître cette technique via différentes techniques. Actuellement, seule l’implantation d’un stimulateur cardiaque sans sonde MICRA (Medtronic©, Minneapolis, MN, USA) est autorisée.
Les premiers stimulateurs cardiaques sans sonde Micra simple chambre ont été implantés en France dans le cadre d’un protocole de recherche à l’IHU de Bordeaux (Dr Ritter, Pr Bordachar) en 2014 puis en pratique courante à partir de 2015 (65 000 dans le monde). L’efficacité et la sécurité de cette technique(2,3) a conduit les autorités à permettre l’utilisation en pratique courante de la stimulation cardiaque sans sonde (Arrêté Journal officiel du 21 février 2019) selon des recommandations précises i) stimulation ventriculaire exclusive (i.e. certains BAV paroxystiques, BAV complet sur FA ou brady FA) ; et ii) chez des patients à haut risque de complications post-implantatoires avec un système traditionnel (i.e. dialyse chronique avec FAV, antécédent de sepsis ou endocardite).
Cependant, cette technique ne s’intéresse qu’à une portion limitée des patients implantés de stimulateurs cardiaques : ceux n’ayant pas besoin d’une synchronisation atrio-ventriculaire permanente.
Il était donc indispensable de pouvoir, via les améliorations technologiques et algorithmiques, permettre une synchronisation atrio-ventriculaire et ainsi élargir les options pour nos patients.
La détection de la systole atriale (onde A en échocardiographie) est basée sur le signal de l’accéléromètre intégré au dispositif. Cette détection atriale dynamique permet d’ajuster le timing de la stimulation ventriculaire afin d’obtenir une bonne synchronisation AV. Des filtres ont été conçus afin d’éviter la surdétection du bruit lié à l’activité mécanique cardiaque intrinsèque, mais aussi au remplissage passif. Lorsqu’une contraction atriale est détectée, un intervalle AV est débuté (mode VDD, 10 ms du fait du délai électro-mécanique) conduisant à une stimulation ventriculaire (figure). En l’absence de détection atriale, une stimulation ventriculaire droite est réalisée avec un intervalle plus long (environ 100 ms) que l’intervalle RR médian(4). Enfin, afin de limiter la stimulation VD, le dispositif vérifie périodiquement l’existence d’une conduction AV (mode VVI 40 + vérification de la conduction) et retour en VDD en cas de stimulation VD à 40 bpm (intérêt en cas de BAV paroxystiques). L’étude MARVEL 2 a démontré une nouvelle fois l’efficacité (95 % des patients avec une synchronisation AV > 70 % du temps en VDD vs 0 % en VVI, p < 0,001) et la sécurité (aucune pause ni aucun épisode de tachycardie induite par la stimulation) de cette technique(5). Les caractéristiques du MICRA AV (1,75 g, 0,8 cc, 18 mm, IRMcompatibilité) et la technique d’implantation sont similaires au MICRA VR avec une longévité estimée entre 8 et 13 ans (vs 12 ans pour le VR).
Figure. Synchronisation atrio-ventriculaire du MICRA AV.
AM : marqueur de l’activité mécanique atriale indiquant que le dispositif a détecté l’activité mécanique de l’oreillette (signal A4). VP : stimulation ventriculaire.
VE : marqueur de fin événements ventriculaires. Fenêtre de détection de A3 (phase passive de la diastole ventriculaire) : le réglage est peu sensible (ligne rouge) de façon à ce que seul un signal de forte amplitude puisse être détecté. Fenêtre de détection de A4 : utilisée pour détecter le signal A4 (systole atriale). Blanking atrial post-ventriculaire (PVAB) : aucune détection atriale n’a lieu pendant cette période.
En France, les premiers Micra AV ont été implantés en mai 2020 (plus d’une cinquantaine de patients).
La stimulation hissienne
La stimulation ventriculaire droite peut avoir des effets délétères sur la fonction ventriculaire gauche et ainsi induire une cardiopathie rythmique. Cette cardiopathie survient d’autant plus s’il existe une dysfonction ventriculaire gauche préalable même modérée. Ainsi, lorsque cela est possible (i.e. dysfonction sinusale ou BAV paroxystique) il est impératif d’utiliser les algorithmes de préservation de la conduction atrio-ventriculaire afin de réduire le pourcentage de stimulation ventriculaire droite.
Lorsque la stimulation ventriculaire est indispensable, l’objectif est donc de se rapprocher au maximum d’une activation ventriculaire physiologique homogène. C’est ainsi que depuis quelques années, la stimulation hissienne suscite un intérêt et un enthousiasme majeurs, plus particulièrement ces derniers mois dans l’alternative à la CRT classique.
L’implantation consiste à l’utilisation d’une sonde dédiée dans une gaine afin d’obtenir un enregistrement du faisceau de His. La stimulation hissienne peut être sélective ou non (fusion de la capture du his et des tissus ventriculaires adjacents). Le recueil ventriculaire est souvent plus faible que dans les autres sites ventriculaires droits avec des seuils plus élevés nécessitant une stimulation avec durée d’impulsion de 1 ms. Une capture d’un bloc de branche est également possible, mais nécessite une énergie supérieure.
Différentes populations ont été étudiées (BAV complet, BBG…) avec des résultats encourageants et positifs, y compris sur des critères durs. Cependant, ces études n’ont concerné majoritairement qu’un nombre limité de patients, et étaient régulièrement rétrospectives, monocentriques ou non randomisées. De nombreuses interrogations subsistent comme l’identification pré-implantation des patients pouvant le plus bénéficier de la stimulation hissienne ; différence entre stimulation sélective ou non ; anomalies de conduction distales…
La stimulation hissienne est une technique très prometteuse, mais des améliorations technologiques ainsi que des études randomisées, multicentriques de plus grande envergure chez les patients en BAV complet ou devant bénéficier d’une CRT vont/doivent être menées.
Resynchronisation cardiaque
La stimulation biventriculaire (CRT) est un outil mature de l’arsenal thérapeutique de l’insuffisance cardiaque à fraction d’éjection altérée avec asynchronisme électrique en association aux traitements médicamenteux. Les évidences sont claires sur son bénéfice concernant l’amélioration des symptômes, de la fonction systolique ventriculaire gauche ; mais aussi la réduction des hospitalisations pour IC et la mortalité. Le bénéfice le plus important de la CRT a été démontré chez les patients présentant un asynchronisme électrique important (i.e. BBG > 150 ms, zone latéro-basale d’activation retardée). Dans d’autres populations, comme les patients en fibrillation atriale, avec un bloc indifférencié, une cardiopathie ischémique le bénéfice peut être plus faible. C’est ainsi que l’on se souvient qu’environ 30 % des patients sont considérés comme « nonrépondeurs » à la CRT. Il est donc indispensable de mieux identifier ces patients, les raisons de la non-réponse et de trouver d’autres stratégies thérapeutiques pour améliorer cette dernière.
Les sondes quadripolaires implantées actuellement permettent la stimulation VG multipoint (MPP). Après de nombreuses études de faibles envergures, monocentriques montrant un bénéfice, le soufflé est retombé après les résultats de l’étude MORE-CRT MPP(6). Aucun bénéfice n’a été mis en évidence pour l’activation du MPP chez les non-répondeurs. Un sous-groupe avec un écart anatomique inter-électrode de plus de 30 mm et un délai court de stimulation de 5 ms semble avoir un bénéfice. Une étude est en cours en ce sens(7).
Une autre option pourrait être la stimulation multi-zone et endocardique via différents moyens technologiques. Différents systèmes sont en cours d’évaluation dont la mise en place de puces endocardiques à différents niveaux (VG principalement) avec un système de générateur sans fil implanté à proximité (UCLA and TIH, WISE-CRT). Ceci permettrait de rendre une stimulation VG plus homogène. Enfin, la stimulation hissienne (cf. supra) et la stimulation de la branche gauche semblent être des solutions encourageantes, mais qui nécessitent encore des investigations robustes.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :