Publié le 01 oct 2017Lecture 5 min
Stimulation épicardique ou endocardique chez l’enfant : la question reste débattue
Sonia SALMI-BELMIHOUB, Philippe CHEVALIER, service de rythmologie, Hôpital cardiologique Louis Pradel, Lyon
Grâce au développement des techniques chirurgicales, le nombre d'enfants porteurs de cardiopathie congénitale complexe opérés avec succès a progressé avec par conséquent un accroissement du nombre d'implantations de stimulateurs cardiaques. Dans le choix de la technique d'implantation, de nombreux éléments sont à prendre en compte tels que la taille et le poids, l’existence d’anomalies intracardiaques et la croissance.
Nous rapportons les cas de deux enfants porteurs de stimulateur cardiaque don’t l’évolution a été compliquée de dysfonction de sonde.
Cas clinique n°1
C.C., née le 3 avril 2010 se présente à sa consultation systématique de contrôle de pacemaker (PM) : il s’agit d’une petite fille aux antécédents de transposition des gros vaisseaux et de CIV, de diagnostic anténatal, opérée en période néonatale d’un switch artériel avec fermeture de CIV.
Les suites opératoires ont été compliquées de bloc atrio-ventriculaire complet (BAVC) ayant nécessité l’implantation d’un stimulateur cardiaque double chambre épicardique.
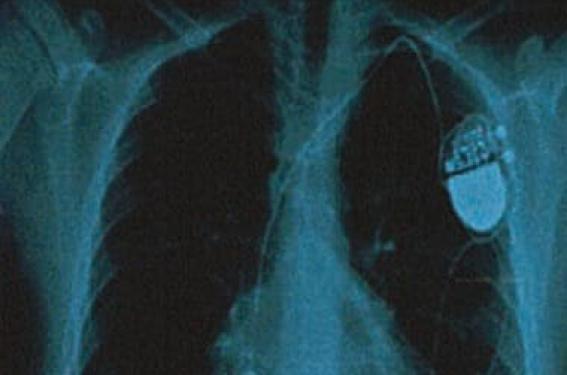
L’interrogation du stimulateur cardiaque lors de cette consultation, 3 ans après implantation met en évidence de nombreuses surdétections (figure 1) sur le canal ventriculaire. La mère de C.C. ne rapporte pas de malaise ou de perte de connaissance, la radiographie de thorax ne montre pas de rupture de sonde (figure 2) dont l’impédance a diminué passant de 380 à 140 ohms. C.C. est stimulodépendante, nous réglons le stimulateur en mode asynchrone VOO et elle est opérée rapidement. En per-opératoire, une effraction de la gaine plastique de l’électrode est mise en évidence (figure 3), celle-ci est extraite et une nouvelle sonde est mise en place ; la sonde atriale fonctionne correctement, les deux sondes sont raccordées à un nouveau boîtier intra-abdominal.
Figure 1. Nombreuses surdétections sur le canal ventriculaire.
Figure 2. Absence de rupture de sonde.
Figure 3. Effraction de la gaine plastique.
Cas clinique n°2
• B.A., né le 17 mai 2001, aux antécédents de BAV complet après chirurgie de fermeture de CIV se présente en 2014 à la consultation systématique de contrôle de son stimulateur cardiaque simple chambre relié à une sonde endocavitaire implantée en 2002 avec un changement de boîtier en 2009. Une première sonde épicardique mise en place à un mois de vie s’est compliquée de rupture.
L’interrogation du boîtier met en évidence une élévation brutale de l’impédance de la sonde à 3 000 ohms, du seuil de stimulation ventriculaire et une perte de la détection ventriculaire.
B.A. est asymptomatique, il n’est pas stimulodépendant. Nous réglons l’appareil en mode VVI 40 avec une sortie à 5 volts, la radiographie thoracique est normale (figure 4).
Après discussion collégiale, nous décidons de réimplanter B.A. en épicardique avec un boîtier intra-abdominal afin de préserver le capital veineux.
Figure 4. Radiographie normale.
Discussion
L’implantation de stimulateurs cardiaques en pédiatrie représente moins de 1 % de l’ensemble des pacemakers implantés(1).
La stimulation cardiaque chez l’enfant nécessite un suivi à long terme et diffère de chez l’adulte, elle doit tenir compte de la croissance, de la taille, du poids de l’enfant et du capital vasculaire. La longévité du stimulateur cardiaque peut être évaluée par des mesures telles que tension et impédance de pile, mais la longévité d’une sonde épicardique ou endocardique ne peut être prédite. Elle dépend de la croissance et de l’activité physique souvent intense.
Généralement, les sondes épicardiques sont utilisées chez l’enfant de petite taille et de petit poids (< 20 kg), la technique est invasive nécessitant une thoracotomie, sternotomie ou une approche sous-xyphoïdienne.
Chez l’enfant plus grand, il est souvent préféré la voie endoveineuse moins invasive permettant souvent un seuil de stimulation ventriculaire chronique inférieur à celui d’une sonde épicardique. De grands progrès ont été réalisés avec l’avènement des sondes épicardiques à élution de stéroïdes, permettant un seuil chronique stable rivalisant avec les sondes endocardiques.
Les systèmes endoveineux ont été moins utilisés chez l’enfant en bas âge et le nourrisson en raison de complications telles que les occlusions veineuses survenant dans environ 13,7 % des cas(1). S’agissant d’enfants nécessitant une stimulation cardiaque durant toute la durée de leur vie, l’extraction de sonde et le changement de sonde pourront représenter de grandes difficultés, c’est pourquoi le capital veineux doit être préservé au maximum.
Le risque de rupture et de dysfonction de sonde paraît supérieur avec le système épicardique (dans une étude rétrospective le taux atteint 10,3 % pour les sondes épicardiques et 4,3 % pour les sondes endocardiques)(2). Toutefois, les sondes endoveineuses peuvent également être concernées par les dysfonctions, comme nous l’avons vu dans le cas de B.A.
La longueur de la sonde peut ne pas être adaptée à la croissance de l’enfant malgré une boucle réalisée dans l’oreillette droite de la sonde ventriculaire (adhérence à la veine cave inférieure). La sonde endoveineuse peut se compliquer d’accident thromboembolique chez l’enfant porteur d’un shunt intra-cardiaque, dans ce cas la sonde épicardique doit être préférée.
Une insuffisance tricuspide peut également être aggravée par les sondes ventriculaires droites.
Quant aux complications infectieuses, elles ne sont pas rares, estimées entre 2 et 7 % selon les publications(2). Ce risque semble accru en cas de trisomie 21 et de réintervention, mais il n’y a pas de différence dans la fréquence des infections entre sonde épicardique et sonde endocardique.
En dépit du nombre croissant d’implantations de pacemakers endoveineux, un grand nombre d’auteurs préfèrent la stimulation épicardique chez les nourrissons et les enfants de moins de 15 kg. Certaines équipes retiennent même l’indication d’un stimulateur cardiaque épicardique chez tous les patients de moins de 30 kg et de moins de 16 ans(3).
Le nombre de sondes est aussi une question qui se pose chez l’enfant.
En cas de stimulation endoveineuse, la limite d’une stimulation double chambre est l’accès vasculaire et le petit diamètre des vaisseaux.
En cas de stimulation épicardique, l’implantation d’une sonde atriale par une approche sous-xyphoïdienne n’est pas possible et nécessite une thoracotomie gauche ou une sternotomie. Le choix du pacemaker doit tenir compte de la fréquence maximale de suivi autorisée par l’appareil, sachant que la fréquence sinusale de l’enfant peut aller jusqu’à 180, voire 200 bpm, pouvant excéder la fréquence cardiaque maximale de suivi et être à l’origine d’un bloc atrioventriculaire 2/1 symptomatique, c’est pourquoi chez les enfants de petite taille et une fréquence ventriculaire rapide, une stimulation simple chambre à fréquence asservie VVIR sera préférée.
En pratique
La stimulation cardiaque pédiatrique est un défi perpétuel.
La majorité des enfants porteurs d'un pacemaker nécessiteront une stimulation cardiaque durant toute leur durée de vie.
La supériorité d'une voie endoveineuse ou épicardique n'a pas été établie, mais la stimulation épicardique apparaît sûre et fiable, notamment chez les très jeunes enfants permettant la préservation d'un capital veineux.
Un suivi rapproché est essentiel afin de dépister toute dysfonction de sonde, anticiper les signes d'usure, optimiser les réglages et assurer la marge de sécurité suffisante concernant le seuil de stimulation.
Le pacemaker sans sonde pourrait devenir une alternative chez les enfants, mais de nouvelles études sont nécessaires.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :