Cardiologie interventionnelle
Publié le 01 juin 2017Lecture 10 min
GRCI : où en sont les promesses techniques ?
Pierre AUBRY, Hôpital Bichat Claude-Bernard, Paris
Le Groupe de réflexion sur la cardiologie interventionnelle (GRCI) est constitué de professionnels de santé intéressés par le partage d’expériences et la transmission d’informations sur la cardiologie interventionnelle. La cardiologie interventionnelle est une discipline dynamique avec un nombre grandissant de pathologies traitées, des innovations développées par les industries du médicament et des dispositifs implantables ainsi que des recommandations professionnelles régulièrement renouvelées. Le congrès a été l’occasion de discuter de technologies initialement prometteuses mais qui ont du mal à s’inscrire dans la pratique courante.
Stents biorésorbables : il est prudent d’attendre
D’après V. LEGRAND, Liège (Belgique)
Les stents médicamenteux métalliques permettent des angioplasties coronaires avec d’excellents résultats à court et moyen terme. Le risque de thrombose ou de resténose avec les prothèses de dernière génération est inférieur à 3 ou 10 % après 5 ans selon les indications. Néanmoins, des événements tardifs, tels que thromboses, athéromes intrastent (néo-athérosclérose), resténoses secondaires à une fracture de prothèse sont décrits. De plus, l’implantation d’une structure métallique empêche la restitution d’une fonction endothéliale normale et représente une contrainte pour une éventuelle intervention de pontage aortocoronarien. C’est pour ces multiples raisons, que le rempla cement du stent métallique par une structure de soutien intravasculaire résorbable et temporaire a été imaginé. Cette idée était d’autant plus pertinente que les stents enrobés de première génération (Cypher©, Cordis et Taxus™, Boston Scientific) présentaient un risque élevé de thromboses tardives pouvant requérir une double thérapie antiplaquettaire à très long terme.
Les stents biorésorbables, ou BVS (biovascular scaffold)/BRS (bioresorbable scaffold) selon les auteurs, offrent donc l’avantage théorique de restaurer à terme une lumière vasculaire « physiologique », libérée d’une structure métallique.
La disparition du soutien métallique pourrait atténuer le risque thrombotique à moyen et long terme et rétablir une fonction endothéliale normale.
Cet avantage est particulièrement pertinent chez les sujets jeunes ou pour traiter de longues sténoses, notamment sur l’artère IVA.
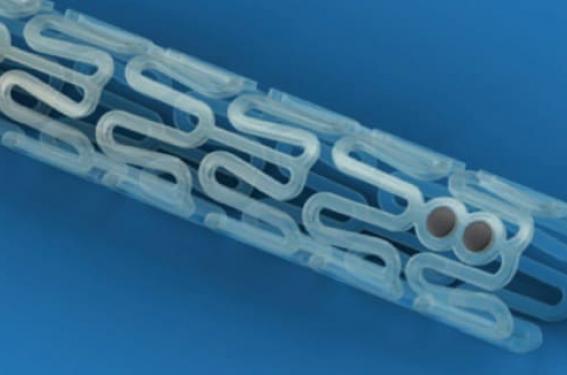
Quatre stents biorésorbables ont reçu une autorisation commerciale : Absorb (Abbott Vascular), DESolve® et DESolve® Cx (Elixir) et récemment Magmaris (Biotronik). La structure biorésorbable des stents Absorb (figure 1) et DESolve® est constituée de polymères hydrolysables de PLLA, celle du stent Magmaris est en oxyde de magnésium. Ces stents sont imprégnés d’une substance antiproliférative, respectivement l’évérolimus pour Absorb, le novolimus pour DESolve® et le sirolimus pour Magmaris. Ces polymères sont conçus pour assurer un support vasculaire ferme durant 6 à 12 mois. Ensuite, le stent perd sa rigidité et disparaît par hydrolyse en 3 à 4 ans. Le médicament antiprolifératif se libère au cours des 3 premiers mois. Les propriétés physico-chimiques de ces structures résorbables constituent le point de faiblesse majeur par rapport à celles des alliages métalliques des drug eluting stents (DES) actuels.
Afin d’assurer un soutien vasculaire suffisant durant plusieurs mois, les mailles de ces prothèses doivent être épaisses et la densité du maillage accru. Il en résulte que ces stents recouvrent une surface vasculaire plus étendue (30 % vs 13 % pour un DES) et que les mailles sont plus épaisses (160 μm vs 50/90 μm pour les DES). Le stent Absorb a été implanté la première fois en 2006, il est commercialisé depuis plus de 5 ans et la plupart des données présentées dans cet article concernent cette endoprothèse. Les données cliniques concernant le DESolve® et le Magmaris sont limitées à ce jour. Que nous ont appris les études et registres publiés ?
Figure 1. Stent BVS Absorb (Abbott).
Placer correctement un BVS est plus difficile et plus onéreux
Les mailles épaisses et larges constituent un handicap pour glisser le BVS dans un vaisseau calcifié, rigide ou tortueux. Par ailleurs, le risque d’occlusion de branches vasculaires latérales est accru et le résultat angiographique final (MLD) est toujours inférieur avec un BVS en raison de l’épaisseur de ses mailles, ceci ayant une importance significative pour les petits vaisseaux (< 2,5 mm). De plus, les stents BVS ne sont pas (ou très peu) compliants, ce qui impose un choix précis du diamètre de la prothèse. Le risque de malapposition avec ces stents non compliants est augmenté et celui d’une fracture de mailles élevé en cas de postdilatation avec un ballon plus large. De même, ces stents ne sont pas recommandés si le diamètre de la partie proximale de la sténose excède celui de la partie distale (en cas de bifurcation, par exemple). Enfin, ces stents ne sont pas visibles aux rayons X et le contrôle de leur ouverture impose le recours à l’imagerie endocoronaire (OCT ou IVUS). En conséquence, il est indispensable de bien dilater le vaisseau avec un ballon non compliant et d’effectuer ensuite un contrôle du résultat par OCT ou IVUS avant de choisir le diamètre et la longueur du BVS. Une postdilatation est toujours nécessaire avec un ballon non compliant et un contrôle final avec OCT/IVUS est recommandé.
La lésion idéale pour ce type de stent est une sténose courte de type A ou B1 dans un vaisseau de 3,0 à 3,5 mm pouvant être couverte par un stent de 18 mm, en évitant une bifurcation. L’approche de sténoses plus complexes peut être envisagée avec l’expérience.
Des résultats cliniques avec les BVS de 1re génération décevants, voire inquiétants : thromboses précoce et tardive plus fréquentes
Le risque de thrombose précoce est deux fois plus important après BVS.
Cela s’explique par un risque de malapposition plus important et par les dimensions plus larges des BVS. Les résultats récents du suivi après 3 ans de l’étude ABSORB II révèlent un risque persistant de thrombose au-delà de la première année, ce risque atteignant 2,8 % à 3 ans. Les images, notamment endocoronaires par OCT, obtenues chez les patients avec thrombose de stent révèlent que la malapposition, la désintégration inégale et la fragmentation des stents expliquent, en partie, les événements précoces et tardifs. Le risque de thrombose est majoré en cas de vaisseaux de petit calibre, de résultat sub-optimal ou de sténose ostiale.
Une fréquence d’infarctus péri- ou postprocéduraux accrue
La thrombose du stent occasionne fréquemment un infarctus avec sus-décalage ST. D’autres infarctus plus limités surviennent durant la procédure (occlusion de branche latérale) ou plus tard (embolisation de fragment du stent). Après 1 an, ce risque est majoré de 50 % par rapport aux DES.
Une prolifération néo-intimale plus marquée
Comparativement aux DES, le BVS Absorb, assure le même taux de succès pour prévenir une resténose justifiant une nouvelle revascularisation. Cependant, le résultat angiographique à 1 an est meilleur après DES (minimal lumen diameter plus large de 0,08 mm). Une fois encore, ces différences en faveur du DES s’observent essentiellement pour les artères dont le calibre est < 2,5 mm.
La vasomotricité endothéliale n’est pas améliorée
Contrairement à l’hypothèse avancée lors du lancement des BVS, ceux-ci ne montrent pas de bénéfice évident pour la fonction endothéliale. Dans la récente étude ABSORB II, l’administration de nitroglycérine intracoronaire ne favorise pas une dilatation vasculaire plus marquée au niveau du site traité par un BVS « résorbé », 3 ans après son implantation réussie.
En conclusion, les stents BVS de première génération n’ont pas répondu aux espoirs qu’ils avaient soulevés lors de leur commercialisation il y a 5 ans (figure 2). Bien qu’il ne faille pas jeter le bébé avec l’eau du bain, force est de constater que les stents résorbables n’ont pas encore atteint le degré d’efficacité et de sécurité des DES de dernière génération.
Les leçons reçues des études randomisées, des nombreux registres et d’observations accumulées au cours des deux dernières années nous invitent à la prudence et il convient de réserver ces stents à des vaisseaux proximaux de gros calibre (≥ 3,5 mm), aisément accessibles, chez des sujets jeunes. L’avenir nous apprendra si les BVS de deuxième génération, actuellement en étude clinique de phase 2 ou 3, se montrent plus efficaces et plus sûrs.
Figure 2. Guérison vasculaire et évolution anatomique après DES et BVS.
Voies mini-invasives et robotique en chirurgie coronaire
D’après J.-F. FUZELLIER, Saint-Étienne
La chirurgie coronaire miniinvasive peut se définir comme toute chirurgie de revascularisation myocardique évitant la sternotomie. Plusieurs procédures peuvent rentrer dans cette définition.
La première approche consiste en pontages par minithoracotomie antérolatérale : MIDCAB (minimally invasive direct coronary artery bypass). La seconde approche est la chirurgie de pontages réalisée de façon totalement endoscopique à l’aide du robot TECAB (totally endoscopic coronary artery bypass). Enfin, la troisième approche est un mélange des deux techniques précédentes : MIDCAB-robot assisté.
Ces trois techniques peuvent être réalisées avec ou sans circulation extracorporelle (CEC), sans clampage aortique ou à cœur arrêté. Dans ce type de procédure, le chirurgien est confronté à différents défis : prélèvement des greffons mammaires, anastomoses coronariennes de bonne qualité et réalisation de pontages multiples.
MIDCAB
Le principe est d’effectuer l’intervention par minithoracotomie, le plus souvent gauche, et de réaliser le prélèvement mammaire et l’anastomose sous vision directe. Le prélèvement peut être plus difficile à réaliser que par sternotomie, selon la morphologie du patient, et il peut y avoir des difficultés de libération jusqu’à l’artère sous-clavière avec une longueur de greffon parfois plus courte. L’abord coronaire peut être réalisé par des techniques de luxation du cœur.
Les anastomoses distales sont réalisées le plus souvent à cœur battant à l’aide de stabilisateurs adaptés à la chirurgie mini-invasive. Dans ce type de procédure, le prélèvement mammaire bilatéral est impossible par un abord unique et les anastomoses proximales aortiques sont difficiles. Lors de la réalisation de pontages multiples, il faut privilégier les greffons séquentiels et les montages en Y au niveau de l’artère mammaire gauche avec souvent le greffon radial. Il existe certaines contre-indications à ce type de chirurgie : présence d’adhérences pleurales et antécédents de thoracotomie gauche, déformations sternales type pectus excavatum et artères coronaires calcifiées ou intramyocardiques.
La série la plus importante a été publiée par McGinn et coll.(1) à propos de 450 patients. Des pontages multiples ont été réalisés dans 80 % des cas. Les pontages étaient réalisés sans CEC à cœur battant dans 83 % des cas.
Dans cette étude, les résultats étaient satisfaisants en termes de mortalité (1,3 %) et de morbidité avec une conversion par sternotomie de 3,8 %, une reprise pour saignement de 2,2 % et un taux d’infection de 0,2 % uniquement superficielle.
La même équipe a comparé le MIDCAB versus la chirurgie par sternotomie(2) avec un taux d’infection moindre pour le MIDCAB (0 vs 4 %) et une réhabilitation plus rapide pour la chirurgie mini-invasive (12 jours vs plus de 5 semaines). La perméabilité des greffons a été étudiée à 6 mois chez 151 patients(3) avec un taux de perméabilité de 92 % (100 % pour les greffons mammaires gauches et 85 % pour les greffons saphènes). L’excellente perméabilité des greffons mammaires a été corroborée par une métaanalyse(4) comparant la revascularisation de l’artère IVA par MIDCAB ou angioplastie : à 6 mois, les résultats étaient favorables à la chirurgie mini-invasive avec un taux inférieur de nouvelle revascularisation et d’événements cardiovasculaires.
Chirurgie robotique
Le robot est représenté actuellement uniquement par le système da Vinci (figure 3) qui facilite la chirurgie coronaire mini-invasive en permettant d’effectuer une chirurgie totalement endoscopique. Il permet un prélèvement bilatéral par la même voie avec son système de vision 3D ainsi que des anastomoses de qualité permettant de revasculariser tous les territoires grâce à son instrumentation totalement articulée et à un système de stabilisation adapté.
Différentes stratégies peuvent être réalisées grâce au robot : une chirurgie coronaire totalement endoscopique (TECAB), soit à cœur battant sans CEC (BHTECAB), soit avec une CEC et un clampage endovasculaire (AHTECAB) ou une chirurgie combinée au MIDCAB avec un prélèvement mammaire réalisé avec le robot et une anastomose réalisée sous vision directe (MIDCAB robot assisté). Le robot possède certaines limites : longueur de la procédure, courbe d’apprentissage, coût plus important et disponibilité. Dans une revue de la littérature, Cao et coll.(5) a montré que le temps d’intervention variait selon l’équipe et l’expérience : temps de prélèvement mammaire de 26 à 60 minutes, temps d’anastomose de 28 à 60 minutes et temps d’intervention de 166 à 444 minutes.
La plus grande expérience de TECAB a été publiée à partir de 500 patients(5). Un tiers des patients avait bénéficié de pontages multiples jusqu’à 4 pontages et la procédure était réalisée le plus souvent sous CEC et clampage aortique (78 %). La mortalité opératoire était basse (1 %) avec un taux de conversion en MIDCAB ou sternotomie de 10 % et une absence de complications majeures chez 95 % des patients. Les facteurs prédictifs d’absence de conversion et de complications majeures étaient la réalisation d’un monopontage, l’utilisation d’une CEC avec clampage aortique et les patients opérés audelà de la courbe d’apprentissage du chirurgien considérée à plus de 20 patients. Le même groupe a comparé 334 patients avec monopontage à 150 patients avec double pontage(6). Les résultats étaient favorables au groupe monopontage en termes de durée d’intervention (240 min vs 375 min), de conversion (9,3 % vs 20,7 %) et de mortalité opératoire (0,3 % vs 2 %) avec cependant une réhabilitation identique.
Dans une étude rétrospective(7) reprenant la base de données nord-américaine 2008-2010, Cavallaro a comparé la chirurgie coronarienne robotique à la chirurgie par sternotomie. L’activité robotique représentait 0,4 % de l’activité de chirurgie coronarienne.
Figure 3. Robot da Vinci.
Un bénéfice en faveur de la chirurgie robotique était retrouvé avec une réduction de morbidité et une diminution des transfusions chez les patients bénéficiant d’un monopontage. Par contre, il existait une mortalité et une morbidité plus importante mais non significative de la chirurgie robotique en cas de pontages multiples.
La chirurgie coronaire mini-invasive ou robotique est faisable et reproductible même pour la réalisation de pontages multiples. La perméabilité à court et long terme est excellente, en particulier pour les greffons mammaires, et superposable à la chirurgie conventionnelle.
Un bénéfice est démontré avec une réduction des complications postopératoires chez les patients bénéficiant de monopontages. En cas de pontages multiples, les bénéfices postopératoires n’ont pas été démontrés. Par contre dans tous les cas, il existe une réhabilitation des patients plus rapide. La stratégie hybride avec chirurgie de monopontage de l’artère IVA et angioplastie complémentaire a vraisemblablement un intérêt chez les patients pluritronculaires dans les équipes entraînées.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :