Cardiologie générale
Publié le 14 avr 2014Lecture 4 min
Conduite à tenir devant la découverte d’un épanchement péricardique asymptomatique
P. MEURIN, J.-Y. TABET, Les Grands Prés, Centre de réadaptation cardiaque de la Brie, Villeneuve-Saint-Denis
Il n’est pas exceptionnel de découvrir un épanchement péricardique asymptomatique (Epe) lors d’une échographie cardiaque transthoracique : cette éventualité concerne environ 5 % des examens réalisés dans un laboratoire d’échographie d’un hôpital général par exemple, mais, l’incidence de ces Epe est fortement dépendante des modalités de pratique de chacun d’entre nous. Il est évident, par exemple, que l’échographiste d’un service de médecine interne spécialisé dans les maladies auto-immunes sera plus souvent confronté à cette éventualité. Face à cette situation, le praticien doit répondre à plusieurs questions simples. Est-ce vraiment un épanchement péricardique ?
Le diagnostic échographique est habituellement facile. Un épanchement banal non cloisonné prédomine en zone déclive et sera d’abord visualisé en arrière de la paroi postérieure du VG en incidence parasternale et en regard du VD en incidence sous-costale. L’extension se fait ensuite autour de la paroi latérale des ventricules puis vers les oreillettes. L’Epe est alors circonférentiel.
En conséquence, un épanchement localisé en antérieur, en regard du VD en incidence parasternale gauche, est inhabituel s’il n’y a pas de lésion péricardique locale préalable (épanchement péricardique postopératoire ou infectieux) et doit plutôt être considéré comme la présence de franges graisseuses épicardiques jusqu’à preuve du contraire.
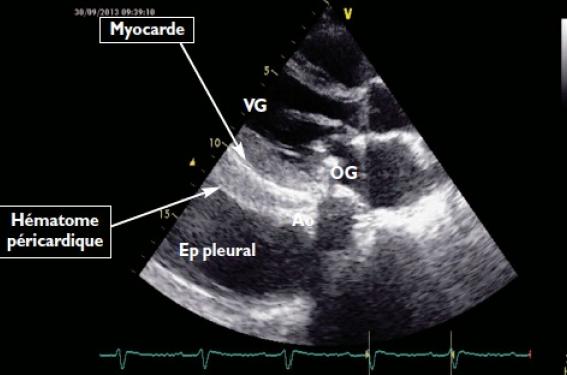
Un éventuel épanchement pleural gauche est localisé derrière l’aorte thoracique descendante en incidence parasternale gauche (alors que l’épanchement péricardique sera en avant).
Les autres diagnostics différentiels (sinus coronaire dilaté, hématome paracardiaque par exemple rétrosternal postopératoire, tumeur péricardiaque, etc.) sont plus rares et peuvent rendre nécessaire la réalisation d’un scanner ou d’une IRM pour confirmation.
Y a-t-il un risque de tamponnade ?
Rappelons que le cadre fixé par cet article est celui de la découverte d’un Epe asymptomatique. Il faut néanmoins savoir chercher des symptômes frustres tels que nausées, hoquet, anorexie, grande asthénie, lipothymie, dyspnée modérée, petits œdèmes des membres inférieurs, turgescence jugulaire, pouls paradoxal, etc. Le moindre signe clinique doit entraîner un drainage en urgence.
L’évolution vers une tamponnade dépend de 2 facteurs : le volume de l’épanchement péricardique, bien entendu, mais aussi la rapidité de l’évolution ; un volumineux épanchement de plus d’un litre peut être parfaitement asymptomatique s’il s’est développé lentement alors qu’un petit épanchement soudain (hémopéricarde post-traumatique) de 100 à 200 ml peut être très mal toléré.
Les signes échographiques de tamponnade sont indiqués au tableau 1. Il faut insister sur le fait qu’aucun signe échographique n’est pathognomonique et que la clinique prime. Retenons cependant qu’une tamponnade sans perte du collapsus inspiratoire de la veine cave inférieure est rare (sensibilité 97 %). Finalement, pour un épanchement de volume moyen à important (plus de 10 mm en diastole), le risque de tamponnade est estimé à au moins 25 %, ce qui justifie une surveillance très régulière.
Y a-t-il un risque d'évolution vers une péricardite contrictive ?
Le risque d’évolution vers une péricardite chronique constrictive est très faible ; il est en particulier lié à l’étiologie : on l’estime à 0,5 % après une péricardite idiopathique ou virale, à 2,5 à 3 % après un épanchement péricardique postopératoire ou après une péricardite sur maladie auto-immune, à 5 % pour un épanchement péricardique néoplasique et respectivement à 20 et 30 % pour les épanchements péricardiques tuberculeux et purulents.
Comment déterminer la cause de cet épanchement ?
C’est le problème le plus difficile. La recherche étiologique dépend de l’épidémiologie locale et surtout de la prévalence de la tuberculose (première cause mondiale d’Epe).
Dans deux tiers des cas, lors de la découverte d’un Epe, le diagnostic étiologique est déjà connu : il s’agissait d’une échographie systématique de surveillance d’une maladie ou d’un traitement qui a permis le dépistage de l’épanchement péricardique qui est, rappelons-le, asymptomatique. Aucun bilan étiologique supplémentaire n’est alors nécessaire.
Dans le tiers des cas restants, le bilan étiologique doit être rigoureux.
Cinq grands types de pathologie peuvent être à l’origine de ces épanchements dans les pays développés : cancer, traumatisme (chirurgie, geste invasif), infection, connectivite, épanchement d’origine hémodynamique (insuffisance cardiaque, hypoprotidémie, etc.) (tableau 2). Il n’est pas possible de proposer un arbre décisionnel adaptable à tous les patients, car les examens réalisés sont orientés par le terrain et la clinique. Schématiquement, un bilan large et éventuellement répété sera à réaliser (tableau 3b).
Malgré cela, assez souvent (50 % des épanchements sans étiologie évidente au départ), la cause ne sera pas retrouvée et le diagnostic porté sera celui d’« épanchement péricardique chronique idiopathique ». Ce diagnostic pourra être reconsidéré à moyen terme en fonction de l’évolution.
Comment traiter ?
Le traitement est celui de la maladie causale. Un épanchement péricardique asymptomatique n’est pas une péricardite. Cependant, rarement, s’il existe un syndrome inflammatoire et une suspicion de péricardite idiopathique ou virale frustre récente, on pourra tenter un traitement d’épreuve par aspirine (ou anti-inflammatoire non stéroïdien) et colchicine (tableau 3a). Dans tous les autres cas, ce traitement anti-inflammatoire est inutile.
Hématome péricardique postopératoire (plastie mitrale) : ce patient est porteur d’un épanchement inhabituel : solide, dense, hyperéchogène, que l’on distingue facilement du myocarde ventriculaire gauche : il s’agit d’un hématome. Cet épanchement est en avant de l’aorte thoracique descendante (Ao), contrairement à l’épanchement pleural associé.
En pratique
Dans la plupart des cas, les épanchements péricardiques (Epe) asymptomatiques ne sont pas des péricardites. Un traitement par anti-inflammatoire et colchicine est alors inutile (le traitement est étiologique).
Dans 60 % des cas, la cause de l’Epe est déjà connue lors de sa découverte. Dans les 40 % des cas restants, l’origine restera souvent inconnue (la moitié des cas environ), mais il faut activement chercher cancers, maladies auto-immunes, infections, etc., car le pronostic est celui de la maladie causale.
Le risque de tamponnade à moyen terme est estimé à plus de 25 % pour les Epe moyens à abondants (> 10 mm, mesuré en diastole), ce qui justifie une surveillance régulière (au moins après 1 à 2 semaines, 1 mois et 6 mois).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :