Publié le 21 avr 2009Lecture 6 min
Quand et pourquoi mesurer l'index de pression systolique ?
Y. KAGAN, Fondation de Rothschild, Paris
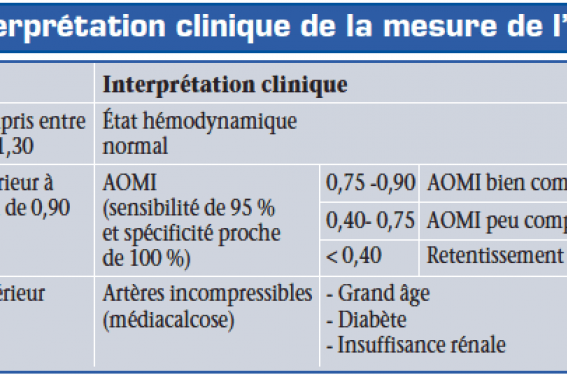
La mesure de l’index de pression systolique (IPS) avec un Doppler de poche a un double intérêt : détecter une artériopathie oblitérante des membres inférieurs (AOMI) le plus précocement possible et indiquer un risque accru de morbi-mortalité cardiovasculaire. Un IPS < 0,9 signe une AOMI asymptomatique et indique un risque d’accident cardiovasculaire inversement corrélé à sa valeur.
Mis au point il y a plus de 40 ans(1), l’IPS suscite un regain d’intérêt depuis quelques années. L’IPS est le rapport de la pression systolique à la cheville sur la pression systolique humérale, mesurées à l’aide d’une sonde de poche Doppler (Doppler portable).
Un IPS inférieur à un seuil de 0,90 signe l’existence d’une AOMI avec une sensibilité de 95 % et une spécificité proche de 100 %.
Détecter précocement une AOMI
L’intérêt de la mesure de l’IPS est de détecter une AOMI le plus précocement possible à un stade asymptomatique, soit parce que le symptôme « claudication d’effort » ne s’est pas encore extériorisé chez un patient mobile, soit parce que le patient, peu mobile, a un périmètre de marche insuffisant pour qu’il se déclenche. La douleur peut aussi ne pas s’exprimer en cas de neuropathie associée (diabétique ou non). Les formes asymptomatiques d’AOMI voient donc leur fréquence augmenter avec l’âge.
Pourquoi ?
Pour mesurer un risque
Risque local
Le niveau de l’IPS est corrélé à la sévérité de l’artériopathie. Plus il est bas, plus le retentissement de l’AOMI est grave.
Détecter une AOMI a donc un intérêt local. Ainsi, un patient âgé qui à la suite d’une pathologie aigue se trouve alité ou immobilisé est un sujet dont le risque d’escarre est accru. À noter qu’un IPS trop élevé a aussi une valeur péjorative.
Risque surtout général
Détecter une AOMI a surtout un intérêt général. Une AOMI témoigne d’une artériosclérose et signe un risque accru de morbi-mortalité cardio- et cérébrovasculaire.
Cela a été démontré chez les sujets claudicants qui, à 5 ans, ont un risque d’environ 30 % de faire un accident coronarien ou vasculaire cérébral (1 fois sur 3 létal)(2).
Une étude récente sur un suivi de 12 ans de 1 600 sujets de 55 à 75 ans a permis de démontrer(3) que plus l’IPS est abaissé, plus la morbi-mortalité cardiovasculaire est élevée. On ajoutera qu’un IPS franchement augmenté > 1,30 constitue alors un marqueur indépendant de risque cardiovasculaire et a la même valeur péjorative qu’un IPS < 0,9.
Pour réduire le risque de morbi-mortalité vasculaire
La mise en évidence d’une AOMI indique une morbidité cardio et cérébrovasculaire accrue qui peut être réduite par une triade médicamenteuse associant : statines-antiagrégants plaquettaires-inhibiteurs de l’enzyme de conversion (IEC). Dans la pratique, deux situations peuvent s’individualiser.
Il n’existe pas d’autre localisation athéromateuse connue
Soit le patient n’avait aucun traitement à visée cardiovasculaire et la trithérapie sus mentionnée peut lui être logiquement proposée.
Soit - et c’est plus souvent le cas - il est déjà traité pour une HTA ou une hypercholestérolémie. Il sera alors légitime de lui adjoindre un antiagrégant plaquettaire et une statine s’il n’en avait pas. Quant au traitement antihypertenseur, au cas où l’HTA était insuffisamment équilibrée, l’adjonction d’un IEC au traitement antérieur est logique en surveillant la créatininémie lors de la mise en route.
Le patient a déjà une autre localisation athéromateuse connue
Si tel est le cas, rappelons que l’existence de la seconde localisation athéromateuse qu’est l’AOMI double le risque de morbi-mortalité cardiovasculaire. Cela a été démontré par le registre REACH.
Registre REACH
Il s’agit d’une vaste étude observationnelle mondiale de 55 000 patients de plus de 45 ans souffrant d’une maladie athérothrombotique, incluant une cohorte Française de 3 514 patients. Sur 1 an de suivi, les patients ayant une atteinte polyvasculaire ont eu un taux d’événements cardiovasculaires majeurs à 1 an passant de 11,7 % pour une atteinte athérothrombotique unique à 22,3 % pour deux localisations ou plus.
L’ordonnance d’un patient ayant déjà eu un accident coronarien ou cérébrovasculaire comporte en règle déjà la triade : antiagrégant-statine-IEC.
La mise en évidence d’une AOMI doit être un argument de plus en faveur d’une observance sans faille. Mais elle ne modifie pas fondamentalement l’ordonnance, à une réserve près : le fait que le praticien devrait être amené à remplacer l’aspirine par du clopidogrel, à la lumière de l’étude CAPRIE (4).
Étude CAPRIE
L’étude CAPRIE est une étude internationale multicentrique randomisée en double aveugle. Sur une durée de presque 2 ans, elle a montré que le clopidogrel (75 mg) diminuait de 8,7 % par rapport à l’aspirine (325 mg) le risque global d’événement vasculaire chez près de 20 000 patients athérothrombotiques ayant eu un accident ischémique cérébral, un infarctus du myocarde (IDM) ou une artériopathie des membres inférieurs, et dont 26 % étaients polyartériels.
S’il s’agit d’un coronarien sous bêtabloquants, la mise en évidence d’une AOMI n’est (contrairement au syndrome de Raynaud) pas une contre indication à cette classe médicamenteuse.
En pratique : deux cas de figure
Soit un écho-Doppler artériel est nécessaire
Dans 3 types de situations
En cas d’ischémie critique révélée par une douleur de décubitus ou un ulcère artériel, l’écho-Doppler artériel doit être obtenu en urgence.
En cas de claudication intermittente, le diagnostic d’AOMI est quasiment un diagnostic d’interrogatoire, les claudications neurologiques ayant une autre sémiologie.
En cas d’examen clinique anormal des trajets vasculaires, le diagnostic d’AOMI est sûr ou probable. Il est certain s’il existe un souffle vasculaire (iliaque ou fémoral), un anévrisme ou une abolition d’un pouls fémoral, Il est presque certain en cas d’abolition d’un pouls tibial postérieur et est probable en cas d’abolition d’un pouls pédieux.
L’IPS est alors effectué par le doppleriste
De toute façon, dès le moindre doute, un écho-Doppler des membres inférieurs est réalisé pour confirmer le diagnostic et faire un bilan des lésions artérielles en appréciant leur topographie et en évaluant leur degré de sténose.
La mesure de l’IPS peut être alors demandée à l’opérateur. Elle confirme le diagnostic et contribue à apprécier le degré de gravité de l’ischémie (surtout en cas d’ischémie critique).
Soit un écho-Doppler artériel ne s’impose pas
Le patient est asymptomatique et l’examen clinique des trajets vasculaires ne révèle aucune anomalie. Pour autant, et même s’il s’agit d’un patient mobile sans claudication, une AOMI asymptomatique est possible.
Comme de nombreuses pathologies, la prévalence de cette pathologie augmente avec l’âge. On estime que l’AOMI concerne plus de 10 % des personnes de plus de 70 ans et plus de 20 % des personnes âgées de plus de 75 ans. Faut-il pour autant dépister systématiquement l’AOMI chez toute personne âgée et si oui à partir de quel âge ?
Il n’y a en l’état actuel de nos connaissances aucun argument en faveur d’un dépistage systématique par le praticien, muni d’un Doppler de poche permettant l’évaluation de l’IPS. Il est toutefois possible de raisonner en fonction de populations à risque.
Quand mesurer l’IPS ?
Dans le cadre d’une hospitalisation
Détecter une AOMI de principe apparaît utile chez les patients âgés hospitalisés quelle que soit la cause. On peut ici se référer à l’étude ELLIPSE qui a trouvé 45 % de patients âgés hospitalisés avec un IPS pathologique.
Étude ELLIPSE
Cette étude épidémiologique, observationnelle, multicentrique, menée en France sur 6 mois en 2007 sur plus de 2 000 malades hospitalisés tout venants de plus de 55 ans et d’âge moyen 73 ans et sans AOMI connue a trouvé 42 % de sujets avec un IPS < 0,90 (4 % avec un IPS < 0,50, 12 % avec un IPS entre 0,50 et 0,70, 26 % avec un IPS entre 0,70 et 0,90), et 3 % de sujets avec un IPS ≤ 1,30.
On peut donc imaginer que l’utilisation du Doppler de poche puisse être systématisée au cours de l’hospitalisation de tout sujet âgé.
Et en ambulatoire ?
Détecter de principe une AOMI en suivi ambulatoire apparaît raisonnable, quel que soit leur âge, chez des sujets :
- ayant un antécédent coronarien ou cérébrovasculaire, ce qui est étayé par le registre REACH qui retrouve une AOMI chez un quart des coronariens et plus d’un tiers des cérébrovasculaires ;
- ayant au moins un facteur de risque vasculaires connus comme une HTA ou une hypercholestérolémie et avec mention particulière pour le tabagisme et un diabète évoluant depuis une dizaine d’années ;
- ayant une neuropathie périphérique (diabétique en tête) qui peut abolir toute douleur d’effort.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :