Études
Publié le 22 avr 2008Lecture 10 min
Les registres ne sont-ils pas plus utiles au clinicien que les essais randomisés ?
J.-P. CAMBOU, CHU Rangueil, Toulouse et Société française de cardiologie, Paris
La médecine fondée sur les preuves, l’ « evidence-based medicine » ou « médecine factuelle », est devenue le pivot de notre mode de pensée médicale et les études prospectives randomisées en constituent la base. Les contraintes méthodologiques imposées par les études prospectives sont telles qu’elles ne peuvent inclure qu’une très faible proportion des malades présentant la maladie qu’elles ont pour objet d’étudier. Il s’ensuit un biais de sélection. La question posée par cet article est de savoir si les médecins doivent continuer à perdre leur temps et leur énergie à collecter des données dans les différents registres mis en place en France ou bien s’ils doivent attendre les résultats des grands essais randomisés pour adapter leurs pratiques.
La médecine fondée sur les preuves, ou « médecine factuelle », est devenue le pivot de notre mode de pensée médicale et les études prospectives randomisées en constituent la base. Les bonnes pratiques médicales supposent une adéquation entre la pratique et les recommandations des différents consensus publiés par l’HAS, l’ACC/AHA, l’ESC ou la SFC. Tous ces textes classent leurs préconisations par grade, le grade le plus élevé correspondant aux recommandations découlant des résultats d’essais randomisés, si possible menés en double-aveugle contre placebo ou traitement de référence. Ces études sont indispensables et ont fait progresser de manière considérable la médecine en général, et la cardiologie en particulier. Pourtant, la médecine fondée sur les preuves ne peut se résumer à l’analyse (ou à la métaanalyse) des essais thérapeutiques prospectifs randomisés.
Des outils permettant de vérifier que les conclusions tirées de ces études sont pertinentes pour l’exercice clinique au quotidien sont indispensables.
Il apparaît clairement que si ces essais cliniques apportent des informations « valides », ces dernières ne peuvent pas être transposées de manière mécanique dans la pratique quotidienne du fait du « biais » de sélection inhérent à tout essai randomisé. Celui-ci serait donc « valide » mais non « exportable » ou généralisable du fait d’un écart parfois considérable entre la pratique quotidienne et la population prise en charge dans les essais (tableau 1).
En effet, les contraintes méthodologiques imposées par les études prospectives sont telles qu’elles ne peuvent inclure qu’une très faible proportion des malades présentant la maladie qu’elles ont pour objet d’étudier. Il s’ensuit un biais de sélection, plus ou moins important en fonction de la question posée, et qui mérite qu’on s’intéresse, en complément, à la façon dont est prise en charge au quotidien, dans le « monde réel » la maladie en question. Et c’est justement l’objet des registres que de collecter le plus possible de données sur les pratiques effectives dans tel ou tel domaine. Les registres offrent ainsi plusieurs types de renseignements.
Données épidémiologiques
Un registre peut être mis en place rapidement, il peut être « dupliqué » et répété à intervalles réguliers. Il permet donc d’appréhender les changements de l’histoire naturelle de la maladie et de fournir des données descriptives. Dans le cadre d’une étude transversale, ces données sont complémentaires de celles fournies par les statistiques nationales (INSEE, CREDES, CNAMTS). Il faut savoir cependant identifier les limites liées au manque de représentativité de la population examinée (en particulier pour les registres monocentriques) du fait de l’absence de dénominateur (le recrutement d’un service ne peut être rapporté à une population précise).
La vérification de l’application des recommandations dans la pratique courante
Le registre permet une connaissance des pratiques dans un service hospitalier donné : il est possible de connaître les examens pratiqués, la stratégie thérapeutique réellement mise en route pendant l’hospitalisation ainsi que les prescriptions à la sortie de l’hôpital. Le registre permet de confronter la réalité des pratiques médicales avec les recommandations et les consensus et, à contrario, de confronter les recommandations avec le « monde réel ». Les registres peuvent mettre en évidence un comportement particulier et permettre une prise de conscience. Les résultats peuvent servir de base à une discussion sur les pratiques. L’écart observé entre « ce qui se dit » et ce « qui est fait » permet une réorientation des pratiques. En outre, les résultats des registres sont repris par les médias, les journaux médicaux, la grande presse généraliste, avec un impact possible en retour sur les enseignants, les étudiants, les internes.
Des comparaisons entre pays
La publication de données à partir d’un registre international permet une comparaison des pratiques. Un certain nombre de registres internationaux ont fait avancer la réflexion : ainsi, le registre MONICA (multinational MONItoring of trends and determinants in CArdiovascular disease) nous a permis de mieux connaître l’évolution de l’incidence et de la mortalité de la maladie coronaire dans le monde industrialisé ; l’étude EUROASPIRE (European Action on Secondary and Primary Prevention by Intervention to Reduce Events) a apporté des informations majeures sur le contrôle des facteurs de risque en prévention secondaire, le registre REACH (REduction of Atherothrombosis for Continued Health) a enrichi nos connaissances sur l’histoire naturelle, la prise en charge, et le devenir des patients artériopathes.
Le registre peut être la première étape avant la mise en place d’un essai thérapeutique
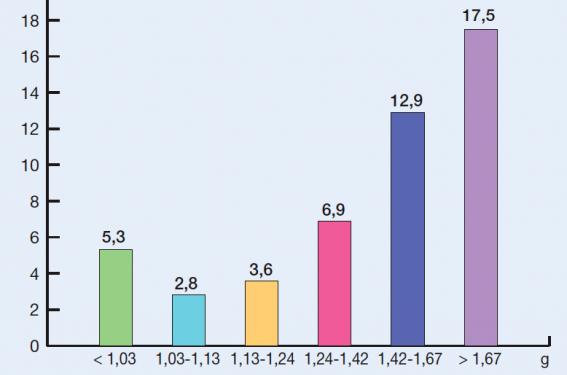
Un registre permet de fournir les informations pour le calcul du nombre de sujets nécessaires à l’étude (connaissance de la distribution des variables comme le sexe, l’âge, la morbidité, la mortalité, la prévalence des facteurs de risque et des traitements). L’analyse des données des registres permet aussi de poser des questions qui devront être résolues par les essais thérapeutiques. Ainsi, dans USIC 2000, une relation a été trouvée entre la glycémie d’entrée et le pronostic (figure 1), ce qui pourrait, à terme, avoir des retombées thérapeutiques
Figure 1. Étude USIC 2000 : mortalité à 30 jours en fonction de la glycémie à l’admission*.
Les registres permettent de savoir si les populations des essais thérapeutiques sont comparables à celles du « monde réel »
Plusieurs publications montrent que, parmi des patients vus tous les jours par les cardiologues, les patients exclus des essais thérapeutiques sont majoritaires (jusqu’à 60 à 70 %). Ces patients inéligibles sont plus graves, plus âgés, avec plus de comorbidités (en particulier plus d’insuffisance cardiaque et plus de diabète.) Les registres permettent de vérifier si les conclusions des essais randomisés peuvent être extrapolées à ces patients. À titre d’exemple, les essais thérapeutiques montrent un pronostic équivalent des patients avec IDM sans élévation du segment ST dans le groupe « angioplastie » et dans le groupe « pontage », alors que les patients du groupe angioplastie ont plus souvent des resténoses que ceux du groupe ponté. Dans le registre Euro-Heart-Survey Revascularisation, des résultats similaires sont retrouvés dans le groupe des patients éligibles pour un essai thérapeutique, alors que dans le groupe des patients inéligibles, les patients pontés ont un pronostic plus péjoratif (décès totaux ou bien décès ou récidives d’infarctus). Ce registre a pu montrer que, dans les essais comparatifs entre angioplastie et pontage, on est loin du monde réel du fait de la randomisation qui ne peut par définition tenir compte des indications particulières de chaque modalité de prise en charge dans la vraie vie.
Les registres permettent de vérifier si les conclusions des essais randomisés peuvent s’appliquer à des populations de patients peu ou pas incluses dans les essais thérapeutiques (sujets très jeunes, très âgés, insuffisants rénaux, femmes enceintes).
Un des meilleurs exemples en est celui des populations âgées.
La population de sujets âgés dans les études réalisées au stade aigu de l’infarctus est souvent numériquement peu importante, si bien que le bien-fondé même de l’utilisation de la thrombolyse dans cette population a pu être contesté. Les registres permettent de vérifier si, dans les conditions d’emploi quotidiennes, la thrombolyse apparaît plutôt bénéfique ou plutôt délétère chez ces patients. Dans le registre USIK 1995, dans USIC 2000 et dans FAST MI, la survie à un an des patients âgés ayant un traitement de reperfusion par thrombolyse ou angioplastie est significativement meilleure que celle des patients n’ayant pas eu un tel traitement. L’effet bénéfique du traitement de reperfusion est maintenu, même après ajustement par analyse multivariée.
Les patients diabétiques, hospitalisés pour infarctus : chez ces patients, le possible effet délétère des sulfamides hypoglycémiants, dont certains inhibent les canaux potassiques myocardiques et suppriment les mécanismes de reconditionnement ischémique, a été évoqué. Dans le registre USIC 2000 puis dans FAST MI, la mortalité hospitalière des patients diabétiques sous sulfamides est significativement plus faible que celle des diabétiques ne recevant pas de sulfamides, et cela, en dépit des caractéristiques initiales plus sévères (en particulier du plus grand âge) du premier groupe. Ici encore, l’impact favorable des sulfamides est constaté après ajustement en analyse multivariée.
Un simple registre permet donc de répondre, au moins partiellement à deux questions d’importance clinique quotidienne : au stade aigu d’un infarctus, il n’y a pas de risque particulier à traiter les patients âgés par thrombolyse (ou angioplastie) et le traitement par sulfamides hypoglycémiants n’a pas d’effet délétère (et pourrait même s’avérer bénéfique) chez les sujets diabétiques.
Les registres peuvent permettre de vérifier l’impact dans le monde réel de certaines thérapeutiques préconisées dans les guidelines
Dès lors qu’une molécule est recommandée, aucun essai thérapeutique ne peut plus être mis en place avec un bras placebo.
Par exemple, il est actuellement impossible de vérifier l’impact des IEC chez les artériopathes. Les recommandations se basent sur une seule étude (HOPE). Cette étude fournit des informations pronostiques de morbi-mortalité chez des patients à haut risque, dont des artériopathes, mais le stade de l’AOMI n’est pas connu et il n’y a aucune donnée sur le devenir du membre (taux d’amputations). Seuls les registres vont pouvoir répondre, à l’avenir, à cette question importante : doit-on prescrire un IEC à tous les artériopathes et en particulier doit-on l’utiliser (et à quelle dose ?) chez tous les patients en ischémie critique ?
De même, il est impossible de valider l’impact des polypills.
L’effet de l’association aspirine/pravastatine a été mis en évidence par une métaanalyse qui a repris les données des essais thérapeutiques (Hennekens) sur la pravastatine ; ces résultats ont été confirmés par le registre Prevenir 3 (figures 2 et 3). Dans ce registre, 10 % des patients n’étaient traités ni par aspirine ni par pravastatine, ce qui a permis de constituer un groupe témoinjouant le rôle de groupe placebo.
Figure 2. PREVENIR 3 : analyse multivariée. (D’après Cardiovasc Drugs Ther. 2006 ; 20 (1) : 55-61). (réf. Pas de statines ni AAP)*
Figure 3. Mortalité totale selon la prescription de statines ou d’antiagrégants plaquettaires. (D’après Cardiovasc Drugs Ther. 2006 ; 20 (1) : 55-61).
Les registres peuvent répondre à des questions scientifiques
À titre d’exemple, le registre USIK 1995 a confirmé l’intérêt pronostique du traitement par inhibiteurs de l’enzyme de conversion (IEC) après un infarctus avec fonction ventriculaire gauche altérée. Chez les malades avec une fraction d’éjection ≤ 35 %, la survie à un an est de 68 % chez les patients recevant des IEC, contre 35 % chez ceux n’en recevant pas. L’analyse multivariée confirme la valeur prédictive indépendante de ce traitement avec une diminution du risque de décès de plus de 50 % chez les patients recevant un IEC.
À l’inverse, les études randomisées comparant angioplastie primaire et thrombolyse ont montré la supériorité de la technique de reperfusion mécanique. Cependant, elles ont été réalisées dans des centres performants et motivés, ce qui ne reflète pas forcément la réalité du terrain à l’échelle d’un pays. De fait, les résultats de l’étude USIC 1995 puis USIC 2000, et plus récemment FAST-MI ne retrouvent pas cette supériorité de l’angioplastie : la population des patients dilatés et celle des patients thrombolysés ont des caractéristiques initiales très voisines. À un an, la survie est comparable dans les deux groupes. En utilisant des techniques d’analyse multivariée, le type de traitement de reperfusion n’est pas un élément pronostique. Ainsi, les conclusions d’études réalisées dans des centres sélectionnés semblent ne pas se vérifier à l’échelle de notre pays : les conditions d’utilisation au quotidien de l’angioplastie primaire font sans doute qu’elle y perd son avantage par rapport à la thrombolyse intraveineuse, dont la mise en œuvre est évidemment plus aisée.
Quelques précautions à prendre avant la mise en place d’un registre
Si les registres fournissent de très nombreux éléments de réflexion, ils ne peuvent répondre avec la même rigueur que les études randomisées aux questions concernant l’apport formel d’une thérapeutique. Afin d’améliorer la qualité d’un registre, quelques écueils majeurs doivent être évités (tableaux 2 et 3) :
– il faut d’emblée faire le choix entre un registre permettant de valider des pratiques (il peut compter peu de variables) et un registre ayant vocation à répondre à des questions scientifiques (il doit être le plus exhaustif et détaillé possible) ;
– il faut aussi se poser la question de l’intérêt d’un registre continu (lourd à gérer) ; il est souvent préférable d’enregistrer tous les cas consécutifs sur une période de temps ;
– il faut éviter en revanche l’inclusion d’un nombre de patients prédéterminés par centre (manque de représentativité).
En pratique
Les registres et les essais thérapeutiques n’ont pas le même objectif, le même but.
Les essais ont des limites bien connues mais servent à comparer deux groupes de patients comparables, les opposer n’a pas de sens.
Les registres sont avant tout un outil d’information et d’évaluation des pratiques. Pour qu’un registre puisse apporter des réponses à des questions « scientifiques », il faut qu’il se donne les moyens en termes d’exhaustivité, de qualité du recueil à la phase initiale ; il doit y avoir un suivi qui doit obligatoirement dépasser la durée de la phase hospitalière.
Les registres, outre leur intérêt sur le plan épidémiologique, fournissent des informations cliniques complémentaires de celles des études randomisées contrôlées. Elles permettent à la fois de vérifier la pertinence, sur le terrain, des conclusions de ces dernières, et d’apporter des éléments de réponse à d’autres questions que celles-ci ne peuvent résoudre.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :