Congrès et symposiums
Publié le 01 mar 2020Lecture 8 min
Avancées dans l’ischémie myocardique et l’insuffisance cardiaque - Focus sur le patient diabétique
Le pronostic du patient diabétique est en grande partie dépendant des complications cardiovasculaires. La prise en charge de la maladie athéromateuse et de ses complications a beaucoup progressé mais il reste une marge de progrès dans la prévention des complications qui passe par la stratification du risque et l’amélioration des stratégies thérapeutiques en prévention secondaire. Le diabète est aussi un facteur de risque d’insuffisance cardiaque indépendamment des événements ischémiques. À ces deux titres, il pourrait bénéficier d’un traitement par iSGLT2.
Quel dépistage de la maladie athéromateuse ?
La stratification du risque chez le patient diabétique est complexe. Il est relativement facile d’identifier les patients à bas risque a priori (< 10 ans de diabète et absence d’autres facteurs de risque) de même que les patients à très haut risque (dysfonction rénale, ECG anormal, rétinopathie, échographie anormale). En revanche, tous les autres patients nécessiteront un bilan plus approfondi pour mieux cerner leur risque.
L’utilisation du CAC score permet probablement de mieux déterminer le risque cardiovasculaire en évaluant la charge athéromateuse par la mesure du volume des calcifications. L’existence d’un score d’Agatston très élevé est associé à une multiplication par 8-10 du risque de mortalité ou d’événement cardiovasculaire comparativement à un score bas ; inversement, un score nul indique un très bas risque. Sur 1 045 patients diabétiques de type 2 asymptomatiques examinés à l’hôpital Lariboisière, près de la moitié avaient un score < 10 ; 20-40 % avaient un score élevé, et pourraient bénéficier d’une approche préventive. Le CAC score varie selon plusieurs paramètres : le sexe, l’origine ethnique et l’âge. L’échographie permet aussi d’évaluer le pronostic du patient.
Chez un patient diabétique, la stratégie d’évaluation du risque repose initialement sur l’ECG et la biologie. Si le patient est à risque modéré (DT < 10 ans, pas de facteurs de risque), il n’est pas nécessaire de poursuivre le bilan ; s’il est à très haut risque d’emblée (protéinurie, insuffisance rénale, rétinopathie) et chez les patients dont le risque est incertain, un écho-Doppler et un CAC score, éventuellement complétés par un test de stress pour rechercher une ischémie silencieuse permettent de mieux stratifier le risque et de déterminer les cibles de traitement :
– haut risque : LDL-C < 0,70 g/l, pas d’aspirine en prévention primaire ;
– très haut risque : LDL-C < 0,55 g/l, l’aspirine peut être indiquée.
Quelle inhibition plaquettaire chez le patient diabétique ?
Les patients diabétiques ayant fait un IDM ou un AVC sont une population à très haut risque.
Selon les données du registre suédois, les sujets diabétiques ayant une maladie coronaire stable sont aussi à haut risque : l’estimation à 3 ans du risque de décès, IDM ou AVC ajustée sur l’âge et le sexe montre la même incidence de 13 %. Cette population justifie d’un traitement antiagrégant antiplaquettaire (AAP), essentiellement une monothérapie par aspirine. Cependant, l’aspirine a des limites chez le diabétique, entre autres liées au turn-over accéléré des plaquettes. Une administration en deux prises pourrait être plus efficace ; l’essai Andaman comparant monoprise et biprise chez les diabétiques ayant un SCA permettra de trancher la question. Le clopidogrel un peu plus efficace que l’aspirine chez le diabétique ; certains patients sont néanmoins de médiocres répondeurs, davantage chez les diabétiques que les non diabétiques (38 % vs 8 %).
Qu’en est-il des autres AAP ?
Nous disposons de données sur le ticagrelor grâce aux études PLATO dans le SCA et PEGASUS chez les sujets en post-IDM à haut risque, qui montrent la supériorité du ticagrelor vs aspirine/clopidogrel et aspirine seule, avec un bénéfice concordant chez les diabétiques et les non-diabétiques. Nous disposons de quelques données chez les coronariens stables diabétiques grâce à l’étude CHARISMA qui comparait aspirine + clopidogrel à l’aspirine seule chez des patients à haut risque cardiovasculaire ou avec une athérothrombose avérée ; l’étude n’a pas montré de supériorité de la bithérapie, mais l’effet était hétérogène selon ces deux sous-groupes. Apparemment il n’y a pas de bénéfice en prévention primaire chez les diabétiques, voire un effet délétère.
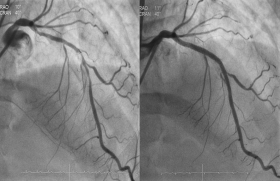
L’étude THEMIS a recruté des patients diabétiques de type 2 avec une maladie coronaire avérée (sans antécédent d’IDM ou AVC), définie par un antécédent d’angioplastie coronaire, de pontage ou une sténose coronaire angiographique. Les patients recevaient tous de l’aspirine à faible dose et étaient randomisés pour recevoir du ticagrelor ou un placebo. L’étude montre qu’il s’agit clairement d’une population à haut risque (13 % d’événements à 5 ans) et qu’il y a un bénéfice à adjoindre du ticagrelor qui réduit le taux d’événements d’environ 10 %. La mortalité cardiovasculaire n’est pas significativement diminuée mais il y a moins d’IDM et d’AVC ischémiques et une réduction de 50 % des événements périphériques et des amputations. Le prix à payer est un doublement du risque de saignement graves, statistiquement significatif, et une augmentation des hémorragies intracrâniennes, donc un bénéfice/risque discutable. Le bénéfice clinique net est différent selon les populations ayant un antécédent d’angioplastie coronaire (soit environ la moitié de la population) ou non : il est présent dans le premier cas avec une différence significative de 15 % et un effet plutôt délétère en son absence. Ce meilleur rapport bénéfice/risque chez les patients ayant déjà eu une angioplastie s’expliquerait parce que les patients ont déjà toléré une bithérapie.
Pour 1 000 patients avec antécédent d’angioplastie coronaire traités pendant 3 ans, on prévient 15 événements ischémiques sans excès d’hémorragie intracrânienne ou mortelle, soit un bénéfice net de 15 événements ; en l’absence d’antécédent d’angioplastie, on entraîne surtout des hémorragies. Le bénéfice du traitement sur la prévention des événements ischémiques dure au moins 6 ans, peut-être 10 ans, après l’angioplastie.
Comment évaluer le risque d’insuffisance cardiaque en pratique ?
Le diabète est un facteur de risque important d’insuffisance cardiaque (IC x 2,5) indépendamment des événements ischémiques, de l’HTA ou de l’obésité. Il aggrave le pronostic de l’IC qu’il s’agisse d’IC à fraction d’éjection préservée ou altérée. Le lien entre diabète et IC est tellement étroit qu’il est bidirectionnel ; l’insuffisance cardiaque s’accompagne souvent d’insulinorésistance qui peut conduire au diabète via des phénomènes d’activation sympathique. Les causes d’insuffisance cardiaque chez le diabétique sont multiples : sédentarité, obésité, hypertension, qui prédisposent à développer des coronaropathies, une FA, une cardiomyopathie diabétique, une sténose aortique. Dans 75 % des cas, il s’agit d’une IC à FE préservée. La cardiomyopathie spécifique du diabète est confirmée dans des modèles murins, en lien avec le stress oxydatif, la lipotoxicité et la dysfonction mitochondriale, qui aboutissent à une rigidité myocardique, une hypertrophie et la fibrose.
Une forme préclinique d’insuffisance cardiaque a été décrite dans les études échocardiographiques et IRM. Chez des patients diabétiques sans pathologie vasculaire avérée, on peut mettre en évidence la présence d’une HVG ou d’un remodelage concentrique et, chez un quart des patients, une altération de la fonction systolique VG qui se traduit par la diminution du strain global longitudinal et fréquemment une dysfonction diastolique.
C’est ce que les Américains appellent le « stage B heart failure » (altérations structurelles et fonctionnelles mais asymptomatiques). Cette forme préclinique d’insuffisance cardiaque s’accompagne d’une réduction de la capacité à l’effort. L’identification de ces formes cliniques d’IC a un impact pronostique car la dysfonction diastolique est un facteur de risque d’insuffisance cardiaque et de mortalité. Une analyse en clusters réalisée à l’hôpital Henri Mondor a permis de discerner 3 groupes de patients en échographie : un groupe plutôt constitué d’hommes jeunes avec un faible risque de mortalité et hospitalisation ; un groupe de femmes hypertendues, obèses avec dysfonction diastolique ; un groupe d’hommes avec HVG et strain altéré, dont le pronostic est moins bon. Les deux éléments pronostiques les plus défavorables sont la présence d’une HVG et d’une altération du strain.
Il est donc possible d’identifier, parmi les patients diabétiques, ceux qui sont à risque d’IC et de mortalité cardiovasculaire, mais ces données devront être validées sur des cohortes pour affiner les indices pronostiques. Ces patients à risque pourraient bénéficier d’une intensification de la prise en charge des facteurs de risque cardiovasculaire et sans doute d’un iSGLT2.
iSGLT2 dans l’insuffisance cardiaque : de la prévention au traitement
Les données de la cohorte lilloise CORONOR montrent qu’indépendamment de la récidive d’un événements coronarien aigu, un patient coronarien stable est exposé à de multiples complications qui augmentent le risque de mortalité à 5 ans : IDM x 2, AVC x 6, IC x 12, hémorragie intracrânienne x 24. Les facteurs favorisant la survenue d’une IC chez un coronarien stable sont l’âge, le diabète et l’HTA. Le risque de décès à 3 ans en présence d’une IC est de 25 %. L’existence d’un diabète traité aggrave le pronostic.
Plusieurs études des iSGLT2 ont fait la preuve de leurs bénéfices cardiovasculaires sur l’amélioration du MACE 3, et une réduction des hospitalisations pour IC. L’étude DECLARE TIMI-58 a été la première à montrer une amélioration pronostique de 17 % de l’insuffisance cardiaque, décès ou hospitalisation pour IC. Elle a confirmé les résultats des précédentes études et montré que l’amélioration du pronostic passe essentiellement par la réduction des hospitalisations pour IC ou des visites en urgence pour décompensation avec nécessité d’un traitement injectable.
L’étude DAPA-HF a été réalisée chez des patients avec une IC à FE réduite (31 %), symptomatiques, dont 40 % avaient un diabète connu à l’inclusion ; ces patients étaient particulièrement bien traités (un quart avec un défibrillateur implanté, 70 % sous ARM). L’étude a montré une réduction significative de 26 % du critère principal de jugement, hospitalisation ou traitement injectable en urgence pour IC ou décès cardiovasculaire. La stratification des résultats sur l’existence ou non d’un diabète ne montre aucune interaction. Cette molécule conçue comme antidiabétique améliore l’insuffisance cardiaque chez le diabétique et chez le patient le non diabétique. Les effets bénéfiques des iSGLT2 passent notamment par leur action sur l’hémodynamique rénale ; chez le diabétique il existe des modifications de l’artériole afférente qui participent à une hyperfiltration glomérulaire et vont induire une glomérulosclérose diabétique. Expérimentalement, une amélioration des anomalies myocardiques est également observée sous iSGLT2.
Des études ancillaires montrent que les malades coronariens qui sont à risque accru d’IC, pourraient bénéficier de la dapagliflozine ; une forte interaction est observée avec les anomalies de la fonction rénale rénales (protéinurie et altération de la filtration glomérulaire). Par ailleurs, le bénéfice de la dapagliflozine apparaît plus important quand le NT-proBNP est augmenté. Ce marqueur pourrait servir à identifier les patients les plus à même de tirer bénéfice du traitement.
D’après un symposium AstraZeneca avec la participation de P. Henry, P.G. Steg, L. Ernande et N. Lamblin
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :