Publié le 01 déc 2017Lecture 5 min
Utilité de l’échographie pulmonaire pour le cardiologue
Arnaud HUBERT, Erwan DONAL, CHU de Rennes

Bien que connue — et pratiquée — depuis de nombreuses années par les anesthésistes-réanimateurs, l’échographie pulmonaire, avec notamment les comètes, reste largement méconnue et donc sous-utilisée par les cardiologues. Sa simplicité et sa grande disponibilité peuvent pourtant permettre de clarifier rapidement des situations litigieuses ou difficiles, notamment lorsque l’examen clinique n’est pas contributif (d’où son utilisation en réanimation).
Diagnostic d’insuffisance ventriculaire gauche (IVG)
Après une description rapide dans les années 80(1,2), cette découverte des comètes est pourtant française, par l’équipe de Lichtenstein en 1997, qui avait mis en évidence une corrélation entre des artéfacts à l’échographie pulmonaire qu’il appelle alors comète et une infiltration alvéolo-interstitielle au scanner thoracique témoignant d’un œdème aigu pulmonaire(3).
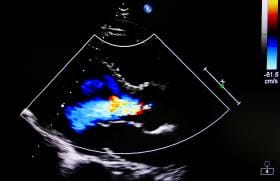
La comète pulmonaire se définit comme une « ligne discrète, comme un laser, verticale, hyperéchogène, partant de la ligne pleurale et atteignant le bas de l’image sans interruption, bougeant de façon synchronisée avec la respiration »(4) (figures 1 à 3).
Figure 1. Exemple de comète pulmonaire, appelée aussi « ligne B » (ici avec une sonde convexe).
Figure 2. Exemple d’un échographe protable, le Vscan® dual-probe, commercialisé par General Electrics.
Figure 3. Le patient est considéré en IVG si on note la présence de lignes B bilatérales avec un nombre total supérieur ou égal à 5(16)
Elle peut aussi être appelée « ligne B », en opposition par exemple aux lignes A, correspondant à la réflexion de la ligne pleurale. Pour réaliser une échographie pulmonaire, il suffit de placer une sonde d’échographie (soit convexe, i.e. une sonde d’échocardiographie classique, soit linéaire, i.e. une sonde utilisée pour le vasculaire). Afin de s’assurer d’une bonne qualité de l’image, il est indispensable de visualiser la ligne pleurale qui bouge au rythme de la respiration.
Depuis sa découverte, de nombreuses études ont prouvé sa valeur, démontrant sa corrélation pour affirmer le diagnostic d’œdème pulmonaire avec la radiographie thoracique(5), les NTproBNP(6), le rapport E/A en Doppler pulsé à l’anneau mitral(7), le rapport E/e’(8), ainsi que la pression capillaire pulmonaire moyenne mesurée par cathétérisme cardiaque(9). Par ailleurs, dans chacune de ces études, le nombre de lignes B était proportionnel au degré de congestion pulmonaire et au niveau de pression capillaire pulmonaire. La présence de cet artéfact à un seuil significatif, qui peut varier selon les techniques utilisées (soit un protocole « rapide » d’analyse de chaque hémithorax en 4 points soit une analyse de chaque hémithorax en 14 points), reflète donc une pression capillaire pulmonaire moyenne supérieure à 15 mmHg. Il a par ailleurs été démontré la capacité de cette méthode à détecter un œdème pulmonaire infraclinique(10). Aucune étude n’a cependant été réalisée pour démontrer une relation entre la quantité de lignes B et l’élévation de la pression télédiastolique du ventricule gauche.
Quelques diagnostics différentiels de l’œdème pulmonaire sont à connaître en présence de lignes B, les deux principalement rencontrées étant la pneumopathie infectieuse (lignes B en regard du foyer de condensation pulmonaire, pouvant orienter à tort sur un œdème aigu pulmonaire si la pneumopathie est bilatérale) et la fibrose pulmonaire.
Suite à ces études réalisées grâce à des échographes standards, d’autres ont pu démontrer la faisabilité de cette technique avec des échographes portables(11,12) (figures 2 et 4) permettant ainsi d’augmenter significativement la disponibilité de cet examen, notamment en pouvant le réaliser en consultation d’insuffisance cardiaque pour des patients ambulatoires. Platz et coll.(12) ont ainsi très récemment pu mettre en évidence que le tiers de patients qui présentait le plus de lignes B, mesurées avec un échographe portable, avaient quatre fois plus de risques d’hospitalisation et de mortalité toutes causes (HR = 4,08) par rapport au tiers de patients qui en présentait le moins. Parmi le tiers le plus à risque, 81 % des patients avaient une auscultation pulmonaire normale, confirmant la valeur ajoutée de cet examen par rapport à l’examen clinique. Cette morbi-mortalité accrue des patients ayant de nombreuses lignes B a également été démontrée pour des patients sortant d’hospitalisation pour insuffisance cardiaque(13). La grande accessibilité de l’échographe portable permet également de l’utiliser pour faciliter le diagnostic d’œdème aigu pulmonaire aux urgences via l’analyse des lignes B, qui permet d’apporter une valeur ajoutée aux NT-proBNP et à la clinique en termes de sensibilité et de spécificité(8).
Figure 4. Exemple d’un examen au lit du patient.
Un autre avantage non négligeable de cette méthode est sa simplicité, ce qui permet de réaliser une échographie pulmonaire fiable en peu de temps (3 minutes en moyenne), à moindre coût (surtout en cardiologie avec la disponibilité des échographes), avec une courbe d’apprentissage très rapide, même chez les novices en échographie.
Malgré cette littérature relativement riche, l’échographie pulmonaire pour la recherche de comètes n’apparaît que très peu dans les grandes recommandations internationales cardiologiques, en dehors de papiers de recommandations d’experts principalement destinés aux médecins urgentistes(14). Elle n’est par ailleurs pas citée dans les recommandations américaines les plus récentes sur l’évaluation des pressions de remplissage et de dysfonction diastolique du ventricule gauche(15).
Au vu des résultats scientifiques récents, il est cependant très probable que cet examen apparaîtra plus distinctement dans les recommandations afin de populariser chez les cardiologues cette technique qui est à tort sous-utilisée (beaucoup plus utilisé par les urgentistes et réanimateurs mais trop peu par le cardiologue, pourtant l’information est complémentaire à celle de l’analyse des structures et des flux intracardiaques).
Localisation et quantification des épanchements pleuraux
C’est l’indication historique de l’échographie pulmonaire pour confirmer et affiner une suspicion clinique d’épanchement pleural. La situation la plus fréquente en cardiologie est l’épanchement par transsudat provoqué par une insuffisance cardiaque droite. Cet épanchement est hypoéchogène et donc noir et homogène sur une image échographique. Le parenchyme pulmonaire en regard apparaît hyperéchogène, avec des mouvements rythmés par la respiration du patient. L’échographie permet de repérer avant, pendant et après un geste de drainage pleural.
En pratique
L’échographie pulmonaire permet une évaluation hémodynamique non négligeable des patients cardiopathes, notamment pour apprécier une insuffisance ventriculaire gauche débutante ou de diagnostic difficile.
Sa praticité et sa simplicité permettent une utilisation au quotidien de cette technique, potentialisant l’échographie cardiaque (avec les mêmes sondes et les mêmes échographes) pour débrouiller des situations cliniques litigieuses.
La recherche à ce sujet est actuellement dynamique et va permettre à court terme sa popularisation chez les cardiologues.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :