Publié le 11 sep 2007Lecture 14 min
Les clés de l'examen échocardiographique de l'insuffisance mitrale organique
B. GALLET, centre hospitalier Victor Dupouy, Argenteuil
L’examen échocardiographique d’une insuffisance mitrale (IM) doit répondre à trois questions fondamentales dont dépendra la prise en charge ultérieure et qui concernent son importance, son retentissement et les possibilités de chirurgie conservatrice. Seules seront envisagées ici les insuffisances mitrales organiques, à l’exclusion des fuites ischémiques et fonctionnelles dont l’abord est différent.
Quantification de l’IM
Elle repose actuellement sur les recommandations de l’American Society of Echocardiography (ASE), publiées en 2003, qui classent les IM en trois catégories (modérées, moyennes et importantes) en se basant sur une approche multiparamétrique. Ces recommandations distinguent des « signes spécifiques », dont la spécificité pour affirmer qu’une fuite est sévère ou modérée est d’au moins 90 %, et des « signes d’orientation », qui sont moins robustes mais peuvent être utiles dans les cas douteux. Le recours aux méthodes quantitatives est recommandé dès que l’IM apparaît plus que modérée. Ces méthodes quantitatives, basées sur l’analyse de la zone de convergence (ou PISA) ou sur le Doppler quantitatif, permettent le calcul de la surface d’orifice régurgitant (SOR), du volume régurgitant et de la fraction de régurgitation.
IM importante
Il existe quatre signes spécifiques d’une fuite mitrale volumineuse :
- un aspect de « valve mitrale flottante » qui correspond le plus souvent à une rupture de cordages ;
- une largeur de la vena contracta d’au moins 7 mm associée à un large jet central ou à un jet excentré tournant dans l’oreillette gauche ;
- une zone de convergence importante définie par un rayon d’au moins 9 mm pour une vitesse d’aliasing de 40 cm/s ;
- une inversion du flux systolique des veines pulmonaires, en sachant que l’ETT est à cet égard spécifique mais peu sensible car seule la veine pulmonaire supérieure droite est généralement analysable, alors que l’ETO est à la fois sensible et spécifique car elle permet d’analyser l’ensemble des veines pulmonaires (figures 1 à 4).
Les signes d’orientation pouvant étayer le diagnostic sont :
- une accélération de la vitesse de l’onde E mitrale dépassant 1,2 m/s ;
- un aspect triangulaire du flux d’insuffisance mitrale en Doppler continu qui représente l’équivalent de l’onde V géante observée au cathétérisme sur la courbe de pression capillaire pulmonaire ;
- une dilatation des cavités cardiaques gauches qui peut cependant manquer en cas d’IM aiguë.
Le recours aux méthodes quantitatives est nécessaire et fait plus souvent appel à l’analyse de la zone de convergence qu’au Doppler quantitatif. La fuite est volumineuse en cas de SOR d’au moins 40 mm2, de fraction de régurgitation d’au moins 50 %, et de volume régurgitant d’au moins 60 ml (tableau 1).
Figure 1. Aspect de « valve mitrale flottante » en rapport avec une rupture de cordage du feuillet mitral postérieur.
Figure 2. Vena contracta large dont le diamètre est mesuré à 8 mm.
Figure 3. Zone de convergence importante dont le rayon est mesuré à 13,5 mm pour une vitesse d’aliasing de 44 cm/s.
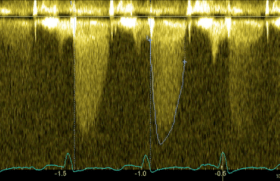
Figure 4. Inversion mésosystolique (flèche) du flux de la veine pulmonaire supérieure gauche enregistré par voie transœsophagienne.
Insuffisance mitrale modérée
Les signes spécifiques d’une fuite modérée sont :
- une largeur de la vena contracta < 3 mm ;
- une zone de convergence absente ou minime définie par un rayon < 4 mm pour une vitesse d’aliasing de 40 cm/s ;
- une surface de jet de moins de 4 cm2 à condition que le jet soit central. C’est la seule situation où les recommandations reconnaissent un intérêt à la surface du jet pour la quantification de lIM.
Les signes d’orientation en faveur d’une fuite modérée sont :
- une dominance de l’onde A du flux mitral, c’est-à-dire un rapport E/A < 1 ;
- une dominance de l’onde S du flux veineux pulmonaire c’est-à-dire un rapport S/D > 1 ;
- une morphologie parabolique du flux d’IM en Doppler continu avec un signal de faible intensité ;
- un ventricule gauche non dilaté.
Le recours aux méthodes quantitatives n’est pas nécessaire en présence de signes spécifiques de fuite modérée. Si elles étaient utilisées, elles montreraient une SOR < 20 mm2, une fraction de régurgitation < 30 %, et un volume régurgitant < 30 ml (tableau 1).
IM moyenne
Le diagnostic de fuite moyenne est évoqué quand les signes spécifiques témoignent d’une fuite qui est plus que modérée mais sans atteindre les critères d’une IM sévère. La vena contracta est généralement comprise entre 3 et 6 mm, et le rayon de la zone de convergence se situe habituellement entre 4 et 9 mm pour une vitesse d’aliasing de 40 cm/s. Les signes d’orientation sont également en zone intermédiaire.
Le recours aux méthodes quantitatives est indispensable dans cette situation. L’IM moyenne correspond à une SOR entre 20 et 40 mm2, une fraction de régurgitation entre 30 et 50 % et un volume régurgitant entre 30 et 60 ml. Ces fuites moyennes peuvent être subdivisées en deux sous-groupes : modérées à moyennes et moyennes à importantes, ce qui aboutit à retrouver une classification en quatre grades (tableau 1).
Importance de la zone de convergence et de la vena contracta
Ces deux méthodes sont les plus utiles car elles apportent des signes spécifiques pour le diagnostic d’IM modérée (vena contracta < 3 mm, rayon de la PISA < 4 mm pour une vitesse d’aliasing de 40 cm/s), et pour celui de fuite importante (vena contracta d’au moins 7 mm, rayon de la PISA d’au moins 9 mm pour une vitesse de 40 cm/s).
L’analyse de la zone de convergence est, de plus, une méthode quantitative. Elle permet le calcul de la SOR qui a des conséquences sur le pronostic et la prise en charge. Les patients ayant une SOR > 40 mm2 ont une mortalité cardiaque plus de 5 fois supérieure à celle des patients ayant une SOR < 20 mm2, selon une étude de Enriquez-Sarano rapportée en 2005. Il en résulte qu’une fuite mitrale volumineuse chez un patient asymptomatique et sans dysfonction ventriculaire gauche représente une indication opératoire admise de classe IIa, selon les recommandations ACC/AHA de 2006, à condition que la probabilité de pouvoir réaliser une plastie mitrale soit > 90 % et qu’il n’existe pas de comorbidité. Cette indication est plus discutée dans les recommandations ESC de 2007, selon lesquelles elle est en classe IIb. Si la plastie apparaît incertaine, une attitude attentiste est licite, consistant à réserver l’indication opératoire à l’apparition de symptômes, d’une dysfonction ventriculaire gauche, d’une hypertension artérielle pulmonaire ou d’une fibrillation atriale. Cette attitude attentiste n’entraîne aucune surmortalité par rapport à la survie attendue, comme l’a montré Rosenhek en 2006.
Considérations techniques
La largeur de la vena contracta est mesurée de préférence dans une incidence où le faisceau ultrasonore est perpendiculaire au jet afin de limiter les problèmes de résolution latérale, c’est-à-dire généralement en coupe parasternale longitudinale par voie transthoracique, en positionnant la focale au niveau de la vena contracta, en utilisant le zoom et en retenant la moyenne de plusieurs mesures (figure 5). La vena contracta peut également être mesurée par voie transœsophagienne.
Figure 5. Mesure de la vena contracta en incidence parasternale longitudinale (utilisation du zoom et réglage de la focale au niveau de la vena contracta).
La zone de convergence est généralement analysée par voie apicale, en utilisant le zoom et en déplaçant vers le bas la ligne de zéro de l’échelle des vitesses en Doppler couleur pour diminuer la vitesse d’aliasing entre 30 et 40 cm/s. Le rayon est mesuré en mésosystole entre la zone de premier aliasing et l’orifice régurgitant. La SOR est calculée par la formule (2pr2 x Va)/ Vitesse IM dans laquelle « r » est le rayon de la zone de convergence, « Va » la vitesse d’aliasing, et « Vitesse IM » la vitesse maximale du flux d’insuffisance mitrale (figure 6). Le volume régurgitant est obtenu en multipliant la SOR par l’intégrale temps vitesse du flux d’IM. La fraction de régurgitation est calculée en divisant le volume régurgitant par le volume total éjecté par le ventricule gauche (qui correspond à la somme du volume régurgitant et du volume d’éjection aortique).
Figure 6. Analyse de la zone de convergence. En haut à gauche : flux d’IM en Doppler couleur. En bas à gauche : mesure du rayon de la zone de convergence (r) après diminution de la vitesse d’aliasing (Va) à 35 cm/s et utilisation du zoom. En haut à droite : mesure de la vitesse maximale du flux d’IM en Doppler continu. La surface est calculée à 0,18 cm2 (toutes les valeurs utilisées dans le calcul doivent être exprimées en centimètres).
Plusieurs difficultés peuvent survenir dans l’analyse de la zone de convergence. Le confinement ou compression de la PISA par une paroi du ventricule gauche entraîne une surestimation de la SOR. Il faut alors soit augmenter la vitesse d’aliasing pour faire disparaître le confinement mais sans dépasser 10 % de la vitesse maximale du flux d’IM, soit utiliser un facteur de correction angulaire, ce qui complique la technique, soit renoncer à la méthode. En cas de double jet, il est possible d’additionner les SOR calculées individuellement pour chacun des deux jets. En cas de variations systoliques du rayon, il est recommandé d’utiliser soit le rayon mesuré en mésosystole, soit un rayon systolique moyen en mode TM. Enfin, les fuites mitrales strictement télésystoliques peuvent être considérées comme non volumineuses (figure 7).
Figure 7. Exemples de limites de l’analyse de la PISA. En haut à gauche : compression de la zone de convergence par la paroi postérieure du ventricule gauche. En haut à droite : double jet d’IM. En bas à gauche : variations systoliques du rayon de la zone de convergence en mode TM couleur par voie transœsophagienne. En bas à droite : PISA strictement télésystolique également en mode TM couleur par voie transœsophagienne.
Ces limites de l’analyse de la zone de convergence peuvent conduire à recourir au Doppler quantitatif. La technique repose sur la comparaison des débits mitral (ou du débit ventriculaire gauche) et aortique. La fraction de régurgitation est égale à la différence entre le débit mitral (ou le débit ventriculaire gauche) et le débit aortique, rapportée au débit mitral (ou au débit ventriculaire gauche). La méthode permet également le calcul de la SOR et du volume régurgitant. Les limites en sont l’insuffisance aortique, la sténose mitrale ou la présence d’une prothèse mitrale, la fibrillation atriale et la nécessité d’un apprentissage. Il est possible que la détermination des volumes ventriculaires gauches en mode 3D temps réel renouvelle cette technique qui reste actuellement peu utilisée en pratique.
Retentissement de l’IM
L’analyse du retentissement de la fuite mitrale consiste à rechercher une dysfonction ventriculaire gauche ou une hypertension artérielle pulmonaire, et à apprécier la tolérance à l’effort chez les patients présumés asymptomatiques.
Dysfonction ventriculaire gauche
La fraction d’éjection ventriculaire gauche doit être calculée par la méthode de Simpson biplan. Elle est fréquemment normale malgré une fuite mitrale volumineuse en raison de conditions de charge favorables, mais elle diminue souvent en postopératoire à cause d’une augmentation de la postcharge. La fraction d’éjection préopératoire est un facteur prédictif important de la fonction ventriculaire gauche postopératoire ainsi que de la survie à long terme. Une fraction d’éjection préopératoire < 60 % augmente le risque de décès et de dysfonction ventriculaire gauche postopératoire et représente une indication opératoire formelle en cas de fuite volumineuse asymptomatique, même si un remplacement valvulaire est nécessaire (indication de classe I selon les recommandations ACC/AHA de 2006 et ESC de 2007).
Une augmentation du diamètre télésystolique du ventricule gauche atteignant 45 mm augmente le risque de dysfonction ventriculaire gauche postopératoire, comme l’a montré Enriquez-Sarano en 1994, et représente également une indication opératoire formelle de classe I en cas de fuite volumineuse asymptomatique, même si un geste conservateur n’est pas réalisable. Cette valeur seuil de 45 mm, qui était celle retenue dans toutes les recommandations jusqu’à la période récente, a été abaissée à 40 mm dans les recommandations ACC/AHA de 2006. Les raisons ayant conduit à cette diminution sont mal définies mais ont pris en compte une étude de Flemming rapportée en 2000, selon laquelle un diamètre télésystolique > 40 mm aurait une spécificité de 100 % pour conclure à une dysfonction contractile du ventricule gauche. La valeur de 45 mm reste cependant celle qui est retenue dans les recommandations ESC de 2007.
Hypertension artérielle pulmonaire
La pression artérielle pulmonaire systolique peut être estimée chez la majorité des patients par l’analyse d’un flux d’insuffisance tricuspide ; cette estimation peut être réalisée au repos et à l’effort. Une hypertension artérielle pulmonaire est retenue en cas de pression artérielle pulmonaire systolique > 50 mmHg au repos, dans toutes les recommandations, et en cas de valeur > 60 mmHg à l’effort dans les recommandations américaines de 2006. Il faut souligner plusieurs points :
- le niveau des pressions artérielles pulmonaires dépend de la compliance de l’oreillette gauche et sera généralement plus important en cas d’insuffisance mitrale aiguë que de fuite chronique ;
- la valeur seuil de 60 mmHg proposée à l’effort dans les recommandations ACC/AHA de 2006 ne repose pas sur des données validées et n’a pas été reprise dans les recommandations ESC de 2007 ;
- enfin, les valeurs observées au repos comme à l’effort doivent toujours tenir compte de l’âge des patients.
La constatation d’une pression artérielle pulmonaire systolique > 50 mmHg au repos chez un patient ayant une fuite mitrale volumineuse asymptomatique sans dysfonction ventriculaire gauche est une indication opératoire admise de classe IIa selon toutes les recommandations actuelles, mais surtout si une plastie est réalisable. L’indication chirurgicale est également admise en cas de pression artérielle pulmonaire systolique > 60 mmHg à l’effort, selon les seules recommandations américaines de 2006.
Tolérance à l’effort
Un échocardiogramme d’effort est indiqué chez les patients ayant une fuite mitrale volumineuse asymptomatique afin d’apprécier la tolérance à l’effort, l’évolution des pressions pulmonaires et de l’IM, et l’existence d’une réserve contractile. Il s’agit d’une indication de classe IIa, selon les recommandations ACC/AHA de 2006. Son intérêt principal est de dépister les patients faussement asymptomatiques, ayant une tolérance à l’effort réduite malgré l’absence de symptômes avérés, et qui pourraient représenter près de 20 % des cas, selon une étude de Messika-Zeitoun de 2006 basée sur la mesure du pic de VO2. Les autres objectifs sont moins bien établis. L’interprétation des pressions pulmonaires à l’effort peut être difficile en raison de la validité discutable du seuil de 60 mmHg actuellement proposé, notamment chez des sujets âgés. Le caractère dynamique de la régurgitation est beaucoup moins bien documenté dans le cas des fuites mitrales organiques que dans celui des fuites ischémiques. Enfin, l’absence de réserve contractile est définie par une augmentation de la fraction d’éjection de moins de 4 % à l’effort, mais cette valeur seuil est proche de la limite de reproductibilité de la méthode, ce qui peut rendre l’interprétation des résultats difficiles.
Faisabilité de la plastie mitrale
Elle est appréciée à partir du mécanisme de la fuite mitrale, de son étiologie, de l’analyse segmentaire de la valve mitrale et du bilan morphologique.
Mécanisme de l’IM
Le mécanisme de l’IM est évalué en se basant sur la classification de Carpentier qui distingue les fuites avec mouvements valvulaires normaux (type I), les prolapsus mitraux (type II) et les IM restrictives (type III). L’appréciation du mécanisme oriente le diagnostic étiologique. Dans le cadre des IM organiques, une fuite de type I peut être secondaire à une endocardite (perforation valvulaire), une fuite de type II est le plus souvent d’origine dégénérative mais peut être due à une endocardite (rupture de cordages d’origine infectieuse) ou à un infarctus myocardique (rupture de pilier), et une fuite de type III oriente principalement vers une cause rhumatismale.
Étiologie de l’insuffisance mitrale
C’est un élément fondamental pour juger de la faisabilité d’une plastie mitrale. Ce sont principalement les fuites mitrales dystrophiques ou dégénératives qui sont accessibles à un geste conservateur. Selon une étude de Monin rapportée en 2005, une plastie mitrale n’était réalisable que chez 29 % des patients ayant une fuite rhumatismale, chez 63 % de ceux ayant une fuite d’origine infectieuse et chez 93 % de ceux ayant une fuite dégénérative. Le diagnostic étiologique repose sur le contexte clinique, le type de Carpentier et l’analyse de la valve mitrale qui montre un prolapsus avec éventuel épaississement « myxoïde » en cas de fuite dégénérative, une restriction avec épaississement et/ou calcifications valvulaires en cas de fuite rhumatismale, et des lésions infectieuses en cas d’endocardite.
Analyse segmentaire
Elle est particulièrement importante en cas de prolapsus car, si la majorité des patients peut bénéficier d’une chirurgie conservatrice, la proportion en est cependant variable selon les lésions en cause. La plastie est réalisable dans 99 % des cas de prolapsus isolé du segment médian de la valve postérieure (P2), dans 80 % des cas d’atteinte des zones commissurales, dans 77 % des cas de prolapsus de la valve mitrale antérieure et dans 60 % des cas de prolapsus bivalvulaire, selon l’étude de Monin rapportée en 2005. Si l’on suit les recommandations ACC/AHA de 2006 qui exigent que la faisabilité de la plastie soit d’au moins 90 % pour opérer une fuite mitrale volumineuse asymptomatique sans dysfonction ventriculaire gauche, l’indication opératoire ne concernera pratiquement que les prolapsus isolés du segment P2.
L’analyse segmentaire de la valve mitrale repose sur l’analyse de quatre incidences clés qui peuvent être obtenues par voie transthoracique ou transœsophagienne :
- coupe apicale 4 cavités stricte (analyse des segments P1, A2, A3) ;
- coupe longitudinale (analyse des segments A2 et P2) ;
- coupe bicommissurale (analyse des segments P1, A2, P3 ainsi que des commissures) ;
- coupe transversale (analyse de tous les segments et des deux commissures) (figures 8 et 9).
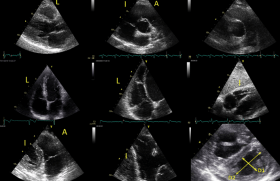
Figure 8. Les 4 incidences clés pour l’analyse segmentaire de la valve mitrale par voie transthoracique : apicale 4 cavités, apicale 3 cavités ou parasternale longitudinale (PSL), bicommissurale (intermédiaire entre les coupes 4 cavités et 2 cavités) et parasternale transversale (PST) (CA : commissure antérieure, CP : commissure postérieure, OG : oreillette gauche, VG : ventricule gauche).
Figure 9. Les 4 incidences clés pour l’analyse segmentaire de la valve mitrale par voie transœsophagienne : 4 cavités, longitudinale vers 120°, bicommissurale habituellement entre 30 et 60°, et transgastrique (CA : commissure antérieure, CP : commissure postérieure, OG : oreillette gauche, VG : ventricule gauche).
Bilan morphologique
L’analyse morphologique de la valve mitrale recherche des éléments qui peuvent contre-indiquer la plastie : calcifications extensives de l’anneau mitral, calcifications valvulaires et/ou sous-valvulaires majeures, lésions infectieuses sévèrement destructrices, « hyper Barlow » (figure 10).
Figure 10. Importante calcification postérieure de l’anneau mitral (flèche).
Appréciation de la faisabilité de la plastie
Au terme de ce bilan, la plastie mitrale peut être considérée comme pratiquement certaine (prolapsus isolé de P2, perforation mitrale isolée), de probabilité intermédiaire (prolapsus de la valve mitrale antérieure, prolapsus commissural, prolapsus bivalvulaire), ou non réalisable (calcification annulaire importante, hyper Barlow, lésions rhumatismales sévères, destructions étendues d’origine infectieuse).
L’échocardiogramme transœsophagien n’est pas indispensable en préopératoire, mais est indiqué quand l’échocardiogramme transthoracique est insuffisant pour quantifier l’IM et apprécier son retentissement ou son mécanisme. L’échocardiogramme transthoracique permet de préciser la faisabilité de la plastie dans 97 % des cas, selon l’étude de Monin de 2005. L’échocardiogramme transœsophagien reste nécessaire en peropératoire pour confirmer le bilan lésionnel et apprécier le résultat de la plastie.
Synthèse et conclusion
Au terme de cette triple évaluation portant sur la quantification de la fuite mitrale, son retentissement et la faisabilité d’une plastie, la prise en charge pourra être orientée à partir d’un algorithme décisionnel basé sur les recommandations les plus récentes (figure 11). Le tableau 2 résume les paramètres indispensables à recueillir en échographie pour appliquer cet algorithme, et le tableau 3 indique les éléments devant figurer dans le compte-rendu de l’échocardiogramme d’une fuite mitrale organique.
Figure 11. Algorithme décisionnel pour la prise en charge d’une IM organique (AC/FA : arythmie complète par fibrillation atriale, DTS : diamètre télésystolique, FE : fraction d’éjection, IM : insuffisance mitrale, PAPS : pression artérielle pulmonaire systolique, SOR : surface d’orifice régurgitant, VG : ventricule gauche).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :