Publié le 13 mar 2007Lecture 8 min
Échographie - Les applications cliniques des nouvelles techniques
K. SERRI, Montréal, Canada et S. LAFITTE, hôpital du Haut-Lévêque, Pessac
Les Journées écho-Doppler cardiovasculaire de Bordeaux
Ces dernières années ont vu l’introduction en pratique de plusieurs nouvelles techniques échographiques permettant une évaluation plus précise et détaillée de la fonction cardiaque. Cette section traitera des plus importantes de ces techniques et de leur contribution à la pratique quotidienne en échographie.
Doppler tissulaire
E. Donal (Rennes) a commencé par traiter de l’évaluation de la fonction myocardique tant globale que régionale car celle-ci constitue un objectif important de l’examen échocardiographique. En raison de sa simplicité, rapidité et grande accessibilité, l’échocardiographie conventionnelle est utilisée de façon quotidienne pour cette évaluation mais reste semi-quantitative. Basé sur l’étude des vélocités myocardiques, le Doppler tissulaire (DTI) ajoute une approche quantitative à l’étude de la fonction cardiaque.
L’utilisation du Doppler tissulaire pulsé à l’anneau mitral fait désormais partie intégrante de l’examen de routine pour l’étude de la fonction diastolique et des pressions de remplissage.
Le DTI couleur et l’analyse posttraitement associée sont d’apparition plus récente et offrent de nouvelles possibilités à l’échographiste. Dans la cardiopathie ischémique, la diminution des vélocités systoliques a été bien démontrée en situation d’ischémie aiguë. Également appliquée à l’échographie de stress, l’étude des vélocités s’est montrée supérieure à la quantification visuelle pour l’évaluation de la fonction régionale. Dans les myocardiopathies, le DTI permet de différencier la myocardiopathie restrictive de la péricardite constrictive, l’hypertrophie physiologique de celle pathologique ainsi que d’identifier la myocardiopathie hypertrophique à un stade infraclinique.
Toutefois, c’est probablement dans le domaine de l’insuffisance cardiaque que le DTI a eu le plus d’impact, permettant une analyse détaillée de l’asynchronisme cardiaque. En effet, il s’agit certainement de la méthode la mieux validée pour l’identification de l’asynchronisme et des répondeurs potentiels à une thérapie de resynchronisation.
Outre l’étude des vélocités, le DTI permet également d’analyser la déformation (strain) et le déplacement tissulaire (tissue tracking). La déformation mesure le pourcentage de raccourcissement des fibres myocardiques en fonction de leur longueur originale. Les principales applications du strain sont la cardiopathie ischémique et l’échographie de stress, où cette technique apporte une meilleure quantification de la fonction régionale. Plus récemment, le strain a été utilisé pour identifier l’asynchronisme ventriculaire gauche. Toutefois, certaines limites inhérentes au Doppler et la complexité de l’analyse ont quelque peu restreint son application dans la pratique quotidienne.
2D-strain
K. Serri (Montréal, Canada) a exposé cette nouvelle méthode de mesure de la déformation basée sur l’imagerie 2D conventionnelle (2D-strain). Traditionnellement dérivée du Doppler tissulaire, l’étude du strain est soumise aux limitations inhérentes à toute modalité Doppler, soit la nécessité d’un angle d’interrogation optimal. La variabilité des mesures et la complexité de l’analyse sont d’autres inconvénients de la méthode Doppler, ayant probablement contribué à une application clinique limitée.
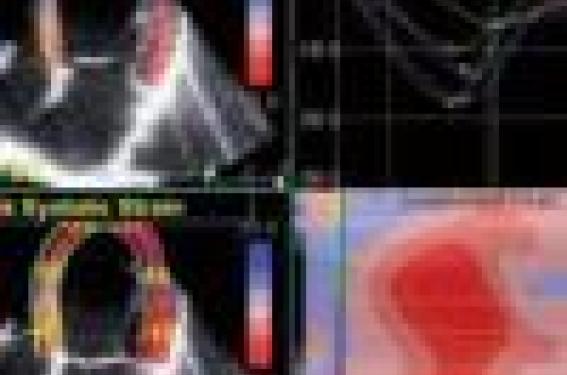
Le 2D-strain se base sur l’identification de marqueurs acoustiques naturels au sein du myocarde : le déplacement de ces marqueurs est suivi image par image au cours du cycle cardiaque, par une technique appelée « speckle tracking », permettant ainsi le calcul des vélocités tissulaires et de la déformation. L’avantage principal de cette méthode vient du fait que les mesures sont indépendantes de l’angle d’interrogation, contrairement aux mesures obtenues par Doppler (figure).
Evaluation des déformations longitudinales en mode « speckle tracking » avec calcul du strain global et régional et visualisation des déformations au cours du temps sous forme de courbe ou de tracé TM.
Le 2D-strain permet l’analyse des trois composantes normales de la déformation dans les axes longitudinal, radial et circonférentiel, tandis que l’analyse par Doppler tissulaire est habituellement restreinte à la composante longitudinale.
La simplicité et la rapidité de cette méthode semi-automatisée en font une technique de choix pour l’analyse de la déformation.
Cette technique a été validée chez l’animal ainsi que chez l’humain en utilisant la microsonométrie et l’imagerie par résonance magnétique. Les résultats obtenus offrent une très bonne corrélation avec les mesures dérivées du Doppler tissulaire ou de la résonance magnétique. En raison de la disponibilité récente des logiciels d’analyse, l’expérience clinique reste encore limitée, mais les nombreux travaux en cours devraient permettre d’établir définitivement cette nouvelle modalité d’analyse de la déformation. Les premières études publiées ont démontré l’intérêt de cette technique chez des patients porteurs de myocardiopathie ischémique, de myocardiopathie hypertrophique, dans l’amylose cardiaque ainsi que dans le domaine de la resynchronisation.
La 2D-strain semble être l’outil idéal pour l’étude de la déformation et pourrait ainsi permettre au strain de devenir un outil clinique accessible à tous au laboratoire d’échographie.
Échographie de contraste
Pour J.-L. Vanoverschelde, (Bruxelles, Belgique), la capacité d’opacifier les cavités cardiaques est connue depuis plusieurs années avec l’opacification du cœur droit à la recherche de shunts à l’étage auriculaire. L’opacification du cœur gauche est longtemps restée impossible en raison du manque de stabilité des microbulles et de leur destruction par les capillaires pulmonaires. Avec l’apparition d’agents de contraste spécifiques constitués de microbulles de gaz de diamètre < 10 µm (leur permettant ainsi de traverser les poumons), l’opacification du cœur gauche devient possible.
Les deux applications principales de l’échographie de contraste sont :
- l’opacification du ventricule gauche (VG),
- l’étude de la perfusion myocardique.
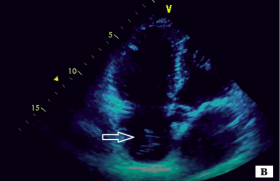
L’opacification du VG permet d’améliorer la détection de l’endocarde en particulier chez les patients peu échogènes (obèses, insuffisants respiratoires, patients de réanimation). L’amélioration de la détection de l’endocarde facilite aussi grandement l’étude des volumes ventriculaires, de la fonction ventriculaire gauche et de la cinétique segmentaire. En échographie de stress, l’utilisation de contraste chez les patients peu échogènes permet une meilleure détection des anomalies de cinétique, avec une qualité d’analyse équivalente à celle de patients échogènes. Plus rarement, le contraste peut être utilisé pour améliorer les signaux Doppler ou pour visualiser des masses intracardiaques (thrombus, tumeurs).
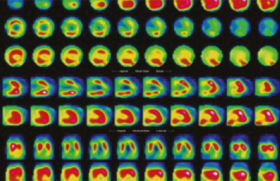
L’échographie de contraste myocardique permet, quant à elle, une étude non invasive de la perfusion. Elle utilise des principes différents de ceux de l’opacification du VG, soit la concentration intramyocardique des microbulles. Après injection intraveineuse, l’étude du transit intramyocardique des microbulles permet d’évaluer le flux sanguin myocardique. Après la destruction des microbulles à l’aide d’ultrasons de haute énergie, on mesurera ensuite (en imagerie à basse énergie) la vitesse à laquelle elles réapparaissent, témoignant ainsi de l’intégrité de la perfusion myocardique. Plusieurs études ont démontré la précision de l’échographie de contraste myocardique dans la détection d’ischémie et de sténoses coronaires, avec des résultats comparables aux méthodes isotopiques.
En France à l’heure actuelle, les agents de contraste sont approuvés pour l’opacification des cavités, mais non pour l’étude de la perfusion myocardique (en dehors du cadre de protocoles de recherche).
Échographie 3D
P. Dehant (Bordeaux) a tout d’abord rappelé que les techniques permettant l’évaluation 3D de structures cardiaques ont connu un grand développement au cours des dernières années. Les premiers systèmes basés sur la reconstruction d’images obtenues en 2D étaient limités par le temps d’analyse posttraitement. Plus récemment, les avancées technologiques ont permis le développement du 3D temps réel, soit l’acquisition d’informations volumétriques en temps réel par balayage d’un volume en un seul cycle cardiaque.
Déjà validés en mode 3D « reconstruit », les calculs de volumes de la masse et de la fraction d’éjection ventriculaire gauche ont plus récemment été validés en 3D temps réel. Pour l’étude de la fraction d’éjection ventriculaire gauche, la méthode 3D s’avère supérieure au 2D conventionnel. L’étude des volumes en 3D démontre également une excellente corrélation avec ceux obtenus en imagerie par résonance magnétique.
De nombreux travaux ont aussi démontré l’utilité du 3D pour l’analyse de la valve mitrale. Dans la sténose mitrale, la méthode permet une excellente évaluation de l’orifice sténosé, de la morphologie de la valve, facilitant ainsi la sélection des candidats à une valvuloplastie percutanée. Dans l’insuffisance mitrale, l’analyse morphologique détaillée peut simuler la vue chirurgicale, pouvant aider le chirurgien dans la préparation de l’intervention. Dans les cardiopathies congénitales, l’utilité du 3D réside surtout dans une meilleure visualisation des différents défects anatomiques, telles les communications interauriculaire et interventriculaire.
Plus récemment, l’échographie 3D a été appliquée à l’étude de l’asynchronisme intraventriculaire gauche et à la sélection des candidats à une resynchronisation. Basés sur l’étude des volumes régionaux et la dispersion temporelle de ces volumes, les résultats préliminaires laissent entrevoir un rôle prometteur pour l’échographie 3D en resynchronisation.
L’échographie 3D n’est pas encore d’utilisation routinière. Toutefois, le développement du 3D temps réel, l’amélioration de la qualité d’images et la simplification des logiciels d’exploitation devraient permettre un usage croissant de cette technologie.
Échographie intracardiaque
L’échographie intracardiaque, traitée par E. Brochet (Paris), a vu son intérêt croître ces dernières années avec le développement de nouvelles sondes. Avec l’apparition de sondes avec imagerie à basse fréquence, la technique permet d’avoir non seulement une excellente résolution mais aussi une meilleure pénétration tissulaire.
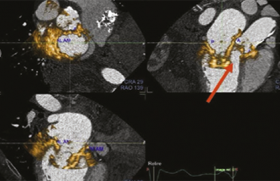
Le principe de l’échographie intracardiaque est simple : un cathéter souple muni d’une sonde échographique (cathéter ACUNAV) est introduit par voie veineuse fémorale et monté dans l’oreillette droite sous guidage fluoroscopique. Le cathéter ainsi en place permet une excellente visualisation des structures cardiaques, en particulier du septum interauriculaire, de l’oreillette gauche et des veines pulmonaires. La proximité de ces structures permet d’obtenir une imagerie de haute résolution.
En pratique, l’échographie intracardiaque est utilisée en salle de cathétérisme pour guider les procédures interventionnelles, en particulier la fermeture de communications interauriculaires ou de foramen ovales perméables, le cathétérisme transseptal et les valvuloplasties percutanées. L’échographie transœsophagienne est la technique traditionnellement utilisée, avec l’inconvénient d’avoir à procéder à une anesthésie générale. L’expérience clinique actuelle a permis de valider le rôle de l’échographie intracardiaque dans la fermeture des communications interauriculaires et des foramen ovales perméables. Dans certains centres, c’est devenu la technique de choix pour ces procédures avec comme avantage principal de pouvoir éviter une anesthésie générale.
Le guidage du cathétérisme transseptal est une autre application clinique de l’échographie intracardiaque, lors d’interventions valvulaires du cœur gauche ou lors de procédures électrophysiologiques. La technique permet une visualisation optimale du septum interauriculaire et de la fosse ovale, sécurisant ainsi la ponction.
D’autres indications potentielles sont l’étude de l’auricule gauche à la recherche de thrombus, et plus rarement le guidage de biopsie de tumeurs intracardiaques, ainsi que la surveillance de valvuloplasties percutanées ou de mise en place de valves percutanées.
La technique semble être sécuritaire sans évidence de complications significatives liées à l’utilisation de ces cathéters, autres que les hématomes au site de ponction et quelques arythmies atriales. L’inconvénient principal reste le coût élevé du cathéter qui est à usage unique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :