Études
Publié le 01 fév 2023Lecture 3 min
Focus sur l’étude OCEAN(a)-DOSE - Évaluation de l’intérêt d’une réduction de la lipoprotéine(a) par un ARN interférent (olpasiran)
Théo PEZEL, CHU Lariboisière, APHP (Paris)
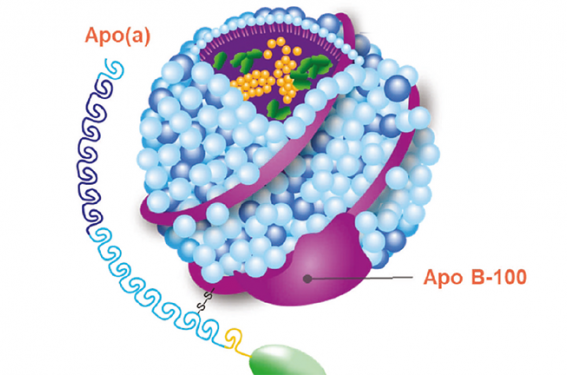
Plusieurs études ont bien démontré que des niveaux élevés de lipoprotéine(a) [Lp(a)] sont une cause importante de maladie coronaire et d’autres formes de maladie cardiovasculaire d’athérosclérose (figure 1). En effet, des niveaux élevés de Lp(a) sont l’anomalie lipoprotéique la plus courante chez les hommes atteints de maladie coronaire avant l’âge de 50 ans et les femmes avant l’âge de 60 ans. Environ 20 % des personnes atteintes de maladie cardiovasculaire d’athérosclérose ont des niveaux élevés de Lp(a). Cependant, il n’existe actuellement pas de thérapies approuvées pour abaisser spécifiquement la Lp(a). En effet, le taux de Lp(a) ne change pas avec les statines et n’est pas affecté par l’ézétimibe.
Il est intéressant de noter que la Lp(a) peut diminuer chez certains patients traités avec un inhibiteur de PCSK9. De plus, il existe des données montrant que les patients qui ont connu une réduction de la Lp(a) avec le cholestérol LDL ont bénéficié davantage du traitement par l’inhibiteur de PCSK9. À noter que les inhibiteurs de PCKS9 peuvent réduire la Lp(a) d’environ 25 à 35 %.
Ainsi, l’objectif de cette étude de phase II était d’évaluer l’intérêt d’une réduction de la lipoprotéine(a) par un ARN interférent, l’olpasiran.
Objectif de l’étude
L’objectif de cette étude de phase II était d’évaluer l’efficacité d’un ARN interférent, l’olpasiran, sur la réduction de la Lp(a) chez des patients en prévention secondaire avec maladie cardiovasculaire d’athérosclérose connue et des taux élevés de Lp(a).
Les mécanismes pharmacologiques impliqués dans le fonctionnement de l’olpasiran (ARN interférent) sont détaillés dans la figure 2.
Les mécanismes d’action impliqués sont : i) petit ARN interférent dirigé vers le foie ; ii) puis, le brin antisens est chargé dans un complexe d’annulation induit par l’ARN (RISC) dans l’hépatocyte ; iii) enfin, le complexe se lie à l’ARNm de l’apo(a), entraînant sa dégradation et empêchant la traduction de la protéine.
Matériel et méthodes
Cette étude randomisée a réparti les patients pour recevoir soit un placebo, soit l’une des quatre doses d’olpasiran : 10 mg, 75 mg ou 225 toutes les 12 semaines ou 225 mg toutes les 24 semaines. Le design complet de l’étude est présent dans la figure 3.
Population
La population étudiée dans cet essai était constituée de patients en prévention secondaire avec une maladie athéromateuse connue et un taux de Lp(a) élevé > 150 nmol/L.
Critères de jugement
Le critère de jugement principal était la réduction du taux de Lp(a). Les critères de jugement secondaires étaient la réduction du LDL-C et de l’apolipoprotéine B (apoB).
Résultats
Au total, 281 patients randomisés (âge moyen 61,9 ans ; 32,0 % de femmes) avec au départ une concentration médiane de Lp(a) de 260,3 nmol/L et un taux médian de LDL-C était de 67,5 mg/dL. Les patients de l’essai ont été bien traités par un traitement médical, 88 % d’entre eux prenant des statines, dont 61 % prenant des statines à haute intensité. Plus de la moitié prenaient de l’ézétimibe et 23 % prenaient un inhibiteur de PCSK9.
Les principaux résultats de l’essai montraient que (figure 4) :
• Dans le groupe placebo : les taux de Lp(a) ont augmenté de 3,6 % après 36 semaines.
• Dans les groupes olpasiran :
– pour les patients traités par olpasiran 10 mg, 75 mg et 225 mg administrés toutes les 12 semaines, les réductions en pourcentage ajustées au placebo des concentrations de Lp(a) étaient de 70,5 %, 97,4 % et 101,1 %, respectivement ;
– pour ceux qui prenaient la dose de 225 mg toutes les 24 semaines, le pourcentage de réduction ajusté au placebo par rapport au départ était de 100 % ;
– parmi ceux ayant reçu la dose de 10 mg toutes les 12 semaines, 66,7 % ont atteint une concentration de Lp(a) < 125 nmol/L ;
– aux doses de 75 mg et 225 mg toutes les 12 semaines, 100 % sont passés en dessous de ce seuil ;
– à la dose de 225 mg administrée toutes les 24 semaines, 98,1 % ont atteint une concentration de Lp(a) < 125 nmol/L.
Il y avait également des réductions significatives du LDL-C et de l’apoB (figure 5). Pour les doses de 10 mg, 75 mg, 225 mg et 225 mg (Q24W), les réductions en pourcentage ajustées au placebo étaient de 23,7 %, 22,6 %, 23,1 % et 24,8 %. Avec l’apoB, les baisses ajustées au placebo étaient de 18,9 %, 16,7 %, 17,6 % et 18,8 %, respectivement. Enfin, la tolérance était bonne avec des réactions au site d’injection et des réactions d’hypersensibilité associées plus fréquemment à la prise d’olpasiran (tableau 1). Ceux-ci ont été décrits comme étant de gravité légère et de résolution spontanée sans traitement.
Figure 5. Résultats secondaires de l’efficacité de l’olpasiran sur la réduction du cholestérol LDL et de l’apolipoprotéine B.
En direct du congrès de l’AHA 2022 à Chicago d’après la présentation de Michelle O’Donoghue (Brigham and Women’s Hospital, Boston, MA) : « Ocean(a)-DOSE Trial: primary results »
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :