Publié le 01 nov 2019Lecture 7 min
L’imagerie à l’ESC : pour un usage raisonné
Erwan DONAL, CHU de Rennes

L’imagerie était présente et est finalement incontournable dans les différents villages du congrès, c’est-à-dire dans les différentes surspécialités de la cardiologie. Il est donc nécessaire de faire des choix et nécessaire de concentrer cet article sur certaines thématiques. À noter que ce congrès de l’ESC était particulier par l’importance prise par le « digital health care » avec un village dédié et des lectures dispensées sur cette thématique. Elle implique énormément l’imagerie et son usage d’aujourd’hui et de demain.
Avant cela, nous pouvons juste insister sur le fait que cette imagerie multimodale justifie une expertise pour en permettre un usage raisonné en pratique clinique. Tout type d’image n’est pas recommandé pour tout patient. Le cardiologue imageur doit apprendre à exploiter la bonne technique pour le bon patient et ainsi aider au mieux au choix, à la réalisation et au suivi du meilleur traitement pour un patient donné. L’imagerie est de fait, au centre du processus de médecine personnalisée et pour ce faire elle s’appuiera de plus en plus sur les atouts de certaines formes d’intelligence artificielle et les traitements statistiques qui s’y associent. UN seul exemple pour illustrer cette importance du « machine learning » : les images contiennent des quantités d’informations que l’être humain n’est pas en mesure d’intégrer ou de mesurer. La machine, elle, peut mesurer tout un tas de choses automatiquement ; elle peut reconnaître des structures automatiquement (radiomics) et elle peut définir sur la base de milliers de paramètres d’imagerie (auxquels il est possible d’associer des données cliniques ou biologiques) des phénotypes de patients auxquels il est possible d’associer un pronostic et une éventuelle probabilité de réponse à telle ou telle stratégie thérapeutique.
Tout cela devrait changer nos conceptions du traitement, même si bien entendu, l’ordinateur ne remplace pas l’expérience de l’expert qui au final prend la décision du traitement.
C’est une aide, une assistance à la prise de décision, mais qui va rapidement impacter nos pratiques comme les scores se sont imposés dans nombre de situations cliniques.
Une situation clinique : l’insuffisance cardiaque à fraction d’éjection préservée
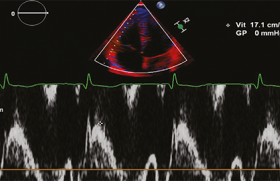
Il a été proposé après des mois de gestation, un nouvel algorithme européen pour permettre un diagnostic plus précis des patients supposés avoir une insuffisance cardiaque à fraction d’éjection préservée. Cet algorithme propose un score qui peut ne justifier que la clinique et l’échocardiographie de repos, mais ce score peut en cas de doute justifier la pratique d’un « diastolic stress test », c’est-à-dire une échocardiographie d’effort mené à un palier faible, mais permettant de surveiller les changements de vitesse maximale de la fuite tricuspide et les changements de E/e’ et e’ lors de l’effort (figures 1 et 2 : éléments du score HFA-PEFF avec les données de l’échocardiographie de repos [figure 1] et les données du diastolic stress test [figure 2]).
Figure 1. Score de l’insuffisance cardiaque à fraction d’éjection préservée (HpEF).
Figure 2. Algorithme HFpFE.
Le score HFA-PEFF ≥ 5 définit l’insuffisance cardiaque à fraction d’éjection préservée. Entre 2 et 4 points sur l’échocardiographie de repos, il faut pratiquer le « diastolic stress test ».
Ce score est nouveau, il n’intègre pas les différents phénotypes d’insuffisance cardiaque à fraction d’éjection préservée. Il en existe pourtant plusieurs. Parmi ceux-là, il y a des patients pour lesquels il faut particulièrement regarder, quantifier la fonction atriale (plusieurs travaux présentés sur le strain atrial comme un marqueur pronostique indépendant et comme un marqueur puissant de prédiction de l’augmentation des pressions de remplissage).
Il y a aussi des patients où c’est le coeur droit : ce cœur droit s’altère « trop » rapidement face à l’augmentation des pressions pulmonaires. La fuite tricuspide apparaît et il est possible que cette fuite tricuspide devienne une cible thérapeutique. Les collègues allemands ont, en effet, montré que l’usage du MitraClip en position tricuspide semblerait capable d’améliorer le pronostic des patients insuffisants cardiaques ayant une fuite tricuspide sévère. Il s’agissait cependant, et il faut être prudent, que d’études observationnelles de patients de registre et comparer la morbimortalité attendue chez ce type de patients (utilisation de score de propensité).
L’imagerie de la fuite tricuspide progresse et elle doit s’adapter aux nouvelles thérapeutiques tel le clip.
Des exemples d’images échocardiographiques de valve tricuspide dans l’optique du traitement percutané sont représentés dans la figure 3.
Figure 3. Exemples d’images échocardiographiques de valve tricuspide dans l’optique du traitement percutané. P : feuillet postérieur, A : feuillet antérieur ; S : feuillet septal
La sténose aortique
Il existe différents phénotypes avec les plus récents qui sont d’évaluation difficile et pour lesquels les prises en charge sont encore mal codifiées.
Rappelons, l’étude randomisée ROTAS étudiant les calcifications au scanner, la fibrose en IRM et les différents marqueurs échocardiographiques pour bien caractériser les rétrécissements valvulaires aortiques à bas gradient et à fraction d’éjection préservée. Une fois ces patients souffrant de cette forme particulière de rétrécissement valvulaire aortique correctement caractérisés, ils sont randomisés : traitement et suivi médical strict versus TAVI. L’idée est de savoir si le traitement de la valvulopathie est indispensable pour améliorer le pronostic vital et fonctionnel de ces patients souvent polypathologiques (investigatrice principale : Elena GALLI, CHU de Rennes). L’ESC a été l’occasion dans ce cadre de proposer et de discuter la place des examens suscités.
A été proposée une nouvelle classification pronostique des rétrécissements valvulaires aortiques (figure 4).
Figure 4. Méthodes : classification des étapes de l’altération VG.
Le pronostic du rétrécissement valvulaire aortique est démontré chez les patients asymptomatiques comme chez les patients symptomatiques comme d’autant plus mauvais que l’on passe du stage 0 au stage 4. Tout cela concourt à proposer et à tester de plus en plus des approches basées sur l’imagerie pour envisager des prises en charge plus précoces des rétrécissements valvulaires aortiques. Nous connaissons les résultats flatteurs du TAVI chez les patients à moindre risque que ceux testés initialement. L’idée de proposer un traitement sur la simple base d’un strain longitudinal ou de la présence de fibrose interstitielle (T1 mapping et/ou calcul du volume extracellulaire) est proposée par certains. La fibrose interstitielle est supposée réversible après traitement de l’obstacle aortique, il n’en est pas de même pour la fibrose de remplacement (cicatrice analysée par la prise de gadolinium tardif). Il semble donc séduisant pour réduire le risque de persistance de symptômes après le remplacement valvulaire aortique, de ne pas attendre ces lésions cicatricielles. Ces idées se font jour, mais aucune démonstration claire et aucune recommandation n’existe encore !
L’imagerie multimodalité est fondamentale pour le myocarde du ventricule gauche, pour la planification de l’implantation de la valve, mais aussi pour l’analyse du ventricule droit des patients porteurs d’un rétrécissement valvulaire aortique.
La dysfonction ventriculaire droite doit être bien caractérisée avant de proposer un remplacement valvulaire aortique, car cette dysfonction est un marqueur pronostique puissant.
L’homme et la femme ne sont pas égaux, c’est un problème aussi vis-à-vis du rétrécissement valvulaire aortique. Les hommes ont deux fois plus de bicuspidie valvulaire aortique. Les femmes ont une moindre calcification des valves, mais une plus importante fibrose de remplacement et un plus grand volume extracellulaire (fibrose interstitielle) que les hommes lorsqu’elles sont évaluées en IRM avant un remplacement valvulaire aortique. Elles semblent avoir une plus grande sensibilité à l’augmentation de la post-charge. Enfin, chez l’homme comme chez la femme, l’importance de ce remodelage et la présence de fibrose de remplacement sont rapportées, avec l’âge, comme deux facteurs pronostiques indépendants et en particulier du genre.
Nous pouvons tout de même retenir que la pathophysiologie du rétrécissement valvulaire aortique n’est pas strictement identique chez l’homme et la femme.
Le remplacement valvulaire aortique devra peut-être plus précoce chez la femme ? il faut attendre des études prospectives.
De la même manière, des travaux convergents laissent penser qu’il faudra réévaluer les indications de traitement des régurgitations aortiques. Ce sont des valvulopathies plus rares, mais les indications de classe I (apparitions de symptômes) semblent avoir un pronostic plus péjoratif une fois traité que les indications portées sur la dimension des cavités cardiaques.
Actuellement les recommandations internationales sont :
1) symptômes (indication de classe I) ;
2) éjection fraction du ventricule gauche < 50 % (classe I) ;
3) chirurgie pour anévrisme de l’aorte ascendante (classe I) ;
4) diamètre télésystolique indexé du ventricule gauche > 25 mm/ m2 (classe IIa) ;
5) diamètre télésystolique du ventricule gauche > 50 mm (classe IIa) ;
6) diamètre télédiastolique du ventricule gauche (LVEDD) > 65 mm (classe IIb).
Dans les travaux récents qui sont rétrospectifs et mono-centriques, il semble que le diamètre télé-systolique indexé du ventricule gauche est fondamental et qu’il faille s’inquiéter plus tôt : dès 20 mm/m2. Le strain du ventricule gauche (seuil à -19 %) est aussi proposé comme un bon marqueur du remodelage ventricule gauche qui doit conduire à proposer une chirurgie pour assurer un pronostic meilleur en postopératoire et un moindre risque d’événements cardiovasculaires (figure 5).
Figure 5. Exemple d’un patient ayant une bicuspidie avec une fuite aortique très excentrée sur prolapsus de cuspe (L-R) avec diamètre télésystolique du ventricule gauche de 33 mm/m2 et dysfonction ventriculaire gauche (FEVG 53 % et strain longitudinal global -14,3 %) ; patient asymptomatique mais indication chirurgicale retenue sur les diamètres télésystoliques (classe IIa).
Il y aurait beaucoup plus à développer dans le domaine de la prédiction du risque rythmique par l’imagerie, dans le domaine de la resynchronisation ou de la caractérisation des cardiomyopathies. Suite au prochain épisode !
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :