Publié le 01 nov 2017Lecture 6 min
Découverte d’un souffle chez un jeune adulte de 17 ans avec malaise
Gaspard SUC, Inès CAZAUBIEL, Centre hospitalier intercommunal de Villeneuve-Saint-Georges
Nous rapportons le cas d’un patient de 17 ans, admis aux urgences pour malaise sans perte de connaissance. L’échocardiographie réalisée devant la découverte d’un souffle systolique aortique met en évidence une membrane sous-aortique avec obstruction de la chambre de chasse du ventricule gauche et une hypertrophie ventriculaire gauche importante.
Monsieur S. est un patient de 17 ans, d’origine malienne, arrivé en France quelques mois auparavant. Il n’a jamais consulté de médecin. Il a comme antécédents une drépanocytose hétérozygote et des migraines à l’école. Sa mère le décrit comme taciturne et dit qu’il refuse de jouer avec ses cousins.
Le patient décrit au cours d’un repas un épisode de douleur médiothoracique, constrictive, d’environ 30 minutes, associée à une sensation de lipothymie sans perte de connaissance et sans prodromes. Il consulte aux urgences pédiatriques. L’examen clinique met en évidence un souffle systolique 3/6, crescendo, méso-systolique, au foyer aortique, irradiant aux carotides. Le patient ne présente pas de signe d’insuffisance cardiaque. L’ECG inscrit un rythme sinusal à 100/min, avec une HVG électrique à 50 mm, avec des troubles de la repolarisation en rapport. Le bilan biologique retrouve une troponine à 100 ng/l, et un NT-proBNP normal.
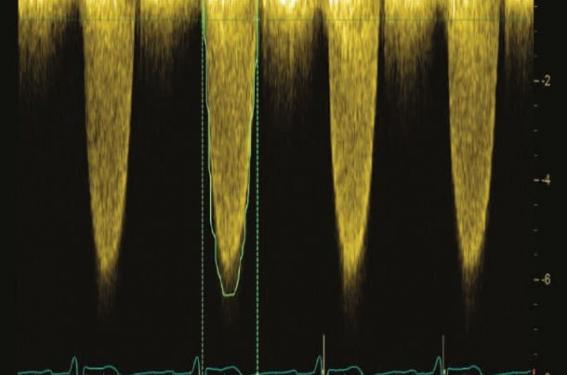
L’échocardiographie réalisée met en évidence une HVG concentrique à 15-16 mm, une FEVG conservée, une membrane sous-aortique avec obstruction, Gmoyen à 100 mmHg et Vmax à 6,1 m/s.
La fuite aortique semble modérée, avec insuffisance mitrale de bas grade. Le reste de l’examen ne met pas en évidence de shunt atrial ou ventriculaire, pas d’autre obstacle de la voie gauche. La PAPS est évaluée à 25 + 5 = 30 mmHg. VD fin. Péricarde sec.
Le patient est ensuite transféré dans un centre spécialisé pour prise en charge. Un angioscanner thoracique réalisé met en évidence une anomalie de naissance de la coronaire droite qui naît en suprasinusal, en regard de l’anneau pulmonaire (entre l’aorte et l’artère pulmonaire) avec un trajet intramural dans sa portion initiale ainsi qu’une fente mitrale.
Le patient est opéré et bénéficie d’une résection de la membrane sous-aortique, une plastie aortique avec réimplantation de la coronaire droite.
Le contrôle échographique postopératoire ne met pas en évidence d’épanchement péricardique, de trouble de la cinétique, une résection complète de la membrane sous-aortique, avec une fuite aortique modérée à moyenne résiduelle sur plastie aortique, respectée dans un premier temps.
Le patient sort d’hospitalisation 3 semaines plus tard sous aspirine 75 mg et bisoprolol 2,5 mg/j.
Les membranes sous-aortiques
Elles représentent 8 à 20 % des causes d’obstruction de la chambre de chasse du ventricule gauche chez l’enfant. Elles sont associées dans un quart des cas à d’autres malformations cardiaques (communication interventriculaire, persistance du canal artériel coarctation de l’aorte, sténose valvulaire aortique, malformation de la valvule mitrale et de l’appareil sous-valvulaire mitral, cardiomyopathie hypertrophique obstructive). La physiopathologie de cette lésion serait une anomalie d’écoulement du sang au niveau de la chambre de chasse du ventricule gauche, qui favoriserait la fibrose par atteinte endothéliale chronique.
On en distingue 3 types :
– la sténose membraneuse, forme la plus fréquente, située à moins de 1 cm de l’orifice valvulaire elle s’insère entre le septum interventriculaire et la grande valve mitrale ;
– la sténose fibreuse, qui correspond à un bourrelet fibreux plus épais et plus étendu en hauteur que la membrane ;
– la sténose diffuse, qui correspond à une masse polypoïde irrégulière, parfois à type de chenal fibreux (sténose en tunnel).
L’interrogatoire recherche des signes d’insuffisance cardiaque, de syncopes qui sont très rares (10 % des cas). L’examen clinique recherche un souffle systolique maximal à la base. Le souffle est d’autant plus intense que la sténose est serrée. Un souffle d’insuffisance aortique peut s’y associer. Ce souffle s’associe généralement à un thrill au niveau de la fourchette sternale.
Le bilan paraclinique consiste en :
– une radiographie thoracique : souvent normale, sauf chez le nourrisson où la cardiomégalie est habituelle ;
– un ECG : recherche d’une hypertrophie ventriculaire gauche, de troubles de la repolarisation (seulement dans 10 % des cas) ;
– une épreuve d’effort : afin de dépister les faux asymptomatiques. Un Holter ECG des 24 h, permet chez l’enfant de rechercher des signes d’ischémie lors des mouvements de grande activité physique ;
– un angio-TDM ou angio-IRM : afin de confirmer le degré de sténose par planimétrie, de rechercher des anomalies aortiques ou coronaires.
L’échocardiographie a trois objectifs, elle confirme le diagnostic positif et la topographie, apprécie la sévérité et le retentissement sur le ventricule gauche, et recherche des anomalies associées.
On recherche des anomalies d’insertion de la valve mitrale, des anomalies des piliers et des cordages. Le Doppler pulsé affirme le siège sous-valvulaire de la sténose, en montrant une accélération du flux sous les valves aortiques. Le retentissement s’apprécie en recherchant une dilatation (surtout chez le nourrisson), et une hypertrophie (chez le grand enfant). La sévérité de la sténose est appréciée par le gradient maximal, gradient moyen en Doppler continu. On recherche enfin des anomalies associées (coarctation de l’aorte, communication interventriculaire, persistance du canal artériel, anomalies mitrales ou supramitrales, obstacle à l’éjection du ventricule droit).
Indication chirurgicale
(tableau)
Prise en charge
Le risque sans opération est celui d’une altération progressive des sigmoïdes aortiques, l’apparition progressive d’une insuffisance aortique. L’intervention évite la progression des lésions.
L’intervention consiste à une résection de la membrane sous circulation extracorporelle par aortotomie et voie transvalvulaire sans léser la valve mitrale sur laquelle s’insèrent le diaphragme et le bourrelet fibreux sous-valvulaire.
La résection de la membrane peut être associée à l’intervention de ROSS s’il existe une insuffisance aortique importante.
Cette opération consiste à remplacer la valve aortique pathologique en utilisant la propre valve pulmonaire du patient (autogreffe pulmonaire). L’intervention de Ross permet d’éviter la prise d’anticoagulants et autorise la croissance de la valvule.
Les obstructions sous-valvulaires en tunnel justifient une intervention de Konno (aorto-ventriculoplastie par résection de la valve aortique et ouverture de la racine aortique au niveau de la commissure coronaire droite gauche, prolongée du septum interventriculaire).
Les complications sans chirurgie sont l’apparition d’une insuffisance cardiaque, la mort subite (2 à 6 % par an), une augmentation du gradient transvalvulaire, des troubles du rythme cardiaque, calcifications aortiques, ou bien une endocardite infectieuse (dans 14 % des cas, principalement sur la valve aortique plutôt que sur la membrane sous-aortique).
L’apparition d’un syndrome d’effort, de troubles de la repolarisation au repos, le développement d’une cardiomégalie sont des éléments de détérioration de la fonction systolique ventriculaire gauche chez les patients suivis au long cours pour une membrane sous-aortique connue.
Figure 1. HVG mesurée en parasternal grand axe, visualisation de la membrane sous-aortique.
Figure 2. HVG importante mesurée en parasternal grand axe mode TM.
Figure 3. Hypertrophie ventriculaire gauche concentrique confirmée en parasternal petit axe, en diastole.
Figure 4. Coupe parasternale grand axe, zoom sur la chambre de chasse du ventricule gauche, visualisation d’un obstacle sous aortique à type de membrane.
Figure 5. Coupe apicale 5 cavités avec zoom sur la chambre de chasse du ventricule gauche. Membrane sous-aortique visualisée.
Figure 6. Doppler continu au niveau de la membrane sous-aortique, obstruction avec gradient moyen à 100 mmHg.
En pratique
Cause non négligeable d’obstruction de la chambre de chasse du ventricule gauche chez l’enfant et l’adulte.
L’échographie confirme le diagnostic, sa sévérité et recherche des anomalies congénitales souvent associées (CIV, coarctation de l’aorte, etc.).
Indication opératoire chez le patient symptomatique, ou en cas de gradient moyen > 50 mmHg ou d’insuffisance aortique.
Résection chirurgicale de la membrane sous-aortique sous circulation extracorporelle.
Récidive postopératoire chez 24 % des patients d’où la nécessité d’une surveillance au long cours.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :