Technologies
Publié le 20 déc 2019Lecture 9 min
MIDAS : moins de 10 % de pacemakers après implantation d’une CoreValve™ ? Avec la golden touch, c’est possible !
G. BONNET, Benjamin SEGUY, Lionel LEROUX, Unité médico-chirurgicale des valvulopathies, CHU de Bordeaux, Pessac
Variable d’une équipe à l’autre, le taux d’implantation de pacemakers après un TAVI CoreValve™ (Medtronic) reste élevé. Il est par exemple de 17,4 % dans l’étude Low Risk(1). L’existence d’un bloc de branche droit, la profondeur d’implantation et l’utilisation d’une CoreValve™ de 34 mm, sont des facteurs prédictifs reconnus de la survenue de troubles de la conduction. Il est pourtant possible dès aujourd’hui de réduire drastiquement ces troubles et ce sans compromis sur la sécurité des patients. C’est ce que nous montre l’étude MIDAS où les auteurs ont tenu compte de la longueur du septum membraneux.
Anatomie et historique
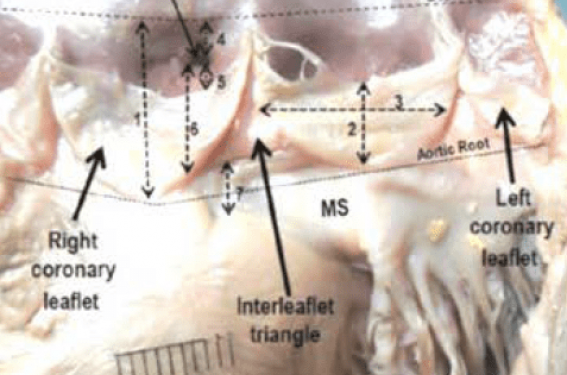
Le septum membraneux (MS) est cette fine partie supérieure du septum interventriculaire située entre l’anneau aortique au-dessus et le septum musculaire en dessous. Il prend naissance entre les feuillets coronaire droit (CD) et non coronaire (NC), et descend dans la chambre de chasse du ventricule gauche (VG) pour rejoindre le septum musculaire. C’est à la base de cette structure anatomique que les voies de conductions font surface dans le VG (figure 1).
Figure 1. Le septum membraneux. A : Vue anatomique du septum membraneux (MS). Il prend naissance en haut entre les feuillets coronaire droit et non coronaire et se termine en bas au niveau du septum musculaire. B : Schéma des voies de conduction faisant surface dans le ventricule gauche (VG) à la base du septum membraneux. C : Coupe histologique passant par la ligne noire de l’image B. Les fibres conductrices sont très superficielles au niveau septum musculaire dans le VG.
Dès 2015, A. Hamdan et al.(2) montrent une relation inverse entre la longueur du MS et la nécessité d’implanter un pacemaker (PM) sur une série de 90 patients ayant reçu une Core-Valve™. Cette publication est très importante car elle révèle plusieurs données fondamentales. Tout d’abord elle nous oblige à nous intéresser à l’anatomie des voies de conduction et du septum interventriculaire. Ensuite, elle nous apprend que la longueur du MS peut se mesurer au scanner et surtout qu’elle est différente d’un individu à l’autre. Enfin, les auteurs remarquent que la présence de calcifications dans cette zone participe à accroître le risque de troubles de la conduction. Dans ce premier papier, le MS est mesuré simplement mais cela est déjà suffisant pour mettre en évidence les grandes variations interindividuelles et introduire le concept du ΔMSID (membranous septum-implantation depth). En effet, le risque de nécessiter un PM en post-TAVI est étroitement relié à la différence entre la longueur du MS et la profondeur d’implantation finale de la valve. Ce ΔMSID est positif quand la valve est déployée au-dessus du septum musculaire et négatif dans le cas contraire. Dans cette étude, le taux d’implantation est de 0 % si le ΔMSID est ≥ 2 mm, de 22 % pour un ΔMSID compris entre +2 et -1 et de 47 % si le chevauchement de la valve sur le septum musculaire est de plus de 1 mm. En 2017, Y. Maeno et al.(3) retrouvent sensiblement les mêmes notions sur une cohorte de 240 patients traités avec une valve balloon expandable. L’année suivante, G. Rocatello et al.(4) montrent l’importance de la force de pression exercée par la CoreValve™ sur les premiers mm du septum musculaire. Enfin, plus récemment, J. T. Tretter et al.(5) proposent de standardiser la mesure du septum membraneux qui devient la distance séparant l’anneau virtuel du haut du septum musculaire.
2019 : l'étude MIDAS
La publication de H. Jilaihawi(6) de cette année, constitue certainement une petite révolution pour les utilisateurs de la CoreValve™. Ce papier contient en réalité deux études.
La première est rétrospective et porte sur 248 patients implantés avec une CoreValve™ (figure 2). Les auteurs ont réparti les malades en 3 groupes. Le groupe le plus à risque de troubles de la conduction comprend les patients porteurs d’un ou plusieurs des critères suivants : BBD, utilisation d’une CoreValve™ 34 mm (C34) et MS < 2 mm. Le groupe à risque intermédiaire a une mesure du MS entre 2 et 5 mm alors que celle du groupe des patients les moins à risque est > 5 mm. Si on exclut les patients BBD ou C34 et que l’on ne considère que le ΔMSID, seulement 2 PM sont implantés chez les 114 malades pour lesquels le ΔMSID est positif, soit 1,7 %. Dans le cas contraire, ce taux passe à 15,5 %.
Figure 2. MIDAS : l’étude rétrospective. L’impact du positionnement de la CoreValve™ par rapport à la longueur du septum membraneux sur le risque d’implantation d’un pacemaker. MS : septum membraneux ; PPMI : implantation définitive d’un pacemaker ; RBBB : bloc de branche droit ; TAVR : remplacement valvulaire percutané. (d’après Jilaihawi et al.(6)).
La deuxième partie de l’étude est prospective, elle concerne 100 patients ayant reçu une Core-Valve™ et montre pour la première fois qu’un déploiement dont la hauteur est adaptée à chaque patient, en ayant en tête la mesure du MS, permet de réduire de manière très significative le risque d’implantation d’un PM (MIDAS : minimizing depth according to the membranous septum). Le taux d’implantation, déjà très bas dans l’étude rétrospective (9,7 % au total), est alors réduit à seulement 3 % dans la partie prospective ce qui n’avait encore jamais été fait avec cette bioprothèse ! Si on regarde plus en détail, on voit que le simple fait d’avoir en tête la mesure du MS avec pour préoccupation de déployer la valve au-dessus du septum musculaire, entraîne une augmentation, de 55 à 80 %, du pourcentage de patients pour lesquels le ΔMSID est positif. L’apparition d’un BBG décroît alors fortement de 25,8 à 9 % et le taux de PM de 9,7 à 3 %. La diminution moyenne de profondeur d’implantation n’est quant à elle finalement que de 1 mm, passant de 3,3 à 2,3 mm (figure 3). Cela confirme le fait que c’est en adaptant à chaque patient la hauteur d’implantation, et non pas en essayant de mettre la valve « au plus haut chez tout le monde », que se fait la différence. Car si on devait en tirer la conclusion simpliste que « plus la valve est haute, mieux c’est », alors, nous aurions immanquablement affaire à un taux plus élevé de pop-up de la valve (migration aortique), or il n’en n’est rapporté aucun dans MIDAS.
Figure 3. Comparaison des deux cohortes rétrospectives et prospectives (d’après Jilaihawi et al.(6)).
Qu'en est-il en pratique ?
La première chose est de réaliser des scanners interprétables et de systématiser la mesure du MS. La deuxième chose est de tenter de gagner en précision au moment du déploiement. C’est ce que nous appellerons la « golden touch » (Midas était un roi de la mythologie grecque a qui les dieux avaient donné le pouvoir de transformer en or tout ce qu’il touchait…).
• Un scanner interprétable. Pour visualiser les cavités droites, rajoutons 10 % de contraste au liquide de rinçage perfusé immédiatement après le bolus radio-opaque.
• Une mesure standardisée du MS. Mesurons-le dans un plan passant par la commissure entre les feuillets CD et NC. C’est la distance séparant le haut du septum musculaire du plan de l’anneau (photo 1, cas clinique).
• Une évaluation simple des calcifications. Dans cette zone, prenons en considération les calcifications de l’anneau, du MS ou du haut du septum musculaire, mais pas celles des feuillets. Il est aisé de distinguer les patients sans calcification (grade 0) de ceux sévèrement calcifiés (grade 2). Les grades 1 sont donc ceux ayant des calcifications modérées dans cette zone.
• Des précautions vis-à-vis des voies de conduction. Interdisons- nous de descendre trop profondément dans le VG et de toucher le septum musculaire. Avançons délicatement jusqu’au niveau zéro de l’anneau aortique, et commençons ici le déploiement.
• La bonne incidence pour augmenter la précision pendant le déploiement. Il faut éviter les erreurs de parallaxe. Il est en général admis que l’OAG est la meilleure incidence pour le déploiement de la prothèse. Mais dans cette incidence, la bioprothèse est en avant de la pig tail et toute mobilisation du tube en caudal entraîne un « écrasement » de la distance entre la pig tail et le bas de CoreValve™. L’OAD avec quelques degrés de caudal permet plus de précision mais génère plus de rayonnement diffusé et ne permet plus de visualiser le positionnement du guide dans l’aorte, sans parler du caractère inconfortable pour les médecins. Il semble donc raisonnable d’utiliser une combinaison des deux incidences : avancée du système dans l’aorte et la valve en OAG, déploiement en OAD, puis retour en OAG pour le largage (photos 2 et 3, cas clinique).
• L’évaluation finale. La meilleure incidence pour visualiser les rapports entre la partie distale de la CoreValve™ et le septum interventriculaire est une OAG perpendiculaire à la bioprothèse.
Cas clinique
Mme D. est une patiente de 81 ans en bon état général mais gênée par des problèmes arthrosiques. Elle est dyspnéique NYHA II du fait d’une sténose aortique devenue serrée au fil du temps. Dans son bilan, on retrouve un bon VG avec une HVG, une valve tricuspide de petite taille, des coronaires saines et un bloc de branche droit. Ses axes artériels membres inférieurs sont de petit calibre mais compatibles avec un TAVI fémoral. Ses scores de risque sont les suivants : STS : 2,5 % ; Euroscore 2 : 2,7 % ; Euroscore 1 : 9 %. Il s’agit donc d’une patiente à risque intermédiaire mais à haut risque de PM post-TAVI du fait de la préexistence du BBD. Elle en accepte le principe et la heart-team valve confirme la décision du TAVI pour cette patiente.
Le choix de la valve ne peut se porter que sur la Core- Valve™ (Medtronic) du fait du risque intermédiaire, de petit anneau et de l’HVG. L’analyse du scanner (Osirix™, Horos) montre un diamètre à 20,2 mm, pas de calcification au niveau de la chambre de chasse et une mesure du septum membraneux à 0,9 mm (photo 1). Les incidences à utilisées sont déterminées grâce à une matérialisation des points bas des cuspides, mais aussi du feuillet non coronaire (accueillant la pig tail) et de la CoreValve™ initialement positionnée dans la commissure entre les feuillets CD et NC (photo 2).
Il est donc réalisé une implantation d’une CoreValve™ 23 mm par voie fémorale avec pour objectif une hauteur finale d’implantation entre 0 et -1 mm (photo 3). Du fait du BBD, une sonde d’entraînement électrosystolique est placée dans le VD en début de procédure. La CoreValve™ est prudemment avancée en OAG jusqu’au niveau 0 de la valve (A). Puis on se positionne en OAD pour un déploiement précis (B et C). Après largage, la profondeur est mesurée à 1 mm. Il n’y a pas de modification de l’ECG (D). En conclusion, chez cette patiente relativement jeune avec un BBD et chez qui seule la CoreValve™ est implantable, un déploiement avec la golden touch a probablement permis d’éviter une implantation de pacemaker.
Photo 1. Analyse du scanner (Osirix™, Horos).
A : Dans ce plan bleu, le MS est facilement visualisable (flèches rouges). B : Au niveau des feuillets, on s’assure que le croisement des axes passe bien par le centre de la valve et on positionne un plan de coupe, ici le bleu, à travers la commissure entre les feuillets coronaire droit et non coronaire (flèches rouges). B’ : Puis on redescend au niveau de l’anneau virtuel où le MS est visualisé dans sa largeur (flèches rouges). C : Réalisation du sizing de la valve. D : Mesure du MS dans le plan bleu. Il s’agit de la distance séparant le septum musculaire de la ligne violette figurant le plan de l’anneau.
Photo 2. Choix des incidences.
A : Matérialisation du feuillet non coronaire (flèches rouges) et positionnement du croisement des axes au niveau de la commissure CD/NC (flèche noire) pour matérialisation de la CoreValve™ dans le plan perpendiculaire. B : Matérialisation de la CoreValve™ par une série de points formant une droite. C : Choix des incidences.
Photo 3. Déploiement de la CoreValve™.
A : L’OAG est utilisée pour avancer la valve dans l’aorte et amener l’amener jusqu’au niveau 0 de l’anneau. B : L’OAD permet un positionnement précis sans erreur de parallaxe. Le but est un positionnement entre 0 et -1 mm. C : Contrôle en OAD avant largage. La profondeur d’implantation est de 1 mm. D : Les ECG avant et après la procédure sont comparables.
Conclusion
La préexistence d’un BBD, un MS court (< 2 mm) et la présence de calcifications dans la zone sont des facteurs de risque importants de survenue de troubles de la conduction en post-TAVI.
Un déploiement de type MIDAS (minimizing depth according to the membranous septum) visant à larguer la CoreValve™ 1 à 2 mm au-dessus du septum musculaire permet de diminuer significativement le taux de survenue des troubles de conduction.
Pour ce faire, la golden touch passe par une bonne connaissance de la longueur du MS, des mesures de précautions vis-à-vis des voies de conduction et une optimisation des incidences à utiliser pendant le déploiement.
Le but ? Moins de 10 % de PM en post-CoreValve™ !
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


