Cas clinique
Publié le 20 déc 2017Lecture 3 min
Lésion non franchissable au ballon traitée par laser Excimer
Nicolas LHOEST, Giulio PRATI, GERC, Clinique de l’Orangerie, Strasbourg
Monsieur C.W., patient de 59 ans, présente comme facteurs de risque une HTA et une dyslipidémie et n’a aucun antécédent cardiologique.
Il est adressé par son cardiologue pour angor d’effort de novo. Une épreuve d’effort maximale est positive cliniquement et électriquement, avec des altérations du segment ST en V5-V6.
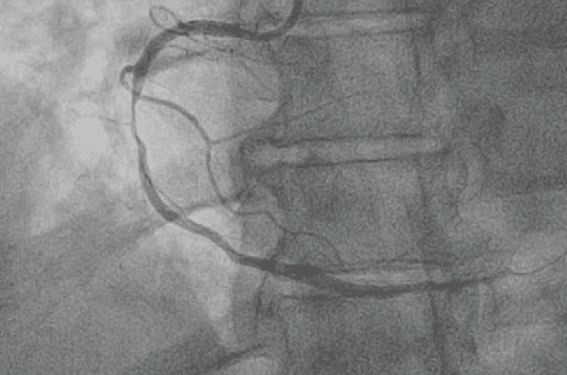
À la coronarographie, le réseau gauche est sans particularité. La coronaire droite présente une sténose critique à 90 % au niveau du segment 2 (figure 1). La plaque a un aspect angiographique de lésion fibreuse, sans évidence de calcification importante.
Figure 1. Sténose critique de la coronaire droite.
La coronaire droite est cathétérisée avec une sonde AL 1 (Medtronic Launcher®) 6F pour maximiser le support, et la lésion est franchie sans difficulté avec un guide de première intention (Asahi Sion Blu®). La lésion est non franchissable par le ballon haute performance de 1.0 mm de diamètre (OrbusNeich Sapphire Pro II®) et ce, malgré l’augmentation du support avec notamment l’utilisation d’une extension de cathéter (Guidion IMDS distribué en France par Biotronik®).
Les angioplasties complexes sont de plus en plus fréquentes et il est donc possible de se trouver dans l’impossibilité de franchir la lésion avec un microcathéter ou un ballon, ou de ne pas réussir à dilater la lésion même avec des ballons non compliants HP (échec du ballon). Une série anglaise(1) a estimé à environ 1 % le pourcentage d’angioplasties non réalisables au ballon seul.
Pour s’affranchir de ce type de problèmes, on utilise classiquement le Rotablator® (Boston Scientifics), mais sur ce type de lésion fibreuse, l’utilisation du Laser semble licite.
L’athérectomie coronaire au laser Excimer (ELCA) permet un debulking efficace et avec de rares complications. Le système (Spectranetics®) consiste en un cathéter qui libère au contact de la lésion et d’une façon pulsée, le rayonnement laser ultraviolet (figure 2) produit dans une console externe (figure 3).
Figure 2. Rayonnement laser.
Figure 3. Console externe du système Spectranetics®.
La technique peut être alternative ou complémentaire à l’athérectomie rotationnelle (RA) avec Rotablator® (Boston Scientifics). Dans le choix de la stratégie, il faut considérer que, pour les plaques très calcifiées, les effets du laser sont limités aux tissus sous-jacents au calcium et donc la réponse au laser en termes de gain en lumière est moins favorable(2). Dans cette indication, la RA reste le traitement de choix mais le guide dédié (Rotawire®) ou un micro-cathéter pour un échange de guide, ne peuvent pas être amenés en distalité dans tous les cas.
L’avantage principal du laser est de permettre son utilisation avec tous les guides 0.014. Dans le contexte d’« échec du ballon », plusieurs cas cliniques ont été publiés par une équipe anglaise qui a démontré la possibilité d’une approche hybride avec laser en première intention pour modifier le « cap » de la plaque, ce qui a permis ensuite de la franchir avec un microcathéteret de compléter l’angioplastie avec le Rotablator (technique que cette équipe a appelée RASER, Rotational Atherectomy, laSER)(3).Dans notre cas clinique de lésion fibreuse non franchissable par un ballon, l’ELCA peut donc être appliqué avec succès.
Plusieurs cathéters laser existent.
Dans ce cas, nous avons utilisé la sonde dédiée aux lésion résistantes, la 0,9 X 80 (Spectranetics®). Pour éviter l’échauffement des tissus et le risque de perforation et de dissection, le système d’injection doit impérativement être purgé du contraste et doit être irrigué en continu avec une solution saline 0,9 % à une vitesse de 1-2 ml/s.
Une fois positionnée en face de la plaque, la sonde doit être avancée lentement (0,5-1 mm/s) pour permettre aux tissus d’absorber au maximum l’énergie du laser. Dans notre expérience, l’augmentation du support grâce à une extension de cathéter est capitale pour la bonne réussite de la procédure. Après plusieurs passages (figure 4), la lésion est franchie par la sonde. L’angioplastie est ensuite complétée avec une prédilatation au ballon (Boston Scientific Emerge® 2,0-20 mm) (figures 5 et 6) et la pose d’un stent Boston Scientific Synergy® 3,0-20 mm. La figure 7 montre le résultat final. ELCA est un outil efficace et sûr pour le traitement de lésions non franchissables ou non dilatables au ballon.
Figure 4. Après plusieurs passages, la lésion est franchie par la sonde.
Figure 5.
Figure 6.
Figure 7. Résultats de la procédure.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


