Complication
Publié le 30 nov 2008Lecture 6 min
Des branches dites « accessoires » mais importantes…
P. AUBRY, O. BOUDVILLAIN, G. DUCROCQ, Centre Hospitalier Bichat-Claude Bernard, Paris
Contexte clinique
Mr D. âgé de 80 ans et sans antécédents coronaires, est hospitalisé pour le bilan d’un infarctus inférieur semi-récent non reperfusé. Il s’agit d’un patient diabétique et tabagique avec une atteinte athéromateuse périphérique (occlusion des artères fémorales superficielles), une rétinopathie diabétique et une insuffisance rénale (DFG estimé à 35 ml/min).
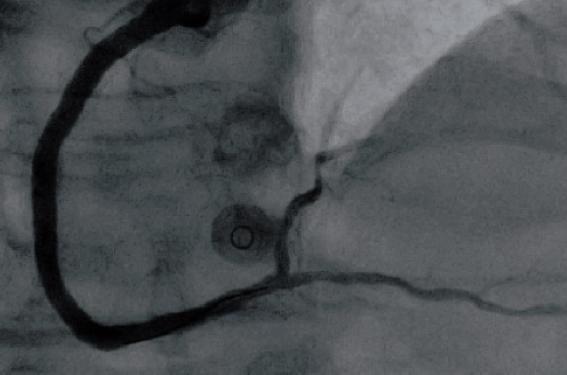
L’échocardiogramme montre une akinésie inférieure avec une fonction systolique modérément altérée (FE à 50 %). La coronarographie met en évidence une sténose serrée de l’IVA proximale et une occlusion de la coronaire droite moyenne (figure 1) ainsi qu’une collatéralité gauche-droite. En l’absence d’angor résiduel post-infarctus, une scintigraphie myocardique mixte est réalisée et montre une séquelle inférieure avec une ischémie périlésionnelle et également antérieure.
Figure 1. Vue en oblique antérieure gauche (oAG) de la coronaire droite avec une sub-occlusion longue à la fin du segment II. Les branches ventriculaires droites sont bien visibles, ainsi que l’artère du nœud sinusal (flèche).
L’indication d’une revascularisation percutanée est retenue en débutant par une désobstruction de la coronaire droite.
Procédure
Elle est réalisée par voie radiale droite avec un cathéter guide JR4 ZumaTM (Medtronic) et sous double thérapie antiplaquettaire (Kardégic® 75 mg + Plavix® 75 mg) avec un bolus intraveineux d’héparine non fractionnée (50 UI/ kg). La recanalisation est ef-fectuée avec un guide PilotTM 50 (Abbott Vascular).
Une prédilatation réalisée avec un ballon Maverick® (Boston Scientific) 3,0/20 mm à 10 bars (figure 2) est suivie d’un aspect de no-flow (figure 3) associé à une douleur thoracique intense et à une majorat ion du susdécalage du segment ST inférieur (figure 4).
Figure 2. Première inflation avec un ballon Maverick 2TM (Boston Scientific) 3,0/20 mm après recanalisation de la coronaire droite.
Figure 3. Aspect de no-flow de la coronaire droite.
Figure 4. Tracé ECG (DI, DII, DIII) avant (en haut) et après (en bas) la première inflation.
Un ballon coaxial SprinterTM (Medtronic) 2,0/12 mm est mis en place pour s’assurer par une injection distale du bon positionnement du cathéter. Plusieurs inflations étagées sont réalisées avec le ballon MaverickTM 3,0/20 mm permettant enfin une visualisation du lit d’aval (figure 5). L’aspect angiographique très pathologique du vaisseau nécessite la pose de 4 prothèses non actives jointives DriverTM (Medtronic) 3,0/30, 3,5/30, 3,5/30 et 4,0/12 mm entre la fin du segment III et le début du segment I. L’artère du nœud sinusal est encore perméable avant l’implantation d’une prothèse à son niveau (figure 6).
Figure 5. Aspect angiographique après des dilatations étagées sur les segments II et III. À signaler, la perte des branches ventriculaires droites.
Figure 6. Visualisation de face de l’artère du nœud sinusal (flèche) avant l’implantation d’une prothèse à son niveau.
Le flux coronaire final est sensiblement normal avec un trépied bien visualisé (figure 7). Par contre, une occlusion de l’artère du nœud sinusal est observée et les branches ventriculaires droites restent aussi occluses (figure 8) malgré des inflations complémentaires à hautes pressions (24 bars) avec un ballon NC SprinterTM (Medtronic) 4,0/20.
Parallèlement, un bloc sinoauriculaire apparaît (figure 9) avec un échappement jonctionnel à 40/min et une hypotension, alors que le sus-décalage du segment ST inférieur a tendance à s’atténuer. Le passage d’un guide dans l’artère du nœud sinusal est tenté sans succès. Une sonde d’entraînement systolique est mise en place par voie fémorale. Deux cents millilitres de produit de contraste iodé Visipaque 320TM (GE Healthcare) ont été administrés.
Figure 7. Aspect angiographique final après la pose de quatre prothèses DriverTM (Medtronic) entre l’ostium et la fin du segment III de la droite. À signaler, la perte de l’artère du nœud sinusal.
Figure 8. Aspect angiographique final en OAG avec disparition des branches ventriculaires droites et de la branche du nœud sinusal.
Figure 9. Tracé ECG (DI, DII, DIII) en fin de procédure avec bloc sinoauriculaire.
Évolution
Elle va être marquée par un tableau de bas débit cardiaque prolongé sur un infarctus ventriculaire droit avec dysfonction échographique et signes électriques classiques (figure 10), un pic de troponine à 22 mg/l et une insuffisance rénale aiguë transitoirement oligoanurique avec un pic de créatinine à 240 mmol/l (valeur initiale à 140) au 7e jour. Une hémodialyse et la pose d’un stimulateur cardiaque (figure 11) ont été discutées mais non réalisées.
Figure 10. Tracé ECG postprocédure avec sus-décalage ST dans les dérivations V1, V3R et V4R.
Figure 11. Aspect d’asystolie à l’arrêt de la stimulation ventriculaire droite au 6e jour.
L’évolution va cependant être favorable sous dobutamine et remplissage avec du sérum physiologique. On note un retour en rythme sinusal au 10e jour après un passage en tachyarythmie par fibrillation auriculaire.
Le patient sort du département au 20e jour en rythme sinusal avec une fonction systolique ventriculaire droite normalisée, une fraction d’éjection ventriculaire gauche identique à celle avant la procédure (50 %) et un retour à la fonction rénale initiale (DFG à 33 ml/min).
Commentaires
Il n’est pas habituel de protéger certaines branches collatérales, même de bon calibre, au cours d’une angioplastie de la coronaire droite. Un ralentissement du flux dans les branches ventriculaires droites après une angioplastie n’est pas rare mais reste généralement sans traduction clinique, électrique ou enzymatique. Une occlusion complète persistante peut donner des signes ischémiques avec en particulier des modifications de la repolarisation dans les dérivations V1-V3 parfois trompeuses. Des signes cliniques et échographiques d’infarctus ventriculaire droit peuvent être associés, avec une évolution et un pronostic identiques à ceux des infarctus biventriculaires, c’est-à-dire une récupération longue mais parfois complète comme cela a été observé chez notre patient.
L’artère du nœud sinusal, vaisseau de petit calibre, naît de la partie proximale de la coronaire droite dans environ 50 % des cas. Son flux peut être compromis au cours des syndromes coronaires aigus ST+ et des procédures interventionnelles, mais le retentissement sur la conduction est rare et souvent très transitoire. Le nœud sinusal a une suppléance artérielle importante qui explique sa résistance à l’ischémie. Cependant une dysfonction sinusale sévère et assez prolongée peut survenir comme dans le cas présenté.
Conclusion
Il est important de ne pas se précipiter pour poser l’indication d’une stimulation définitive, car la récupération spontanée d’un rythme sinusal est le plus souvent observée après la première semaine.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


