Publié le 21 sep 2010Lecture 7 min
Non-compaction ventriculaire gauche : une entité à part ou la présence de simples trabéculations ?
M.-C. MALERGUE, Institut coeur effort santé Paris, Hôpital privé Jacques Cartier Massy
La première description de ce qui fut appelé la non-compaction ventriculaire gauche (LVNC) remonte à 1984 à partir d’une observation échographique ; elle est décrite par un aspect particulier de la pointe, constituée d’importantes trabéculations et de récessus intertrabéculaires myocardiques. Ces anomalies étant regroupées dans le cadre d’une nouvelle cardiomyopathie congénitale(1).
Après cette observation isolée, c’est Chin en 1990 qui rapporta une série de 8 cas avec un contrôle autopsique chez 3 patients(2).
La population observée était jeune, témoignant d’un processus probablement congénital, l’âge allant de 11 mois à 22 ans avec un suivi moyen de 5 ans. L’expression anatomique était très variable, allant de formes sévères avec de larges trabéculations, à des formes plus modérées localisées à la pointe.
Les manifestations cliniques incluaient une dysfonction ventriculaire gauche chez 5 des 8 patients, des phénomènes arythmiques ventriculaires(5), des embolies systémiques(3) une dysmorphie faciale(3) et une récurrence familiale(4).
Cette anomalie serait due à un désordre de la morphogenèse endocardique, caractérisée par la présence d’un excès de trabéculations ventriculaires proéminant dans la cavité, associées à de profonds récessus intertrabéculaires.
Elle intéresse surtout la pointe de la cavité ventriculaire gauche avec un aspect « spongieux ».
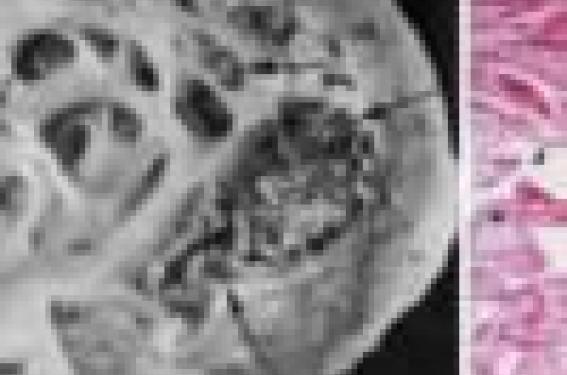
L’épaisseur myocardique est excessive avec une fine couche épicardique compactée et un endocarde très épais ; ce dernier est constitué de couches non compactées, avec des trabéculations faisant saillie dans la cavité, entremêlées de profonds recessus intertrabéculaires (figure 1).
Ces anomalies seraient secondaires à un arrêt anormal de l’embryogenèse, avec un arrêt de la compaction in utero, des formes transitoires à la naissance ayant été décrites.
Figure 1. Lésions anatomiques d’après Chin(2), à gauche les flèches blanches témoignent de large récessus et de nombreuses trabéculations de la pointe, associées à des thrombi in situ (flèches noires). À droite, 7 alternance d’un épicarde fin compacté et de trabéculations avec récessus de l’endocarde.
Classification du LVNC dans le cadre des cardiomyopathies
Les cardiomyopathies ont récemment fait l’objet de classifications différentes selon les sociétés savantes. Pour Maron, on distingue dans les cardiomyopathies primitives, les cardiomyopathies génétiques, mixtes et acquises. La LVNC se classe parmi les cardiomyopathies génétiques (figure 2). Dans la classification européenne (figure 3), le distinguo entre primitif et non primitif n’est pas fait et la LVNC est incluse dans le chapitre des cardiomyopathies « inclassables », rejoignant un groupe non exhaustif de maladies orphelines. Cette cardiomyopathie peut être associée à des désordres neuromusculaires et s’associer à d’autres malformations cardiaques.
La fréquence réelle de cette affection est très difficile à déterminer en raison du peu d’études publiées, du peu de corrélations anatomiques, et probablement des difficultés diagnostiques.
Dans la population pédiatrique, la LVNC apparaît comme la cardiomyopathie la plus fréquente après les cardiomyopathies dilatées et les cardiomyopathies hypertrophiques. Chez l’enfant, on retrouve très souvent un dysmorphisme et d’autres anomalies cardiaques associées de type WPW.
Sur une grande série rétrospective de la Mayo Clinic (1997) sur près de 40 000 échographies réalisées, le diagnostic n’est retenu que dans un très faible pourcentage.
Lors du dépistage familial en cas de LVNC diagnostiqué, la présence de 25 % de cas asymptomatiques est rapportée dans la fratrie, diagnostiqués en échographie.
De nombreuses mutations du génome ont été par ailleurs identifiées permettant d’en confirmer le support génétique et la fréquence des formes familiales.
Figure 2. Classification nord-américaine des cardiomyopathies d’après Maron.
Figure 3. Classification européenne d’après Eliott.
Diagnostic échographique
Dans le travail de Chin, les données échographiques comportaient la mesure du rapport X/Y où Y représentait la profondeur des récessus intertrabéculaires et X l’épaisseur de l’épicarde, ce rapport étant beaucoup plus grand que dans une série de sujets témoins(2). Les images échographiques ont été corrélées aux données morphologiques anatomiques disponibles (figures 1 et 4). Ce rapport X/Y est plus important à la pointe, comparativement aux mesures réalisées au niveau de l’anneau ou au niveau des piliers.
Plus récemment, Jenni (figure 4) a proposé la mesure du myocarde non compacté rapporté au muscle compacté (NC/C)(3); le rapport au-delà duquel on peut parler de LVNC est > 2 ; ce paramètre est estimé comme normal chez l’adulte à 0,5, il est plus élevé chez l’enfant à 1,4. Cette mesure doit être réalisée en systole, en coupe parasternale petit axe.
Le Doppler couleur permet de retrouver un aspect perfusé des récessus intertrabéculaires de la pointe, aidant au diagnostic, de même que l’utilisation d’un produit de contraste ventriculaire gauche comblant les récessus intraventriculaires.
Les critères retenus pour porter le diagnostic de NCLV sont rapportés dans le tableau 1.
Figure 4. Technique de mesure du rapport entre la zone compactée et la zone non compactés. A, rapport X/Y d’après Chin (1990). B Mesure NC/C d’après Jenni (2005).
Figure 5. Aspects échographiques d’un LVNC. A : coupe apicale des 4 cavités avec aspect très trabéculé de la pointe, dysfonction modérée ventriculaire gauche associée à une fraction d’éjection de 45 % ; B : coupe parasternale petit axe retrouvant un aspect de trabéculations en nid d’abeille ; C : Doppler couleur apical 4 cavités, retrouvant une vascularisation des récessus intertrabéculaires.
Les difficultés diagnostiques : LVNC ou simples trabéculations
À côté des formes majeures qui ne posent guère de problèmes diagnostiques, la multiplicité des présentations cliniques et la diversité du devenir peut rendre le diagnostic très difficile, tout particulièrement dans les formes sans dysfonction ventriculaire gauche.
Dans une étude récente, 65 patients chez lesquels le diagnostic de LVNC a été retenu ont été suivis en moyenne sur 46 ± 44 mois(4). Dans 82 % des cas, il existait un certain degré de dysfonction ventriculaire gauche et les 18 % restants avaient des volumes ventriculaires et une fonction ventriculaire gauche normale. Ces formes asymptomatiques touchaient des patients plus jeunes, diagnostiqués lors d’un dépistage familial ; aucun événement particulier n’est survenu lors du suivi chez ces patients. Ces patients asymptomatiques ont donc très souvent un très bon pronostic comparativement aux patients symptomatiques. La prise en charge thérapeutique n’est actuellement pas déterminée.
Le diagnostic peut donc être fait par excès, lorsque le patient est examiné dans le cadre d’une CMD idiopathique où il est possible de retrouver des trabéculations importantes de la pointe, ou à l’inverse par défaut lorsque cet aspect de trabéculations n’entraîne pas de manifestation clinique et survient avec une fraction d’éjection normale. Le diagnostic peut donc être un véritable challenge entre une LVNC authentique et des trabéculations banales, comme cela peut être observé chez le sujet sain ou lors d’une cardiomyopathie d’une autre nature. L’étude échographique doit donc être minutieuse par une mesure, parfois difficile, entre épaisseur de l’épicarde et de l’endocarde, la surface de la zone non compactée semblant corrélée au degré de dysfonction ventriculaire gauche.
Apport de l’IRM
La haute définition de l’IRM est d’un apport essentiel en cas de doute diagnostique. Petersen propose un diagnostic en IRM basé sur le rapport NC/C en diastole(5) ; lorsque celui-ci est > 2,3, cela permet de distinguer les trabéculations pathologiques des autres trabéculations retrouvées chez le sujet sain et dans différentes situations cliniques ; ce paramètre a été déterminé comparativement à une population de sujets sains, mais également à des patients ayant une cardiomyopathie hypertrophique, des athlètes, des coeurs d’hypertendus, des cardiomyopathies dilatées et des sténoses aortiques. De même, en échographie, les territoires apical et latéral sont plus souvent atteints que les segments basal et septal. Un rapport NC/C > 2,3 en diastole permet donc de distinguer la non-compaction pathologique avec une sensibilité, une spécificité, une valeur diagnostique positive et négative respectivement de 86 %, 99 %, 75 % et 99 %. L’IRM est donc un examen d’une très grande utilité grâce à son excellente résolution et à la possibilité de diagnostiquer des formes plus modestes avec une meilleure précision diagnostique (figure 6).
Figure 6. (document J. Garot) IRM d’une forme majeure de LVNC avec une ectasie de la pointe (incidence 4 cavités).
Le registre français
Ce registre, mis en place par Gilbert Habib avec l’aide des différents groupes de travail de la Société française de cardiologie, a permis de regrouper, dans une étude multicentrique, 110 patients. Sur ces 110 patients adultes, le diagnostic est incertain dans 40 % des cas, confirmant la difficulté souvent rencontrée entre trabéculations physiologiques ou pathologiques.
Une prédominance masculine est rapportée, la moyenne d’âge au moment du diagnostic est de 45 ans ± 17 ans. Le diagnostic est parfois fait tardivement audelà de 60 ans.
Dans 18 cas, on retrouve un antécédent cardiaque majeur familial ; dans 8 cas, il s’agit de forme familiale.
La manifestation clinique la plus fréquemment retrouvée reste l’insuffisance cardiaque dans 50 % des cas. Puis, par ordre décroissant, le diagnostic est fait au décours de l’évaluation d’une CMD, de troubles du rythme, d’une embolie systémique, lors d’un dépistage familial dans plus de 10 %.
La fraction d’éjection est < 30 % dans 45 % des cas, mais 15 % des patients ont une fraction d’éjection normale, confirmant ainsi les données de la littérature.
Dans ces cas, la zone de non-compaction est très localisée à la pointe.
En pratique
La LVNC semble une entité à part, associant des anomalies histologiques et des mutations génétiques multiples et hétérogènes. Certaines formes combinées peuvent s’exprimer avec un phénotype divers : LVNC associée à une CMH.
S’il n’y a pas de consensus formel quant au diagnostic, avec des critères variables selon les techniques échographique et IRM ; cet aspect semble correspondre à une véritable cardiomyopathie.
Le diagnostic peut s’avérer difficile dans les formes localisées et/ou asymptomatiques.
Associée à une confrontation des imageries, une enquête génétique est parfois nécessaire d’autant qu’il s’agit d’une forme familiale.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :