Thrombose
Publié le 09 mai 2017Lecture 10 min
Occlusion de l’auricule : le point !
François BRIGADEAU, CHRU de Lille
La fibrillation atriale (FA) est l’arythmie la plus fréquente. Elle est responsable d’une morbimortalité et d’un coût de santé très important. Elle est associée à un sur-risque d’accident thromboembolique artériel (ATE). Globalement ce risque est multiplié par 5 dans la FA, ce qui revêt des situations très diverses selon les patients. Ce risque est évalué par le score de CHA2DS2-VASc qui, s’il excède 0, impose la mise en route d’un traitement anticoagulant oral définitif. Malheureusement, on connaît les difficultés d’éducation thérapeutique, d’observance, de surveillance d’un traitement anticoagulant et de ses complications. Les anticoagulants oraux directs apportent une très substantielle amélioration dans ce domaine mais gardent une iatrogénie importante en termes de risque de saignement, notamment à point de départ digestif, avec un niveau d’efficacité comparable aux AVK (qui réduisent le risque relatif d’ATE d’environ 65/70 % par rapport au placebo). L’occlusion de l’auricule représente une alternative chez les patients ayant une contre-indication aux anticoagulants oraux.
L’oreillette gauche (OG) est la zone élective de constitution des thrombi dans la FA. L’auricule gauche, appendice antérolatéral de l’oreillette, est le plus souvent concerné. On estime sur des études anatomopathologiques, échographiques transœsophagiennes (ETO) et autopsiques que 90 % des thrombi de l’OG sont localisés à l’auricule. Depuis la fin des années 1990, des dispositifs d’occlusion de l’auricule, implantables par voie percutanée ont donc été développés dans le but de réduire le risque d’ATE chez les patients victimes de FA.
L’auricule gauche
Il s’agit du reliquat embryologique de l’OG, le reste de la cavité dérivant plutôt de l’extension musculaire des veines pulmonaires(1). L’auricule est anatomiquement en relation étroite avec la veine pulmonaire supérieure gauche en arrière, l’anneau mitral et la circonflexe en avant (figure 1). Il existe une grande variabilité anatomique interindividuelle qui est importante à prendre en compte car la complexité de la procédure en dépend. Une classification a été proposée en scanner. L’ostium de l’auricule est le plus souvent elliptique avec un diamètre oscillant entre 10 et 40 mm. Dans deux tiers des cas, l’auricule a un ou deux lobes qui partent en avant et reposent sur l’anneau mitral. Histologiquement il est constitué d’un muscle pectiné dont les cordons sont séparés par une membrane pellucide, zone de fragilité importante de la structure. Hémodynamiquement, il a un rôle de réservoir agissant comme un volant de pression. On lui prête également un rôle endocrine via la sécrétion d’ANP.
En FA, on assiste à une modification de l’endothélium atrial, à une hypercoagulabilité et à une réduction majeure des vitesses de vidange de l’auricule. On a donc les conditions complètes de la triade de Virchow pour la constitution des thrombi. On estime que 15 % des patients ont un thrombus intracavitaire. Dans 90 % des cas, il est situé dans l’auricule gauche. Cette proportion diminue dans la FA valvulaire (la moitié des thrombi sont intra-auriculaires), dans l’insuffisance cardiaque et en cas d’antécédent d’ATE.
Figure 1. Image d’auricule bilobé en ETO à 85° (en haut). Même patient (en bas) Reconstruction scannographique de l’auricule.
Technique de mise en place des dispositifs
Bilan préinterventionnel
La procédure nécessite un bilan de faisabilité préalable. Celui-ci comprend une consultation avec le malade et éventuellement son entourage (population âgée), pour l’explication du rapport bénéfice/risque. Il faut prévoir une consultation avec l’anesthésiste, la plupart des procédures étant réalisées sous anesthésie générale. Par ailleurs, une prise en charge multidisciplinaire est recommandée par les sociétés savantes pour poser l’indication, réaliser la procédure, et définir le traitement antithrombotique postinterventionnel.
L’ETO est l’examen préinterventionnel le plus important. Elle permet de mesurer les dimensions de l’auricule à l’ostium, d’en évaluer la profondeur, d’exclure les anatomies trop extrêmes en taille qui ne correspondent pas aux tailles de prothèses disponibles. Surtout, elle permet de visualiser avec une excellente sensibilité et spécificité les thrombi intra-auriculaires qui constituent une contre-indication formelle au geste(2).
Un scanner avec reconstruction tridimensionnelle de l’OG est également hautement souhaitable. Il permet de visualiser aisément le type anatomique, le nombre de lobes, l’orientation tridimensionnelle de l’auricule et ses rapports au reste de l’OG. Il a aussi une très bonne sensibilité et spécificité dans la détection des thrombi (figure 2).
Figure 2. Thrombus en ETO (en haut) et en scanner (en bas).
Les principaux dispositifs
(figure 3)
Deux types de dispositifs sont implantés principalement. Le système Watchman™ (Boston Scientific) est une prothèse en nitinol recouverte de goretex, préchargée dans une gaine que l’on place dans l’auricule. En retirant la gaine la prothèse se déploie obturant de façon étanche l’auricule. La solidité de l’implantation est assurée par des crochets latéraux qui s’implantent dans le muscle auriculaire.
La prothèse Amplatzer™ (ACP) remplacée récemment par la prothèse Amplatzer™ Amulet™ (St Jude Medical) est composée d’un disque interne épais qui constitue la prothèse implantée (avec système d’ancres latérales) et d’un disque externe plus fin et de surface plus large qui recouvre l’ostium sur sa face endoatriale.
Figure 3. Prothèse Watchman™ (en haut) ; prothèse Amulet™ (en bas).
La procédure
Elle doit être réalisée sous anesthésie générale, dans un centre expérimenté, possédant un recours possible immédiat à la chirurgie cardiaque. L’accès à l’OG est effectué via un cathétérisme transseptal sous contrôle ETO. On cathétérise l’auricule avec une pigtail pour ne pas être traumatique. Sur cette sonde on monte une gaine dans laquelle est placé le dispositif. Une fois déployé dans l’auricule, on vérifie la solidité de l’ancrage par une traction, l’étanchéité de la prothèse et sa bonne compression angiographique et échographique (figures 4 à 6). Lorsque la position est satisfaisante la prothèse est libérée par simple dévissage. Dans les études les plus récentes, on obtient un taux de succès de l’implantation en intention de traiter de 95 à 97 %.
Figure 4. Déploiement de prothèse Watchman™.
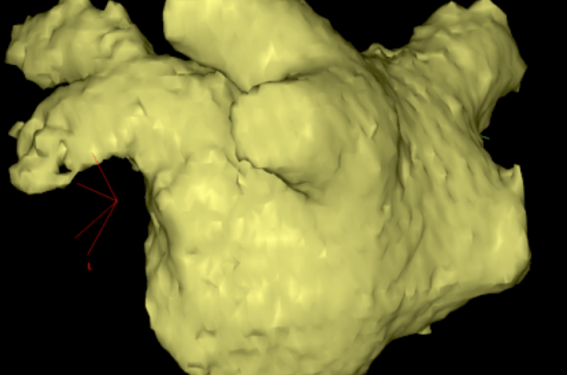
Figure 5. Auricule gauche avant et après implantation d’un dispositif Watchman™.
Figure 6. Prothèse ACP avant largage.
Suivi postinterventionnel
Le patient est revu en consultation à 6 mois puis une fois par an. Il doit avoir une ETO de contrôle à J45, et à 6 mois, pour réévaluer la position et l’étanchéité de la prothèse et réévaluer l’intérêt d’un traitement antithrombotique. Les fuites autour du dispositif peuvent être assez fréquentes (jusqu’à 30 %), elles sont rarement d’un diamètre significatif (arbitrairement choisi à plus de 3 mm). Peu d’entre elles régressent. Elles ne semblent pas être associées à un sur-risque thromboembolique, bien que l’étude de sous-groupe qui le démontre soit réalisée sur un suivi court et chez des patients poursuivant pour certains le traitement par antivitamine K. L’ETO recherche également les déplacements tardifs de prothèse complication rare (0,7 %) mais sérieuse.
Il existe un risque théorique de constitution de thrombus en surface de la prothèse, au décours de la procédure, jusqu’à endothélialisation. Trois schémas thérapeutiques semblent se dégager actuellement au décours de la procédure :
La mise en route d’un traitement anticoagulant oral de 45 jours jusqu’à l’ETO de contrôle, puis aspirine/clopidogrel 6 mois, pour les patients ne présentant qu’une contre-indication au long cours de leur traitement antithrombotique.
Dans le cas d’une contre-indication au traitement anticoagulant sans contre-indication au traitement antiagrégant, on peut proposer 6 mois de bi-antiagrégation plaquettaire aspirine/clopidigrel, ou aspirine seule.
Parfois tout traitement antithrombotique est contre indiqué et l’on doit se résoudre à l’absence de traitement au décours.
Les patients actuellement implantés ont un risque thromboembolique substantiel, puis que le CHA2DS2-VASc doit être supérieur à 4 selon les recommandations de l’HAS. Il faut donc bien évaluer en amont de la procédure et de façon pluridisciplinaire le type de traitement postprocédure.
Indication des implantations et études cliniques
Avec le Watchman™
Deux études randomisées et plusieurs registres ont comparé le dispositif Watchman™ aux AVK soit environ 2 400 patients implantés du dispositif.
La première étude est PROTECT-AF(3), 707 patients randomisés AVK ou implantation, chez des patients avec FA non valvulaire, CHADS2 ≥ 1. Dans cette indication, les patients contre-indiqués aux AVK étaient bien sûr exclus. Après l’implantation, les patients recevaient 45 jours d’AVK, (le temps présupposé d’endothélialisation de la prothèse). Une ETO de contrôle était pratiquée à J45, M6 et M12 pour vérifier l’absence de fuite périprothétique. Les AVK étaient alors arrêtés (au profit de 6 mois de double antiagrégation plaquettaire aspirine/clopidigrel 81 mg/75 mg puis d’aspirine seule) et poursuivis si la fuite excédait 5 mm.
Il s’agit d’une étude de non-infériorité versus AVK pour un critère principal composite (ATE, AVC ischémique ou hémorragique, mort subite inexpliquée ou mort cardiovasculaire). Le critère principal de sécurité analysait les saignements graves (intra ou extracrâniens) et les complications imputables à la procédure.
Les résultats ont montré que le taux de succès d’implantation était de 88 %. Quatre-vingt-douze pourcent de ces patients pouvaient effectivement arrêter les AVK au terme du suivi. Le critère de non-infériorité a néanmoins été obtenu au prix d’un taux de complication d’environ 10 % (taux de complication grave de 4,4 % soit 22 patients : tamponnades drainées, accidents vasculaires cérébraux, déplacement de prothèse). Il existe clairement un effet « courbe d’apprentissage », puisque dans le registre complémentaire CAP(4) qui a poursuivi les inclusions au-delà de l’étude, le taux de complication chute de façon drastique alors que le taux de succès d’implantation passe à 95 %.
Le suivi à long terme (suivi médian de 45 mois) des patients implantés dans PROTECT-AF confirme la non-infériorité de l’occlusion de l’auricule versus AVK avec un bénéfice qui s’accentue avec le temps au profit des patients implantés sur le critère principal et la mortalité totale(5). Néanmoins, la FDA a demandé une étude complémentaire en raison du profil à bas risque des patients implantés et aussi du risque interventionnel important : c’est l’étude PREVAIL(6).
Il s’agit là encore d’une étude de non-infériorité sur 461 patients randomisés dont 269 reçoivent le dispositif. Les patients avaient un risque thromboembolique plus élevé que dans PROTECT-AF, puisque le score de CHADS2 médian était à 2,6. La plupart de centres étaient expérimentés dans cette procédure. Il y avait trois critères d’évaluation principaux :
La survenue d’un AVC ischémique ou hémorragique ou d’un ATE dans les 18 mois de suivi requis.
La survenue d’un accident ischémique ou d’un ATE au-delà du 8e jour après la randomisation pour exclure les accidents directement imputables à la procédure.
La survenue d’un décès, accident vasculaire cérébral, ATE, d’une complication du geste nécessitant une chirurgie cardiaque ou vasculaire, dans les7 jours suivant la procédure.
La non-infériorité n’a pas été obtenue dans cette étude. Il s’agit probablement de la conjonction d’un taux d’événements plus élevé qu’attendu dans le groupe implanté et bien plus faible qu’attendu dans le groupe contrôle (AVK). En revanche, elle confirme la régression du taux de complications et l’effet courbe d’apprentissage.
L’association d’un risque thromboembolique élevé et d’un risque hémorragique élevé avec contre-indication d’une anticoagulation orale au long cours représente une quadrature du cercle qui pour l’instant n’avait pas d’autre solution thérapeutique que l’abstention. Alors qu’il s’agit d’une recommandation de l’ESC de niveau 2bB, le niveau de preuve pour proposer l’implantation d’un système d’occlusion de l’auricule gauche est faible dans ce contexte.
Seule l’étude ASAP(7) a montré un bénéfice. Elle a permis de comparer 150 patients implantés d’un dispositif et présentant une contre-indication définitive aux AC à une population appariée sur le score de CHA2DS2-VASc. Il ne s’agit donc pas d’une étude randomisée. Par rapport à cette population potentielle, on estime la réduction du risque relatif d’accident vasculaire cérébral à 64 % (en tenant compte de l’antiagrégation plaquettaire parfois maintenue chez certains patients). Sur cette donnée, l’HAS(8) a autorisé l’implantation de ces dispositifs en insistant sur la nécessité d’une équipe de prise en charge multidisciplinaire, de la présence sur site d’un bloc de chirurgie cardiaque, de l’inscription des patients dans un registre. Il faut également que l’indication soit posée chez des patients avec score de CHA2DS2-VASc ≥ 2 ainsi qu’une contre-indication formelle et définitive aux anticoagulants oraux. Malgré un niveau de preuve bas, il est précisé dans ces recommandations que cette solution est possible chez ces patients dans la mesure où en l’état actuel il n’y a pour eux aucune alternative thérapeutique. Le refus du patient de se soumettre à un traitement anticoagulant ne constitue pas une indication à la procédure.
Avec l’Amplatzer™ Cardiac Plug (ACP) et l’Amplatzer™ Amulet™
L’évolution du dispositif s’est faite d’un simple dispositif de fermeture de la communication interauriculaire (CIA) vers une structure à doubles disques asymétriques, dont le disque interne est implanté dans l’auricule et l’externe, plus large, est appliqué sur l’ostium. A l’heure actuelle on ne possède que les résultats de registres rétrospectifs(9). Néanmoins, ils montrent une bonne sécurité d’emploi de cette prothèse (taux d’implantation de 97 % avec taux de complication lié à la procédure autour de 5 %, mais une définition variable selon les registres. Il y a une étude en cours avec ce dispositif aux États-Unis pour vérifier que les résultats obtenus avec ce système soient superposables aux résultats obtenus avec le système Watchman.
Conclusions
Il s’agit d’une technique d’avenir qui propose de réduire le risque d’ATE liés à la FA par occlusion de l’auricule. Les résultats initiaux montrent une validité du concept, une faisabilité de la technique avec un taux de complication tout à fait acceptable. L’indication repose actuellement sur l’association d’un risque thromboembolique élevé et d’une contre-indication définitive aux anticoagulants oraux. Il faudra néanmoins asseoir cette indication par la réalisation d’une étude comparant l’absence de tout traitement à la procédure d’occlusion.
Les résultats en alternative aux anticoagulants sont également très encourageants. On ne peut néanmoins pas comparer les résultats sur les milliers de patients avec anticoagulants aux patients implantés d’un dispositif. Par ailleurs, les études comparant l’implantation aux anticoagulants n’ont pas intégré les anticoagulants oraux directs, ce qui est désormais indispensable.
Chaque situation hémorragique étant en soi assez spécifique, insistons sur l’importance d’une prise en charge collégiale, le cardiologue interventionnel n’étant pas toujours le plus à même d’évaluer le risque hémorragique au long cours, et de prescrire le traitement anti thrombotique post procédure.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :