Rythmologie et rythmo interventionnelle
Publié le 10 avr 2007Lecture 7 min
Comment prendre en charge un syndrome de Brugada ?
J.-S. HERMIDA, H. BAKKOUR et M. KUBALA, CHU Amiens-Picardie
Les Journées européennes de la SFC
La prise en charge des patients porteurs d’un syndrome de Brugada dépend principalement de l’aspect ECG et du caractère symptomatique ou non de l’affection.
Sujets symptomatiques
En présence d’un événement rythmique, mort subite ressuscitée ou syncope pour laquelle un trouble du rythme a été documenté ou est fortement suspecté, l’indication de la mise en place d’un défibrillateur automatique implantable (DAI) est impérative. Le taux de récidives à 2 ans est évalué de 22 à 40 %, selon les séries.
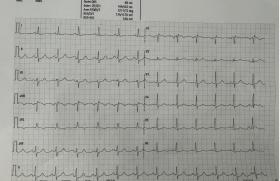
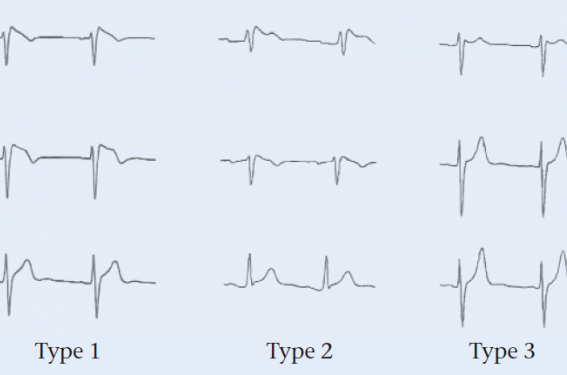
En cas de malaises inexpliqués, mais cliniquement peu évocateurs, l’indication d’un DAI se pose également si l’ECG montre un aspect majeur spontané (type 1) du syndrome (figure). La possibilité d’induire une fibrillation à la stimulation ventriculaire programmée et les antécédents de mort subite familiale ont une valeur discutée. L’utilisation d’un holter implantable peut être utile pour documenter les symptômes litigieux.
ECG du syndrome de brugada.
Sujets asymptomatiques
La problématique est voisine chez les patients asymptomatiques qui ont un ECG de type 1. Le taux annuel d’événements rythmiques qui, dans les publications des frères Brugada en 1998, était de 10 % à 2 ans, est revu régulièrement à la baisse. Les taux annuels publiés actuellement sont de 0,34 à 1,7 %. Il faut souligner d’ailleurs que l’événement rythmique correspond selon les études à l’association à des degrés variables d’une récidive de mort subite, d’une syncope ou d’un choc approprié. On conviendra que chacun de ces critères a une signification et une gravité différentes.
Événement rythmique et mortalité sont des entités différentes
Il n’est pas certain, par exemple, qu’une syncope chez un patient porteur d’un aspect ECG de Brugada soit nécessairement due à un trouble du rythme ventriculaire.
Dans le travail récent de Sacher, seuls 17 % de ces patients, porteurs d’un DAI, ont récidivé leur syncope et, dans 40 % des cas, celle-ci n’était pas due à un trouble du rythme ventriculaire. Il n’est pas certain non plus qu’un patient recevant un choc approprié de son DAI doive la vie à son appareil. On sait que les troubles du rythme ventriculaire peuvent être spontanément non soutenus et que l’intervention du DAI dans ce cas ne fait qu’interrompre prématurément l’accès.
La décision de mettre en place un DAI dans ce contexte se discute de plus en plus, d’autant que ces appareils ne sont pas dénués d’inconvénients et que l’identification des patients devant être appareillés n’est pas clairement établie. Parmi les dysfonctionnements du DAI ou des électrodes, citons les chocs inappropriés, élévations de seuil de défibrillation ou de stimulation, extériorisation et sepsis. L’impact psychologique et socio-professionnel peut être majeur chez des sujets souvent jeunes. Cela est sans compter avec la non-disponibilité du DAI en dehors des pays industrialisés et un coût important. En ce qui concerne la stratification du risque chez les sujets asymptomatiques ayant un ECG de type 1, les dernières publications, notamment de Eckart, Sacher et la métaanalyse de Gehi, ont mis en question la valeur de l’exploration électrophysiologique et des antécédents de mort subite familiale a été remise en question dans la stratification du risque du patient asymptomatique avec ECG de type 1. Ces études souffrent toutefois d’un manque de puissance en raison du faible nombre d’événements à prédire.
Ces considérations devraient conduire à une réflexion sur la place du traitement par quinidiniques. Celui-ci pourrait être plus adapté que le DAI ou que l’abstention thérapeutique du fait de ces nouvelles données.
L’hydroquinidine s’est révélée efficace dans le contrôle des orages rythmiques du syndrome de Brugada et cela, parfois à faibles doses.
Les quinidiniques sont capables également de supprimer la possibilité d’induire une fibrillation ventriculaire à la stimulation ventriculaire programmée dans 75 % des cas. Cela indique une action certaine sur ce substrat électrophysiologique particulier. La piste médicamenteuse apparaît donc comme une alternative à considérer mais demande encore actuellement une validation par une étude prospective randomisée.
Chez les patients asymptomatiques porteurs d’un aspect ECG mineur (type 2 ou 3) du syndrome de Brugada, le test à l’ajmaline s’est révélé le meilleur outil diagnostique, surtout en utilisant les dérivations précordiales droites. Il permet d’éliminer les aspects ECG non liés au syndrome. Chez les patients asymptomatiques porteurs d’un syndrome de Brugada pharmaco-inductible, une surveillance ECG au long cours doit être proposée. Des recommandations sur les thérapeutiques à éviter (antidépresseurs, bêtabloquants, lithium, antiarythmique de classe 1c, anesthésiques locaux) et des précautions à prendre en cas d’hyperthermie (infection, sport) font partie des informations à délivrer.
En cas de syndrome de Brugada acquis transitoire (myopéricardites, antidépresseurs…), la surveillance paraît inutile si le test à l’ajmaline est clairement négatif.
Les formes familiales
En cas de syndrome de Brugada dûment prouvé, une enquête familiale systématique est nécessaire. Elle s’effectue par l’ECG et le test à l’ajmaline.
Le rendement de l’enquête familiale dépend de la conviction avec laquelle elle est réalisée et des moyens mis en œuvre. Lorsqu’elle se borne à l’interrogatoire du propositus, on retrouve un taux de formes familiales de 17 %. Lorsque l’on complète l’arbre généalogique grâce aux informations obtenues de l’ensemble des membres de la famille et que l’on propose systématiquement un ECG et un test à l’ajmaline, le taux de formes familiales atteint 65 %.
En cas de découverte d’autres porteurs du syndrome dans une famille, la conduite à tenir est identique à ce qui est proposé plus haut. Elle se décline selon l’importance des signes ECG et du caractère symptomatique ou non de l’affection.
Pour le propositus lui-même, la découverte d’un autre sujet atteint dans la famille a aussi une signification importante. Elle indique que, dans son cas, l’hypothèse d’un syndrome de Brugada acquis, transitoire ou pas, est improbable. Une origine génétique devient très probable dès lors que plusieurs sujets sont atteints dans la même famille.
Quand le propositus est porteur d’une mutation de SCN5A, les collatéraux qui le souhaitent peuvent être soumis à la recherche de la mutation, ce qui simplifie l’enquête familiale. Il reste toutefois nécessaire de réaliser le test à l’ajmaline chez les sujets porteurs de la mutation quand l’ECG de surface est normal ou de type 2 ou 3. La pénétrance de la maladie est variable et plus le degré de déformation du segment ST, spontanément ou sous l’effet de l’ajmaline, est important, plus on peut suspecter que les transports ioniques peuvent être compromis. Il est tentant de dresser un parallèle physiopathologique avec le syndrome du QT long congénital pour lequel il est reconnu que la longueur de l’espace QT corrigé est un facteur pronostique important.
Les morts subites familiales
La signification des morts subites familiales n’est pas établie avec précision. La survenue d’une mort subite dans une famille est un fait dramatique. Le retentissement émotionnel est d’autant plus important qu’il concerne un sujet jeune et l’éventualité d’une récidive dans la même famille est insupportable. Subjectivement, on peut être fortement tenté d’apporter une réponse radicale dans ce contexte.
Il n’y a pas, toutefois, de données objectives prouvant le caractère péjoratif d’une mort subite familiale pour ceux qui sont également porteurs du syndrome de Brugada, notamment si on se réfère à la méta-analyse récente de A.-K. Gehi.
Le caractère variable de la pénétrance et les qualités protectrices de certains polymorphismes présents aux côtés des mutations indiquent que tous les individus d’une même famille ne sont pas soumis aux mêmes risques. Il convient donc d’être prudent et d’analyser l’ensemble des données disponibles pour chaque individu. Parfois, on peut obtenir des informations sur le sujet décédé. L’aspect ECG peut être utile car on dispose dans ce cas d’une image de ce qui constitue un risque indéniable. Il est primordial également de recueillir d’autres informations telles que l’âge, les facteurs de risque cardiovasculaire et le contexte de survenue de la mort subite. Les étiologies des morts subites sont multiples. Il est parfois possible, après un interrogatoire précis, d’exclure la responsabilité du syndrome de Brugada et de conseiller la famille.
En pratique
La prise en charge des patients porteurs d’un syndrome de Brugada est en pleine évolution chez les sujets asymptomatiques. Ceux-ci sont de plus en plus nombreux à être individualisés.
Les aspects ECG mineurs sont désormais souvent reconnus en dehors du milieu cardiologique tels qu’en médecine du sport, du travail ou en médecine préventive (sécurité sociale). Une confirmation diagnostique est nécessaire et repose en pratique sur le test à l’ajmaline ou à la flécaïnide.
La conduite à tenir dépend de l’importance du sus-décalage du segment ST, seul facteur prédictif qui semble conserver de la valeur. Une aide peut être apportée selon les cas par la mise en place d’un holter implantable (Reveal).
La réalisation d’études randomisées comparant les traitements disponibles et l’abstention thérapeutique, et prévoyant la validation des facteurs de stratification du risque est hautement souhaitable.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :