Rythmologie et rythmo interventionnelle
Publié le 15 avr 2017Lecture 12 min
Rhythm 2017 : les points forts
Édouard GITENAY, Clément BARS, André PISAPIA Hôpital Saint-Joseph, Marseille
Le congrès Rhythm qui cette année, se tenait à Paris, a encore une fois été un succès en fédérant plus de 300 participants autour d’un programme d’une exceptionnelle qualité. Durant deux jours, un panel d’experts nationaux et internationaux se sont réunis autour des sujets d’actualité en rythmologie. Une place importante a été dédiée à la fibrillation atriale, et notamment aux approches d’ablation personnalisées, ainsi qu’à l’ablation des arythmies ventriculaires. De nouveaux concepts dans la compréhension des arythmies complexes ont été développés. Les dernières innovations technologiques en stimulation et en défibrillation cardiaque ont également été mises à l’honneur.
La majeure partie des communications de la première journée du congrès concernait différentes thématiques de la fibrillation atriale (FA).
Anatomie et mécanismes de la FA
C’est K. Mc Carthy de l’équipe d’anatomie spécialisée du Royal Brampton de Londres qui a ouvert les débats avec une présentation abondamment illustrée ayant détaillé les différentes structures des deux oreillettes, très appréciée par l’auditoire. Elle a notamment mis en avant les afférences nerveuses à ce niveau, en mettant en perspective leur implication possible dans le déclenchement et le maintien des arythmies atriales.
M. Alessie (Rotterdam) a présenté les résultats de son travail de mapping endo- et épicardique au moyen de bandes disposant de presque 200 électrodes, réparties sur les différentes zones des deux oreillettes (versants endo- et épicardiques) chez 60 patients en FA persistante (lors d’interventions de chirurgie cardiaque)(1). Le système a permis de mettre en évidence un nouvel aspect physiopathologique de la FA : il existe un asynchronisme endo-épicardique pendant l’arythmie et les zones focales d’apparition des vagues d’activation semblent correspondre à des zones de passage entre les deux couches (figure 1).
Les résultats du nouveau système de mapping non invasif de F. Atienza (Centro Cardiovascular, Madrid) au moyen d’une veste multi-électrodes rejoignent de leur côté les conclusions de plusieurs autres travaux préalables en faveur de l’existence de « drivers » focaux (foyers rapides ou zones rotationnelles « rotors »).
L’impact et la détection de la fibrose atriale par l’IRM cardiaque (se traduisant par un rehaussement tardif après injection de gadolinium) ont ensuite été mis en avant par J. Horvilleur (Institut Cardiovasculaire Paris-Sud, Massy). Les résultats de l’IRM sont anatomiquement bien corrélés avec les constatations électrophysiologiques (cartes de voltage surtout mais aussi fractionnement). Le degré de fibrose apparaît statistiquement lié au temps de radiofréquence ainsi qu’au temps nécessaire pour arrêter la fibrillation pendant l’ablation, et semble prédire le succès de l’ablation de façon plus fiable que le type de FA.
Figure 1. Mapping endo-épicardique de la FA au cours d’une chirurgie cardiaque d’après N. de Groot et coll.
L’IRM pourrait devenir un outil de pratique courante pour sélectionner les patients et guider la stratégie d’ablation dans l’avenir.
Ablation de la FA basée sur les enregistrements endocavitaires
Au cours de cette session, différents experts ont démontré l’importance d’intégrer les signaux électriques endocavitaires dans la stratégie d’ablation de la FA. Dans un premier temps, T. Pambrun (CHU de Bordeaux) a retracé l’histoire de l’ablation de la FA guidée par les signaux électriques, depuis les premières constatations de signaux anormaux et la compréhension de l’anisotropisme dans les années 1980, jusqu’à la compréhension des différentes composantes de la FA, dispersion, fractionnement, firing ayant permis de redéfinir les stratégies ablatives au cours des 20 dernières années.
L’importance de l’analyse du voltage a ensuite été soulignée par A. Jadidi (Bad Krozingen, Allemagne), dont une étude a récemment montré que l’ablation de ces zones peu voltées qui se superposent aux zones de dispersion du signal, adjointes à l’isolation des veines pulmonaires est supérieure à l’isolation veineuse seule dans l’ablation de FA persistante(2).
C. Bars (Hôpital Saint-Joseph, Marseille) a démontré l’intérêt de l’ablation de la FA basée sur l’analyse visuelle de la dispersion spatio-temporelle à travers les résultats de l’étude Substrate HD(3) (figure 2), dans laquelle cette stratégie « sur mesure » avait permis d’arrêter la FA pendant la procédure chez 95 % des patients (77 % FA persistantes), et apparaissait supérieure à une stratégie par étapes (isolation VP ± lignes ± CFAE) malgré un temps d’ablation diminué et une surface relativement restreinte (10 % des 2 oreillettes) au terme d’un suivi de 18 mois (85 % des patients en rythme sinusal après 1,4 procédure en moyenne). Les éventuelles récidives se manifestent la plupart du temps sous la forme de tachycardies atriales plus faciles à ablater.
Figure 2. Mapping de la dispersion spatio-temporelle du signal guidant l'ablation d’après J. Seitz et coll. et A.S. Jadidi et coll.
Les concepts de fractionnement et de dispersion ont ensuite été redéveloppés dans les présentations de K. Nademanee (Los Angeles, USA ; Bangkok, Thaïlande) et de J. Kalifa (University of Michigan, USA). Le premier a insisté sur le fait que tous les potentiels fractionnés ne sont pas les mêmes et que la notion de dispersion permettait de sélectionner les potentiels fragmentés « actifs » cibles de l’ablation. Pour le second, l’existence de résultats discordants dans l’ablation des potentiels fractionnés dans la littérature pourrait s’expliquer par la stratégie d’ablation, qui semble plus efficace lorsque les potentiels sont regroupés en « patchs » (de dispersion temporo-spatiale) par rapport à des applications plus éparses (sur des potentiels fragmentés isolés le plus souvent « passifs »).
Aspects pratiques de l’ablation des arythmies atriales
Les différentes stratégies d’ablation de la FA paroxystique par cryothérapie (O. Thomas, Clinique Ambroise Paré, Neuilly), radiofréquence (S. Combes, Clinique Pasteur, Toulouse), mais aussi des tachycardies atriales (J.-P. Albenque, Clinique Pasteur & P. Maury, CHU Toulouse Rangueil) ont été présentées au cours de cette session ainsi que l’intérêt de l’« ablation index » (F. Halimi, Hôpital Privé, Parly 2), un nouvel outil plus fiable pour évaluer la profondeur des lésions d’ablation.
FA et insuffisance cardiaque
En préambule, É. Marijon (HEGP, Paris) a exposé les résultats de l’analyse des différentes causes de mortalité chez les patients de l’étude RELY, dominées par les morts subites et l’insuffisance cardiaque (37,4 % des décès). Les AVC et les complications hémorragiques des traitements (AVK ou dabigatran) ne représentaient que 9,8 % des décès. M. Anselmino (San Giovanni Battista Hospital, Turin) a, quant à lui, démontré l’intérêt de l’ablation de la FA chez les patients atteints d’insuffisance cardiaque. Celle-ci s’est avérée significativement plus efficace que l’amiodarone pour le maintien du rythme sinusal (objectif primaire) dans l’étude multicentrique randomisée AATAC(4) avec un bénéfice significatif sur un critère mixte associant mortalité et hospitalisation (objectif secondaire). La littérature montre, par ailleurs, une amélioration substantielle des symptômes d’insuffisance cardiaque/qualité de vie et de la FEVG après ablation chez les patients atteints de dysfonction systolique ventriculaire gauche, qui sont donc probablement les patients qui tirent le plus grand bénéfice de l’ablation (figure 3).
Enfin, K. Zannis (Institut Mutualiste Montsouris, Paris) a présenté une approche chirurgicale « mini-invasive » par voie cœlioscopique transdiaphragmatique couplée à une ablation endocavitaire en cours d’évaluation pour les FA persistantes de longue durée.
Figure 3. A. Évolution de la FEVG post-ablation de FA (Hsu et coll. NEJM 2004). B. Survie sans récidive d'arythmie dans AATAC (Di Biase et coll. Circulation 2016).
Anticoagulants
Au cours de cette session, É. Marijon a montré qu’il était raisonnable de poursuivre les AOD sans interruption chez les patients devant bénéficier d’une ablation puis G. Latcu (CH Princesse Grâce, Monaco) a soulevé la question de la pertinence de l’utilisation du score CHA2DS2-VASc à distance d’une ablation. Bien que certaines études semblent montrer une diminution du risque thromboembolique en cas d’efficacité de l’ablation, les recommandations qui suggèrent une période ferme d’anticoagulation de 2 mois puis une réévaluation basée sur ce score, devraient être appliquées en attendant plus de preuves.
En fin de journée, le concours d’e-posters a été remporté par I. Cazzoli (Royal Brampton, Londres) qui avait présenté une série d’ablations de TV chez 3 patients atteints de non-compaction VG dont une avait révélé un substrat épicardique.
Génétique
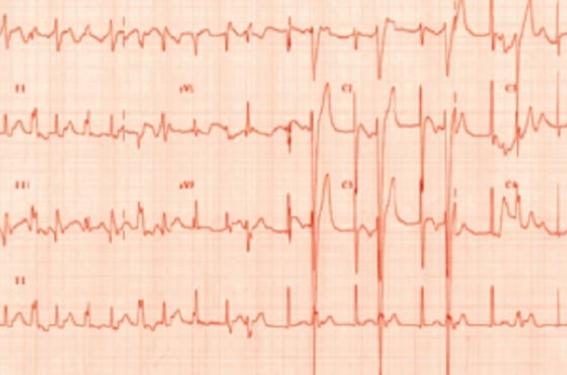
En ouverture, X. Waintraub (Hôpital de la Pitié-Salpêtrière, Paris) a illustré les difficultés de la prise en charge des syndromes de Brugada asymptomatiques. Au cours de la communication de G. Laurent (CHU de Dijon) sur les ESV en rapport avec des syndromes génétiquement déterminés, celui-ci a rappelé la nécessité d’évoquer et de rechercher des TV catécholergiques en cas d’aspect bimorphe/polymorphe et d’association avec l’effort. Dans le cas d’une diminution à l’effort, il faut évoquer des extrasystoles multifocales du Purkinje (ou MEPPC pour Multifocal Ectopic Purkinje-related Premature Contractions), syndrome décrit pour la première fois en 2012 en rapport avec une mutation du SCN5A exposant au risque de mort subite y compris dans l’enfance, et éventuellement de cardiomyopathie dilatée induite par les ESV. L’hydroquinidine (Serecor®) semble efficace à l’inverse de l’ablation (figure 4).
Figure 4. ECG d’un patient avec extrasystoles multifocales du Purkinje. (Courtoisie du Pr G. Laurent)
E. Gandjbakhch (CHU de la Pitié-Salpêtrière, Paris) a, quant à elle, évoqué les syndromes génétiques à dépister devant une mort subite et l’intérêt d’un dépistage systématique, y compris post-mortem et chez les apparentés, tandis que P. Charron (Hôpital Ambroise Paré, Boulogne) a présenté les déterminants génétiques des CMD, qui sont retrouvés jusque dans 50 à 75 % des présentations cliniques dans les dernières études et devraient être recherchées dans les formes familiales. Les résultats génétiques peuvent aider à stratifier le niveau de risque rythmique et donc aider la décision d’implantation de DAI en cas de mutation à haut risque (mutations du phospholamban, de la filamine-C, de la lamine). Un parallèle entre les syndromes de Brugada et de Wolff-Parkinson- White a ensuite été dessiné par C. Giustetto (San Giovanni Battista Hospital, Turin) : risque de mort subite, difficulté de stratification du risque chez les patients asymptomatiques et intérêt de l’ablation.
Enfin, dans une session consacrée aux problématiques du sport chez les patients porteurs de canalopathies, V. Probst (CHU de Nantes) a souligné l’importance d’une analyse individualisée prenant en compte les aspects psychologiques et la sévérité de l’atteinte. Globale ment, le risque reste faible et on peut le plus souvent autoriser une activité en dehors de la compétition.
Dispositifs
C. Israël (Bielefeld, Allemagne) a fait le point sur les dernières avancées dans le champ de la resynchronisation cardiaque : stimulation multipoint, stimulation VG endocardique, sélection des patients sans bloc de branche gauche (intérêt de prendre en compte PR long, déviation axiale, asynchronisme échographique).
Les nouveaux protocoles d’antibioprophylaxie en cours d’évaluation, les enveloppes antibactériennes, l’apport diagnostique de l’imagerie nucléaire et les données les plus récentes dans le domaine de l’extraction ont été abordés dans une présentation consacrée à la prise en charge des infections de dispositifs cardiaques implantés (É. Gitenay, Hôpital Saint-Joseph, Marseille).
Les données les plus récentes issues du suivi des patients appareillés de stimulateurs cardiaques sans sonde et de défibrillateurs sous-cutanés, ont été respectivement présentés par D. Klug (CHU de Lille) et M. Chauvin (CHU de Strasbourg). Un registre international multicentrique (726 patients) récemment publié(5) a prouvé l’efficacité à long terme (2 ans) du pacemaker sans sonde Micra® (Medtronic®) avec un risque de complication majeure à 12 mois de 4 %, soit une diminution de 48 % par rapport au stimulateur endoveineux, et une longévité espérée à 12 ans. Concernant les défibrillateurs sous-cutanés, plus de 27 000 prothèses ont été implantées dans le monde (> 1 700 en France). Les indications sont de plus en plus larges devant le faible taux de complication immédiate (2 %) et la fiabilité du dispositif (> 98,2 % d’efficacité avec plusieurs chocs). La nécessité d’une stimulation chez certains patients reste la contre-indication principale. Le rajout du filtre Smart- Pass® a permis de faire passer le taux de thérapies inappropriées de 8 à 4 % à 1 an.
N. Lellouche (Hôpital Henri Mondor, Créteil) a résumé les dernières études-recommandations concernant l’occlusion percutanée de l’auricule gauche. L’indication actuellement retenue par les sociétés savante est la contre-indication formelle aux anticoagulants oraux ou le refus de ce traitement chez les patients présentant de la FA avec une indication théorique d’anticoagulation. En France, le remboursement n’est disponible que pour les patients avec score CHA2DS2-VASc ≥ 4.
Les nouveaux dispositifs de monitoring du rythme cardiaque (patchs, smartphone) ainsi que leur bénéfice dans le bilan étiologique des AVC cryptogéniques ont été présentés par C. Bertrand (Hôpital Privé, Parly 2).
J. Taïeb (CH d’Aix-en-Provence) a clôturé la session par une mise à jour concernant la télécardiologie, dont l’intérêt n’est plus à démontrer pour le suivi des dispositifs cardiaques implantés, tant pour la surveillance de la batterie, des sondes, la réduction des thérapies inappropriées, l’optimisation de la resynchronisation et la détection précoce des arythmies atriales.
Tachycardie ventriculaire
P. Maury a rappelé les indications d’ablation devant une arythmie ventriculaire : en particulier, orage rythmique ou chocs appropriés sur TV monomorphe soutenue sur terrain ischémique. Plusieurs stratégies d’ablation ont été décrites et il existe désormais un consensus pour adjoindre un traitement « du substrat » en plus de la TV clinique dans les TV provenant d’une cicatrice d’infarctus. Compte tenu d’une efficacité désormais bien démontrée (supérieure à l’amiodarone), on peut s’attendre à une extension des indications (prophylactiques en cas de cicatrice d’infarctus ?). L’abord épicardique apparaît très utile dans les étiologies non ischémiques (notamment DAVD, myocardite).
L’intérêt du mapping à haute densité aux moyens de cathéters multipolaires avec une courte distance inter-électrode a ensuite été expliqué par F. Sacher (CHU de Bordeaux) : rapidité d’acquisition, évaluation plus précise du substrat/détection des LAVA, réduction du far-field. Le couplage de ce mapping à une imagerie intégrant l’épaisseur du myocarde est un outil très prometteur.
Les aspects spécifiques de l’ablation de TV dans les DAVD ont ensuite été abordés par G. Duthoit (Hôpital de la Pitié-Salpêtrière, Paris) avant qu’A. Bouzeman (Hôpital Privé, Parly 2) ne conclue la session avec la présentation des résultats préliminaires du registre multicentrique français d’implantation de DAI chez des patients atteints de tétralogie de Fallot.
Fibrillation ventriculaire
Au cours de cette session particulièrement intéressante, M. Haïssaguerre, encore une fois en pionnier, a démontré qu’il était possible de réaliser un mapping de fibrillations ventriculaires induites (comparablement à la FA !), avec la veste CardioInsight (Medtronic®, seul un outil de ce type permet un mapping « panoramique » en quelques secondes). Celui-ci permet de localiser des « drivers » nécessaires au maintien de l’arythmie, qui sont ensuite ciblés par l’ablation, avec des résultats très encourageants.
Puis K. Nademanee et J. Brugada (Barcelone) ont présenté leur expérience respective dans l’ablation épicardique au niveau de l’infundibulum ventriculaire droit chez les patients porteurs de syndrome de Brugada (figure 5). Selon ce dernier, l’aspect ECG typique doit exister ou être induit par perfusion d’antiarythmique de classe Ic au moment de la procédure. Les zones de bas voltage et d’allongement du potentiel sont alors recherchées et ablatées. L’expérience barcelonaise inclut 135 patients (dont 69 asymptomatiques initialement inductibles). L’ablation induit une modification électrique immédiate et fait ensuite disparaître l’aspect de Brugada (135/135) et l’inductibilité (133/135) dans la quasi-totalité des cas. Seuls 2 événements ventriculaires (dont 1 non soutenu à J1) sont signalés au cours du suivi.
Figure 5. A. Cartographie 3D d'une ablation épicardique du substrat chez un patient porteur d'un syndrome de Brugada (Courtoisie du Dr Nademanee). B. Aspect ECG et test à l'ajmaline avant et après ablation (Courtoisie du Pr Brugada).
La session francophone a été l’occasion de constater l’intérêt et le développement croissants de l’activité rythmologique en Afrique du Nord, au travers des témoignages d’orateurs venus de Tunisie, du Maroc et d’Algérie.
En pratique
La mort subite et l’insuffisance cardiaque sont les causes les plus fréquentes de mortalité chez les patients en FA. Dans l’étude AATAC où l’ablation s’était avérée supérieure à l’amiodarone, on constatait un bénéfice significatif sur le taux d’hospitalisation et la mortalité.
Plusieurs travaux récents semblent montrer l’intérêt des approches « sur mesure » pour l’ablation de la FA, notamment persistante. Celles-ci utilisent notamment l’analyse de la dispersion spatio-temporelle du signal électrique et la détection de zones de bas voltage (fibrose) détectable par l’IRM (rehaussement tardif).
Les anticoagulants oraux directs peuvent être maintenus sans interruption sécuritairement avant une ablation et doivent être maintenus sur la base du score CHA2DS2-VASc à distance.
Un dépistage génétique doit être réalisé systématiquement en cas de mort subite inexpliquée (cas index ou apparentés), mais aussi dans les formes familiales de CMD.
Le stimulateur sans sonde Micra (Medtronic®) et le défibrillateur sous-cutané (BostonScientific®) démontrent un profil de sécurité et d’efficacité très intéressant après plusieurs années de recul.
La survenue de choc approprié en rapport avec une TV monomorphe sur cicatrice d’infarctus doit faire discuter la réalisation d’une ablation, où un traitement du substrat doit être adjoint à celui de la TV clinique.
La fibrillation ventriculaire peut être « mappée » par un système de cartographie non invasif, en vue d’une ablation.
L’ablation de potentiels allongés sur le versant épicardique de la chambre de chasse ventriculaire droite chez les patients porteurs d’un syndrome de Brugada est un traitement qui semble prometteur, notamment chez les patients recevant des thérapies appropriées malgré la prise d’hydroquinidine.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :