HTA
Publié le 31 oct 2015Lecture 18 min
HTA résistante - Quelles stratégies diagnostiques et thérapeutiques ?
J. AMAR, Fédération de Cardiologie, CHU de Toulouse

Nous avons adopté la définition de l’hypertension résistante proposée par la Société française d’HTA(1). Il s’agit d’une HTA non contrôlée en consultation : PA ≥ 140/90 mmHg chez un sujet de moins de 80 ans, ou PAS ≥ 150 mmHg chez un sujet de plus de 80 ans et confirmée par une mesure en dehors du cabinet médical (automesure ou mesure ambulatoire de la pression artérielle), malgré une stratégie thérapeutique comprenant des règles hygiéno-diététiques adaptées et une trithérapie antihypertensive, depuis au moins 4 semaines, à dose optimale, incluant un diurétique.
Prévalence
Sa prévalence est estimée entre 20 et 30 %(2). Ce pourcentage augmente avec les facteurs de risque associés et l’atteinte des organes cibles. Elle est estimée chez le patient coronarien à 38 %(3) où elle est associée à un surcroît notable de risque de mortalité (risque relatif [RR] = 1,29 ; IC95% : 1,13-1,48), de mortalité cardiovasculaire (RR = 1,47 ; IC95% : 1,21-1,78), et d’accident vasculaire cérébral non fatal (RR = 1,61 ; IC95% : 1,17-2,22).
Stratégie diagnostique
Rechercher un effet blouse blanche
Cela repose sur la pratique d’une mesure ambulatoire de la pression artérielle (MAPA) ou d’une automesure tensionnelle (AMT). Les seuils de contrôle sont fixés à 130/80 mmHg pour la MAPA et 135/85 mmHg pour l’AMT.
Rechercher et améliorer des facteurs de résistance
L’observance dans la prise des traitements médicamenteux
- Dépister une mauvaise observance
Dans une étude observationnelle sur l’observance du traitement supposant le recueil d’un consentement conduite chez des patients présentant une hypertension résistante pour lesquels une dénervation rénale avait été envisagée, 56 % seulement des patients prenaient la totalité de leur traitement(4).
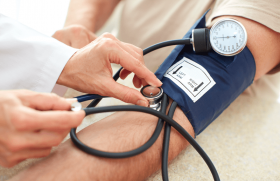
L’appréciation de l’observance est délicate et les erreurs d’appréciation sont nombreuses. On pourra s’aider du questionnaire à remplir par le patient en salle d’attente, disponible sur le site du Comité français de lutte contre l’hypertension artérielle mis au point par Xavier Girerd (figure).
- Améliorer l’observance
Le dialogue, l’information, la recherche des causes, en particulier des effets indésirables et l’aménagement du traitement en conséquence peuvent débloquer une situation. Il faut savoir aller au-devant d’un effet indésirable tel que la dysfonction érectile souvent attribuée aux médicaments antihypertenseurs. À cet égard, il faut rappeler la responsabilité indiscutable de la spironolactone dans la survenue d’une impuissance et l’absence d’élément de fort niveau de preuve soutenant l’imputabilité des bêtabloquants. Il faut aussi garder à l’esprit que la dysfonction érectile chez l’hypertendu traduit une dysfonction endothéliale indépendante du traitement et marqueur d’un risque cardiovasculaire élevé. Après analyse et éventuellement aménagement de l’ordonnance de l’hypertension artérielle, des solutions parfois médicamenteuses sont à envisager avec le patient pour améliorer sa qualité de vie.
Questionnaire à remplir par le patient en salle d’attente, disponible sur le site du Comité français de lutte contre l’hypertension artérielle mis au point par Xavier Girerd.
L’observance des mesures diététiques
- Dépister
Un régime trop salé (> 6 g de sel par jour) et une consommation excessive d’alcool (> 3 verres de vin pour l’homme et 2 pour la femme) peuvent être responsables de la résistance de l’HTA. Le dialogue permet leur dépistage. Des marqueurs biologiques peuvent être utiles. Une évaluation de la natriurèse des 24 heures permet d’avoir une estimation précise de la ration quotidienne en sel selon la formule suivante : apport en sel quotidien (g/j) = natriurèse des 24 h (mmol/l)/17. Le dosage des γGT et du volume globulaire moyen peut confirmer un soupçon. À cet égard, chez des patients souvent en surpoids, un bilan hépatique est de toute façon utile pour dépister une hépatite non alcoolique stéatosique.
- Améliorer
Concernant le sel, il faut centrer les conseils diététiques sur des points simples tels que la ration en pain, fromage, charcuterie. Plus largement, il faut insister sur des régimes de type méditerranéen qui ont démontré leur efficacité dans le cadre d’essais randomisés sur la réduction de la morbidité et de la mortalité cardiovasculaire ainsi que la pression artérielle.
Dépister dans les traitements associés des facteurs de résistance
- Les médicaments directement responsables d’une hausse de pression artérielle
• Les AINS : l’augmentation de la pression artérielle qu’ils provoquent est liée à une rétention hydrosodée. Les AINS sont prescrits par un praticien ou utilisés dans le cadre de l’automédication. Ils peuvent être responsables d’une hausse de pression artérielle quelle que soit leur voie d’administration : orale, injectable ou topique. Parmi leurs autres effets indésirables intéressant le cardiologue, on trouve les hémorragies digestives, l’hyperkaliémie, l’insuffisance rénale, l’insuffisance cardiaque, la thrombose artérielle. Il faut prévenir le patient hypertendu du risque associé à leur emploi et envisager avec le patient et son praticien les conditions de leur remplacement. Si leur utilisation est absolument nécessaire, leur emploi doit être encadré par des mesures de pres sion artérielle, des contrôles biologiques et des aménagements du traitement antihypertenseur.
• Les corticoïdes.
• La contraception estroprogestative : son impact hépatique sur la synthèse d’angiotensinogène serait associé à l’augmentation de la pression artérielle. Sa responsabilité est engagée quelle que soit la voie d’administration : orale ou vaginale. Elle doit être interrompue au profit d’un autre mode contraceptif. L’HTA sous pilule se transforme parfois en HTA maligne responsable notamment d’accident vasculaire cérébral ou d’insuffisance rénale. Elle ne doit pas faire méconnaître une HTA secondaire à une étiologie. Enfin ce paragraphe est l’occasion de rappeler que chez une patiente en âge de procréer, il vaut mieux éviter les IEC et les ARA2 compte tenu des insuffisances rénales et des malformations dont ils sont responsables chez le bébé. Si leur prescription est indispensable, il faut informer la patiente du risque de maintenir ce traitement pendant une grossesse, de la nécessité au mieux de les interrompre préalablement à la grossesse ou dès qu’elle se sait enceinte et à consulter alors son obstétricien.
• Les inhibiteurs de la recapture de la sérotonine et de la noradrénaline.
• Les alpha1-mimétiques tels que les vasoconstricteurs nasaux ou la midodrine utilisée dans l’hypotension orthostatique, en particulier associée à la dysautonomie. À cet égard, il ne semble pas opportun de faire figurer dans un traitement à la fois de la midodrine et un antihypertenseur. Pour lutter contre les paroxysmes tensionnels et l’hypertension nocturne associés à la dysautonomie, il faut préférer le passage en position assise ou debout et la surélévation des pieds soutenant la tête du lit.
• Les immunosuppresseurs : l’HTA est le fait de la famille des calcineurines : ciclosporine et tacrolimus. Cette HTA est caractérisée par une forte vasoconstriction intrarénale, une augmentation de l’activité sympathique, une expansion du volume intravasculaire et une suppression de l’activité rénine. Elle sera à prendre en charge en collaboration avec les spécialistes de la transplantation.
- Les médicaments interagissant avec les antihypertenseurs
Les inducteurs enzymatiques tels que les antiprotéases, la carbamazépine et la rifampicine sont susceptibles de compromettre de façon très significative l’efficacité d’un antihypertenseur à métabolisme hépatique tels les inhibiteurs calciques, les bêtabloquants à l’exception de l’aténolol, les ARA2, etc. Il faut, dans un contexte où ces médicaments sont indispensables, se reporter sur des médicaments antihypertenseurs à métabolisme exclusivement rénal tels que l’aténolol ou le lisinopril et accroître la posologie des inhibiteurs calciques.
Dépister la consommation de substances pressives
- La réglisse
Il faut interroger le patient sur une prise régulière de réglisse sous la forme de confiserie, d’antésite, de chewing-gum ou d’infusion. En effet, l’acide glycirrhizique inhibe l’enzyme en charge de la dégradation du cortisol au voisinage du récepteur de l’aldostérone. Dépourvu de cet enzyme, le récepteur de l’aldostérone va être stimulé de façon inappropriée par le cortisol induisant une HTA avec hypokaliémie associée à une rénine et une aldostérone plasmatique basses.
- Les substances illicites
Les substances stupéfiantes telles que la cocaïne, les amphétamines avec leurs nombreux dérivés comme la MDMA (méthylène- dioxyméthamphétamine ou ecstasy) sont de puissants sympathomimétiques responsables de paroxysmes tensionnels. Il faut savoir évoquer leur usage, même épisodique.
Syndrome d’apnée du sommeil (SAS)
Le diagnostic de SAS doit être évoqué chez un hypertendu résistant, ronfleur, asthénique le matin au lever, impuissant, sujet aux accidents de voiture ou affecté d’une somnolence diurne parfois invincible. Le diagnostic sera posé à l’aide d’un enregistrement polysomnographique du sommeil.
La présence d’un SAS prédit l’apparition de l’hypertension artérielle, une augmentation du risque de trouble du rythme cardiaque et de la morbi-mortalité cardiovasculaire.
La correction du SAS chez l’hypertendu est associée à une amélioration de la qualité de vie et une réduction de la PA proportionnelle à sa sévérité et à la qualité de sa correction. La réduction de PA à espérer est de l’ordre de 5 à 6 mmHg. On ne dispose pas à l’heure actuelle de démonstration fondée sur un fort niveau de preuve d’une amélioration du pronostic cardiovasculaire après correction du SAS. À noter la surmortalité cardiovasculaire et la surmortalité totale retrouvée chez les patients appareillés pour un SAS d’origine centrale dans le cadre d’une insuffisance cardiaque par syndrome d’apnée du sommeil (ESC 2015).
Chez les patients intolérants à l’assistance respiratoire nocturne, il faut envisager l’orthèse d’avancée mandibulaire, les traitements positionnels souvent pour l’heure mal tolérés (balle de tennis cousu dans le dos du vêtement de nuit, coussin dorsal). Récemment approuvé par le FDA, un pacemaker stimulant le nerf hypoglosse et agissant sur la langue. À noter que dans l’étude pivot récemment parue dans le New England Journal of Medicine, le taux d’effets indésirables liés à l’intervention était de 26 %. Le procédé paraît assez invasif…
Rechercher une étiologie
Une étiologie peut expliquer la résistance au traitement. L’histoire personnelle ou familiale du patient associé au bilan standard : kaliémie, créatininémie et étude du sédiment urinaire permettent la plupart du temps de les évoquer. Pour illustrer l’importance de l’interrogatoire et de ces examens simples, voici décrites brièvement des situations pouvant conduire au diagnostic étiologique.
HTA d’origine rénale ou artérielle rénale
- HTA évoluant dans un contexte d’infections urinaires à répétition pendant l’enfance
Le diagnostic à évoquer est celui d’une HTA supportée par une néphropathie interstitielle peut-être favorisée par un reflux vésico-urétéral. Le traitement va reposer sur l’utilisation d’un bêtabloquant qui sera préféré à un IEC ou un ARA2 si le contexte est celui d’une femme en âge de procréer et la recherche d’un reflux persistant ou controlatéral vésico-urétéral.
- HTA d’apparition brutale et d’emblée de haut degré précédée d’une crise douloureuse lombaire
Parmi les diagnostics possibles, figure celui d’une HTA rénovasculaire sur une dysplasie artérielle rénale compliquée de dissection. Un angioscanner des artères rénales permettra de confirmer le diagnostic, de situer le type de dysplasie et une éventuelle association à des lésions anévrismales, d’évaluer le retentissement sur le parenchyme rénal et d’envisager un traitement de la ou des artères impliquées.
- HTA résistante dans un contexte d’anomalie connue du sédiment urinaire dépisté à la médecine du travail ou par la médecine scolaire
Le diagnostic à évoquer est une HTA venant compliquer une néphropathie glomérulaire par exemple une maladie de Berger.
- HTA résistante dans un contexte d’insuffisance rénale sévère familiale
Il faut suspecter l’existence d’une HTA associée à une polykystose rénale ou de formes familiales de glomérulopathie.
- HTA brutalement déséquilibrée dans un contexte d’artériopathie des membres inférieurs
Une composante réno-vasculaire surajoutée doit être recherchée.
- HTA compliquée d’oedème aigu du poumon dans un contexte d’atteinte polyvasculaire
Cette histoire est évocatrice de sténoses volontiers bilatérales des artères rénales.
- HTA déséquilibrée associée à une insuffisance rénale dans les suites d’une coronarographie
L’histoire fait évoquer une maladie des emboles de cholestérol. L’inspection des pieds confirmera le diagnostic. Il faut en effet rechercher des orteils bleus évocateurs d’emboles de cholestérol déclenchés par le geste endovasculaire. L’ischémie rénale est à l’origine du déséquilibre de la pression artérielle et de l’altération du débit de filtration glomérulaire.
HTA d’origine surrénale
- HTA et hypokaliémie améliorées par la grossesse
Cette histoire fait évoquer un hyperaldostéronisme primaire supporté par un adénome de Conn. Le jeune âge de la patiente, la précocité de l’HTA, l’hypokaliémie, l’amélioration du tableau au cours de la grossesse à la faveur de l’effet antialdostérone de la progestérone peuvent argumenter ce diagnostic.
- HTA dans un contexte d’antécédent personnel et familial de cancer médullaire de la thyroïde
Le diagnostic à évoquer en priorité est celui d’un phéochromocytome évoluant dans le cadre d’une néoplasie endocrinienne multiple : maladie génétique associant volontiers cancer médullaire de la thyroïde, phéochromocytome et hyperparathyroïdie. Le diagnostic d’HTA associée à un phéochromocytome s’inscrivant dans le cadre d’une maladie génétique doit être évoqué devant des antécédents personnels ou familiaux de phéochromocytome ou de maladie génétique tels que la maladie de von Hippel Lindau ou de neuro-fibromatose.
- HTA réfractaire associée à une tendance discrète à l’hypokaliémie, à une prise de poids et à une modification de l’aspect du visage
Il faut suspecter un hypercortisolisme. Dans le contexte d’HTA résistante, il est fondé de faire cette hypothèse même en l’absence de signes morphologiques : on connaît en effet une proportion importante de Cushing dit « infraclinique ».
HTA d’origine aortique
- HTA connue depuis l’adolescence avec des pouls fémoraux faibles ou absents
Il faut suspecter une coarctation aortique. Le diagnostic sera confirmé par l’écoute d’un souffle systolique interscapulaire.
- HTA réfractaire et antécédent de dissection aortique
Il faut suspecter soit une atteinte artérielle rénale par extension de la dissection, soit une hypoperfusion d’un ou des deux reins par compression dynamique du chenal perfusant les reins par l’autre chenal.
- HTA réfractaire dans un contexte d’artériopathie des membres inférieurs sans sténose des artères rénales
Il faut évoquer une obstruction aortique sus-rénale, volontiers par un bouchon calcaire.
HTA d’origine neurologique
- HTA associée à des paroxysmes de pression artérielle et une hypotension orthostatique chez un patient indemne d’atteinte médullaire traumatique
Après avoir éliminé le phéochromocytome, il faut envisager le diagnostic de dysautonomie par maladie neurodégénérative. Le diagnostic est aisé s’il s’agit d’un patient atteint de maladie de Parkinson ou d’un diabète. Il faut envisager un syndrome paranéoplasique, notamment un cancer bronchique surtout en cas de tabagisme.
Cette liste de situations ne prétend pas à l’exhaustivité. Elle illustre l’importance de l’interrogatoire dans la recherche d’une étiologie. Une fois l’étape de l’interrogatoire appuyé sur le bilan minimal (créatininémie, kaliémie et bandelette urinaire) franchi, pour confirmer un diagnostic suspecté et/ou poursuivre l’enquête, on peut envisager comme examens complémentaires à la recherche d’une participation réno-vasculaire : un échographie Doppler des artères rénales et des reins, un angioscanner des artères rénales ou une angio- IRM selon les antécédents allergiques du patient, sa fonction rénale, les risques d’irradiation répétée. Au plan surrénalien, un dosage de rénine et d’aldostérone en position assise à l’abri des interférences médicamenteuses est à envisager, un dosage de métanéphrines, normétanéphrines urinaires à partir d’un recueil urinaire sur 24 heures, un test de freination de la synthèse de cortisol après administration à minuit de 1 mg de dexaméthasone. Un enregistrement polygraphique du sommeil selon le contexte peut être convoqué pour dépister un syndrome d’apnée du sommeil.
Stratégie thérapeutique
Analyser le traitement de l’hypertendu résistant en dehors du contexte de l’HTA secondaire
Le patient reçoit-il une trithérapie avec diurétique ?
En référence aux recommandations françaises, une hypertension artérielle est définie comme résistante si l’objectif de PA de consultation n’est pas atteint malgré une stratégie thérapeutique comprenant des règles hygiéno-diététiques adaptées et une trithérapie antihypertensive, depuis au moins 4 semaines, à dose optimale, incluant un diurétique. Il est difficile de définir ce qu’est une posologie optimale de diurétique. Concernant les diurétiques thiazidiques, on rappellera en référence aux résumés caractéristiques des produits qu’ils font l’objet d’une contreindication absolue en cas d’insuffisance rénale sévère (Clcr < 30 ml/min). Par ailleurs, la posologie maximale d’hydrochlorothiazide selon l’autorisation de mise sur le marché de l’Esidrex® est de 25 mg par jour avec la mention sur les résumés caractéristiques du produit : « La posologie ne doit pas dépasser 25 mg/jour (augmentation des effets indésirables sans gain d’efficacité) ». Cependant des spécialités comme le Moduretic® ont une autorisation de mise sur le marché permettant l’administration de 50 mg d’hydrochlorothiazide couplé à 5 mg d’amiloride.
Concernant l’indapamide, la posologie maximale décrite est de 2,5 mg par jour sous forme pelliculée et dans la galénique à la libération prolongée, elle est de 1,5 mg par jour.
Le furosémide : son emploi chez l’hypertendu est limité aux contre-indications des thiazidiques. Voici un extrait du libellé des RCP de cette molécule concernant son indication et sa posologie dans l’hypertension artérielle : « Hypertension artérielle chez le patient insuffisant rénal chronique, en cas de contre-indication aux diurétiques thiazidiques (notamment lorsque la clairance de la créatinine est inférieure à 30 ml/min) », « Hypertension artérielle chez l’insuffisant rénal chronique : en association aux autres traitements antihypertenseurs (notamment les antagonistes du système rénineangiotensine), les doses usuelles recommandées sont de 20 mg par jour à 120 mg par jour en une ou plusieurs prises par jour ».
HTA résistante chez un patient traité par une trithérapie avec diurétique
- Que faire lorsque la posologie de diurétique ne peut être optimisée du fait d’une tendance à l’hypokaliémie
• Sécuriser le traitement. Il faut rechercher la coprescription de médicaments potentialisant le danger de l’hypokaliémie. En pratique, on recherchera des médicaments allongeant le QT. Parmi les médicaments cardiologiques, il faut prendre en compte l’utilisation d’antiarythmique de classe I tel que la flécaïnide et de classe III tel que le sotalol. Le cardiologue doit ensuite étendre son regard à l’ensemble de l’ordonnance et rechercher la coadministration de macrolides, quinolones et neuroleptiques pour les plus fréquents. C’est l’occasion de souligner la présence fréquente dans le traitement au long cours des patients affectés de bronchite chronique obstructive post-tabagique d’un macrolide : l’azithromycine en raison des effets favorables d’une administration chronique sur la fréquence des exacerbations. C’est aussi l’occasion de rappeler au cardiologue la contre-indication absolue à l’association macrolide- colchicine, notamment en raison du risque cardiaque.
La découverte d’une hypokaliémie dans ce contexte de coprescription doit conduire à des mesures diagnostiques et correctrices immédiates : ECG, modification du traitement, correction de l’hypokaliémie.
• Réduire les apports en sel.
Les échanges NA/K au niveau du tube contourné distal sont corrélés à la quantité de sodium qui y parvient et donc à la ration en sel. Ainsi, il faut insister sur l’intérêt de réduire les apports en sel pour faciliter la correction de l’hypokaliémie.
• Envisager l’adjonction d’un diurétique d’épargne potassique au traitement thiazidique. On dispose de deux diurétiques d’épargne potassique : l’amiloride et la spironolactone.
La spironolactone a une action antihypertensive et hyperkaliémiante par blocage de l’action de l’aldostérone. Il faut prendre en compte dans l’évaluation bénéfice/risque de la spironolactone la survenue fréquente d’effets indésirables dose-dépendants incompatibles avec une poursuite au long cours chez l’homme : gynécomastie ou impuissance et à un moindre degré chez la femme : mastodynie, métrorragies. Concernant le risque de cancer du sein et l’utilisation au long cours de spironolactone, il faut signaler qu’une alerte sur le risque tumorigène figure sur les boîtes de ce médicament aux États-Unis. Un large essai sur les bases de données de l’Assurance maladie conduit en Grande-Bretagne a fourni des informations rassurantes en prévention primaire. En prévention secondaire du cancer du sein, il y a incertitude. La spironolactone est contre-indiquée en cas d’insuffisance rénale.
Concernant l’amiloride, elle agit sur le canal ENAC, responsable d’une réabsorption de sodium au niveau du tube contourné distal et d’une excrétion de potassium. L’ouverture de ce canal ENAC est régulée par l’aldostérone. L’effet de l’amiloride sur la pression artérielle en particulier dans l’HTA à rénine basse a été démontré dans l’étude PATHWAY3. Elle n’a pas les effets hormonaux de la spironolactone et n’entraîne pas de gynécomastie ou d’impuissance de façon dosedépendante. En France, sa posologie s’échelonne en référence aux résumés caractéristiques du produit de 5 mg/jour à 20 mg/jour. L’amiloride est contre-indiqué en cas d’insuffisance rénale.
- Que faire lorsque l’utilisation d’un diurétique à posologie optimale est rendue difficile par une tendance à l’hyponatrémie
Tous les diurétiques, en raison de leur mode d’action, c’est-à-dire augmenter la natriurèse, favorisent l’hyponatrémie. Les thiazidiques, dans la mesure où ils négativent la clairance de l’eau libre, ont un effet hyponatrémiant plus important que les diurétiques de l’anse.
L’hyponatrémie, en particulier chez la personne âgée, est associée à une asthénie, des vomissements, une confusion.
• En premier lieu, il faut rechercher un facteur iatrogène.
De nombreux médicaments favorisent l’hyponatrémie par sécrétion inappropriée d’hormone antidiurétique. IL faut notamment citer la carbamazépine et les inhibiteurs de la recapture de la sérotonine. Un dialogue avec le neurologue et le psychiatre doit être noué pour situer les possibilités de substitution.
• Ensuite, en l’absence de facteur iatrogène, il faut rechercher un SIADH, notamment d’origine néoplasique.
Cette recherche peut se faire avec le concours d’un praticien spécialisé dans l’exploration fonctionnelle rénale. Le traitement de la cause peut permettre la correction de l’hyponatrémie.
- Que faire chez le goutteux
La prescription sans précaution de diurétique chez un patient à l’antécédent de goutte fait courir un risque de réactivation du rhumatisme inflammatoire. Il faut donc anticiper avec le rhumatologue ou le médecin généraliste en utilisant plusieurs semaines avant l’introduction du diurétique des hypo-uricémiants sous couvert de colchicine après avoir soigneusement éliminé les contre-indications à cette stratégie et en prenant notamment en compte les interactions médicamenteuses avec la colchicine.
- Que proposer chez l’hypertendu résistant à une trithérapie comprenant une posologie optimisée de diurétique
• Stratégie proposée par les recommandations.
Elle consiste en l’ajout de 25 mg de spironolactone. À cette posologie, l’étude ASPIRANT démontre une réduction significative mais de faible ampleur de la pression artérielle systolique d’environ 5 mmHg. On ne mettra pas en oeuvre cette stratégie en cas d’insuffisance rénale ou d’hyperkaliémie. Il faut recueillir l’accord du patient après l’avoir informé des effets indésirables possibles : gynécomastie et impuissance chez l’homme, mastodynie et ménorragies chez la femme. Il faut encadrer cette stratégie d’une surveillance biologique renforcée de la kaliémie, de la créatininémie et de la natrémie.
• Autres stratégies possibles pour lesquelles on dispose de données dans la littérature.
- Association d’un inhibiteur calcique bradycardisant à un inhibiteur calcique appartenant à la famille des dihydropyridines.
Un essai randomisé a testé cette stratégie(5) et a démontré sur une courte série de patients une réduction d’environ 10 mmHg au pic d’action sur des données MAPA dans le bras testant la combinaison diltiazem plus nifédipine comparé à nifédipine seule. Les effets indésirables à redouter sont surtout les oedèmes des membres inférieurs. Il faut éviter l’association de cette stratégie à un alphabloquant compte tenu d’un risque majeur d’hypotension orthostatique.
- Blocage séquentiel du néphron.
Il s’agit d’associer à la trithérapie classique : bloqueur du système rénine angiotensine, inhibiteur calcique et diurétique thiazidique, un diurétique de l’anse et de la spironolactone. Dans l’HTA résistante cette stratégie a été testée par Bobrie et coll. dans un essai randomisé. En référence à un bras comparateur, une réduction de 10 mmHg a été obtenue. Cette stratégie visant à empêcher la réabsorption sodée à 3 niveaux du néphron a comme principal risque l’hyponatrémie, les désordres kaliémiques et la déshydratation. L’éducation du patient sur la nécessité d’interrompre le traitement en cas de diarrhées profuses, d’impossibilité de s’alimenter est plus que jamais nécessaire. Une surveillance biologique attentive doit aussi être installée.
- Place de la dénervation rénale ou de la stimulation du barorécepteur.
Dans l’essai randomisé avec double aveugle et bras contrôle SYMPLICITY 3(6), la dénervation rénale n’a pas démontré plus d’effet que le placebo. Elle n’a donc pas de place dans le traitement de l’HTA résistante. Son emploi relève du domaine de la recherche. Dans l’essai randomisé avec aveugle(7) mené avec la stimulation du barorécepteur carotidien, ce dispositif n’a pas démontré de différence sur le critère primaire par rapport au bras contrôle. Son emploi relève du domaine de la recherche.
En pratique
L’hypertension résistante est fréquente. Elle exige pour en reconnaître les causes un interrogatoire et un maniement précis des combinaisons d’antihypertenseurs, notamment des diurétiques ou des inhibiteurs calciques.
Pour cela, une lecture attentive de la totalité de l’ordonnance, une surveillance biologique et l’information — au mieux l’éducation — du patient sont nécessaires.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :