Publié le 15 mar 2017Lecture 8 min
Reste-t-il une place pour les tests biologiques visant à évaluer l’efficacité des antiplaquettaires ?
Pascale GAUSSEM, Université Paris Descartes, AP-HP, Hôpital européen Georges Pompidou, service d’hématologie biologique ; UMR S 1140 (Inserm), Faculté de pharmacie
Comment définir objectivement les circonstances dans lesquelles une surveillance biologique de l’efficacité des médicaments antiplaquettaires peut être proposée ? C’est l’objectif de cette brève revue.
Surveillance des anti-P2Y12
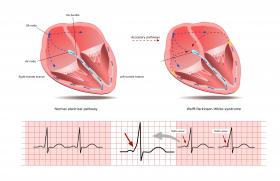
Depuis une quinzaine d’années, nombre d’études biologiques ont prouvé qu’environ 30 % des patients sous clopidogrel 75 mg/j sont mauvais répondeurs au traitement en termes d’inhibition des fonctions plaquettaires. Les principaux tests utilisés sont des tests en sang total « point-of care » (VerifyNowP2Y12®, Multiplate®, etc.) et l’agrégation plaquettaire en plasma riche en plaquettes (ou LTA : « light transmission aggregation »), utilisant l’ADP comme agoniste (figure 1). Ces tests sont à réaliser extemporanément. Il existe, en outre, un test spécifique de la voie de signalisation du récepteur P2Y12. Il s’agit de la mesure du taux de phosphorylation de la protéine VASP, test réalisé par cytométrie en flux dans les 48 heures suivant le prélèvement. Quel que soit le test utilisé, la « résistance biologique » expose à un risque accru d’événements cardiovasculaires (odd ratio = 8)(1).
Figure 1. Signalisation simplifiée du récepteur à l’ADP P2Y12, cible du clopidogrel, prasugrel, ticagrelor et positionnement des principales méthodes d’exploration biologique de l’activité de ces molécules.
Le test VASP est un test spécifique de la voie de l’AMP cyclique, réalisé par cytométrie en flux, nécessitant donc un équipement technique particulier. Les tests d’agrégation plaquettaire sont soit réalisés en plasma riche en plaquettes (méthode de référence) en utilisant l’ADP comme agoniste, soit en sang total réalisables au lit du patient (VerifyNowP2Y12®, Multiplate®, etc.). Est présenté le profil d’agrégation à l’ADP 10 μM d’un sujet « bon répondeur » avant (courbe verte, agrégation 88 %) et après 7 jours de clopidogrel 75 mg (courbe jaune, agrégation 27 %). Le trait pointillé signale l’inhibition de l’adénylate cyclase lors de l’activation du récepteur P2Y12 par l’ADP et la diminution concomitante de la synthèse d’AMPc, conduisant à la déphosphorylation de VASP et à l’agrégation plaquettaire.
Pour augmenter la production du métabolite actif du clopidogrel, plusieurs études ont essayé une escalade de dose. En angioplastie programmée, Bonello et coll. ont administré plusieurs bolus de 600 mg de clopidogrel à 24 heures d’intervalle jusqu’à obtention d’une réponse biologique efficace, ce qui s’est traduit par un taux significativement plus faible d’événements cardiovasculaires à 30 jours(2). Toutefois, deux grandes études prospectives d’adaptation de dose à la biologie (VerifyNow) conduites chacune sur plus de 2 000 patients avec angioplastie coronaire et pose de stent (études GRAVITAS et ARCTIC) n’ont pas permis de montrer un bénéfice clinique de l’adaptation posologique sur la récidive de syndrome coronarien aigu (SCA), de thrombose de stent ou de décès respectivement à 1 mois(3) ou à 1 an, avec un risque hémorragique identique(4). Ceci va contre une recommandation d’adaptation de dose généralisée. Récemment, des résultats similaires ont été publiés chez des patients âgés de plus de 75 ans recevant 5 mg/jour de prasugrel, thiénopyridine de 3e génération, pour laquelle des cas de résistance sont également rapportés(5).
Le tableau résume les principales circonstances au cours desquelles nous pouvons être sollicités en tant que biologistes pour une évaluation de l’effet antiplaquettaire (hors protocoles).
Au cours du SCA, l’utilisation du ticagrelor en première intention a rendu caduque toute recommandation d’adaptation posologique, compte tenu de l’efficacité de la molécule.
En revanche, pour les patients sous clopidogrel au long cours, plusieurs situations physiopathologiques peuvent conduire à une résistance biologique comme l’insuffisance rénale, l’âge avancé, l’inflammation, le diabète de type 2(6).
En outre, nos travaux ont montré que l’allèle 2C19*2, polymorphisme génétique fréquent touchant 25 à 30 % des sujets, est significativement associé à une diminution de la sensibilité au clopidogrel(7). Ce variant code une enzyme CYP2C19 de type « perte de fonction » intermédiaire chez les hétérozygotes mutés et totale chez les homozygotes mutés, qui interfère sur la conversion de la pro-drogue clopidogrel en métabolite actif. D’autres variants comme 2C19*17 « gain de fonction » modulent l’effet du variant 2C19*2 et influencent la réponse au clopidogrel. Les sujets peuvent ainsi être classés selon leur génotype en métaboliseurs « ultra-rapides » à métaboliseurs « lents »(8). Récemment, des variants situés dans d’autres gènes ont été rapportés et modulent également cette réponse. Tout comme les tests d’agrégation, l’analyse génétique est actuellement réservée à des patients ciblés.
La connaissance du génotype permet une thérapeutique personnalisée.
Ainsi, le doublement des doses de charge et d’entretien de clopidogrel permet d’obtenir une réponse biologique chez certains sujets, sauf chez les homozygotes mutés 2C19*2*2(9,10) chez qui une alternative thérapeutique doit être envisagée. Par ailleurs, la description du rôle du CYP2C19 dans le métabolisme du clopidogrel a été le rationnel de l’analyse de l’influence de l’interaction avec les substrats/inhibiteurs de cet isoforme, notamment les inhibiteurs de pompes à protons (principalement omeprazole et lansoprazole).
Le panel des tests d’évaluation biologique des anti-P2Y12 a permis également d’analyser le risque hémorragique associé à la réponse antiplaquettaire. Ainsi, des données obtenues chez plus de 2 500 patients sous clopidogrel ont rapporté une corrélation entre événements hémorragiques et inhibition plaquettaire(11). Il en est de même pour le prasugrel(12) et pour le ticagrelor(13,14). Ces données pourraient justifier une surveillance biologique pour certains patients « fragiles », que ce soit à risque thrombotique ou hémorragique afin de procéder à une adaptation du traitement. Ils permettent également de mesurer l’efficacité potentielle des traitements de substitution en cas de syndrome hémorragique avéré(14).
Surveillance de l’aspirine
L’aspirine inhibe la voie métabolique de l’acide arachidonique par acétylation irréversible de la cyclooxygénase 1 (COX1) plaquettaire. Elle inhibe par conséquent la synthèse du thromboxane A2 (TxA2), puissant agent vasoconstricteur et agrégant plaquettaire, et ce pendant la durée de vie de la plaquette. Ceci s’observe très rapidement par l’inhibition de l’agrégation plaquettaire induite par l’acide arachidonique en 5 min après dose de charge intraveineuse et environ 20 min après administration orale.
La grande hétérogénéité à propos de la résistance biologique à l’aspirine vient de la diversité des tests utilisés pour mesurer l’effet de l’aspirine sur les plaquettes. Les tests considérés comme les plus spécifiques sont le test d’agrégation plaquettaire en présence d’acide arachidonique et le dosage du TxB2, métabolite du TxA2, dans le sérum (figure 2). Certains des autres tests sont indépendants du TxA2, tel le test PFA100®, et ne doivent pas être utilisés pour mesurer l’effet de l’aspirine. Il est ainsi retrouvé un taux de «résistance » allant de 1 à plus de 50 % selon les études et les méthodes d’étude utilisées(15). Même le dosage du TxB2 urinaire donne des résultats discutables, car ce taux reflète la production totale de TxA2 in vivo, COX1 et COX2-dépendante.
Figure 2. L’aspirine, en inhibant irréversiblement la cyclooxygénase-1 (COX1) empêche la conversion de l’acide arachidonique en endoperoxydes puis en thromboxane A2 (TXA2). Le métabolite stable du TXA, le TXB2, dosé par méthode ELISA dans le sérum, permet d’évaluer la pharmacodynamie de l’aspirine. Les tests d’agrégation plaquettaire utilisent l’acide arachidonique (AA) comme agoniste. Les courbes d’agrégation d’un sujet sous 100 mg d’aspirine montrent une inhibition quasi complète de l’agrégation à l’AA 1,5 μM et le manque de spécificité du test quand l’ADP est utilisé comme agoniste (ici présenté à 5, 10 et 20 μM).
Toutefois, les tests mettant en évidence une « résistance biologique » définie généralement par un pourcentage d’agrégation plaquettaire induite par l’acide arachidonique supérieur à 20 %, sont globalement associés à un risque de récidive ischémique(16).
La principale cause de nonréponse à l’aspirine est de loin une mauvaise observance, qui peut atteindre 40 % des sujets. Il existe des cas d’échec thérapeutique chez des patients « biologiquement » répondeurs, pour lesquels une alternative thérapeutique doit être trouvée. Une des causes les plus fréquentes de diminution d’activité de l’aspirine est l’administration concomitante d’anti-inflammatoires non stéroïdiens (AINS), qui bloquent de façon réversible la COX1, et empêchent l’aspirine de se lier sur le site actif de la COX1.
En cas de nécessité de traitement par un AINS, il convient de l’administrer quelques heures après l’aspirine.
Des données récentes mettent en évidence une résistance biologique à l’aspirine administrée en 1 prise/jour dans des pathologies accompagnées d’un renouvellement accéléré des plaquettes. Il s’agit notamment du diabète de type 2, ou de la thrombocytémie essentielle. Il a été montré qu’un fractionnement avec ou sans doublement de la dose permettait de pallier cette résistance dans la plupart des cas(17,18).
Le concept de la spécificité pour l’aspirine des tests dépendant de l’acide arachidonique est actuellement discuté et inversement pour ceux dépendant de l’ADP dans la surveillance des anti-P2Y12. Notre équipe et d’autres ont montré en effet que les anti-P2Y12 interfèrent avec l’agrégation induite par l’acide arachidonique chez les sujets sous bithérapie(19). Inversement, l’aspirine intervient dans les tests d’agrégation dépendant de l’ADP mesurant l’effet des anti-P2Y12, sans toutefois interférer avec le test spécifique VASP(20). Ceci s’explique aisément par la notion que le récepteur P2Y12 a été impliqué dans la synthèse de TxA2. Par ailleurs, des notions récentes tentent d’expliquer pourquoi des patients avec inhibition totale de la génération de TxA2 ont une persistance de l’agrégation à l’acide arachidonique. Il serait possible que, chez certains patients, des voies du métabolisme de l’acide arachidonique indépendantes de la COX1 et donc non inhibées par l’aspirine (dont celle de la 12-lipoxygénase), conduisent à la synthèse de métabolites pro-agrégants. Ces hypothèses seront certainement validées dans les prochaines années.
En pratique
Le développement de la biologie comme méthode de surveillance des antiplaquettaires a permis d’expliquer les causes génétiques et non génétiques de résistance à ces molécules, ainsi que la gestion ciblée de patients à haut risque de thrombose ou d’hémorragie.
Plus en amont, elle permet de mieux évaluer la pharmacologie des antiplaquettaires, autorisés depuis des décennies comme l’aspirine ou en développement, pour améliorer la prise en charge des patients.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :