Rythmologie et rythmo interventionnelle
Publié le 15 fév 2017Lecture 7 min
Conduite à tenir devant un syndrome de Brugada asymptomatique
Nicolas LELLOUCHE et Philip AOUATE, Paris et Creil
Le syndrome de Brugada, décrit en 1992 par les frères Brugada(1), correspond à une pathologie pure de l’électricité cardiaque du ventricule droit qui prédispose les patients à la survenue de trouble du rythme ventriculaires graves de type tachycardie ventriculaire (TV) ou fibrillation ventriculaire (FV) pouvant aboutir à un arrêt cardio-respiratoire. La prévalence de cette pathologie est estimée à 0,1-0,7 % de la population adulte et est encore plus rare chez l’enfant (0,01 %). Il s’agit, par ailleurs, d’une maladie à nette prédominance masculine (10 hommes pour 1 femme). Le problème de cette anomalie électrocardiographique est que, d’une part, l’aspect électrocardiographique est variable dans le temps pour un même patient et, d’autre part, que le risque de mort subite est difficile à évaluer surtout chez les patients asymptomatiques.
Différencier le syndrome de Brugada spontané ou induit
Dans le cadre d’un syndrome de Brugada, il convient d’abord de différencier les 3 aspects électrocardiographiques possibles (figure 1). Tout d’abord il est recommandé, pour sensibiliser le diagnostic, de placer en plus des dérivations standards, des électrodes V1 et V2 hautes au niveau du 3e, voire 2e espace intercostal. On distingue ainsi le type 1 dit aspect en « dôme » avec une ascension du point J d’au moins 2 mm dans les dérivations V1 et/ou V2. Le type 2 dit aspect en « selle » est associé à un sus-décalage du point J d’au moins 2 mm dans les dérivations V1 et/ou V2. Enfin le type 3 correspond à un aspect en dôme ou en selle avec une ascension du point J < 2 mm.
Figure 1. Cette figure montre les 3 types électrocardiographiques du syndrome de Brugada : le type 1 avec aspect en dôme et élévation du segment ST ≥ 2 mm ; le type 2 avec l’aspect en selle et élévation du segment ST ≥ 2 mm ; le type 3 avec aspect en dôme ou en selle et ST < 2 mm. À noter que ces aspects peuvent être variables dans le temps chez un même patient.
Le diagnostic de syndrome de Brugada en tant que tel correspond à l’aspect de type 1 à l’ECG.
Il est aussi possible de sensibiliser le diagnostic chez des patients présentant un aspect de type de 2 ou 3 grâce à un test pharmacologique consistant à injecter un antiarythmique de classe Ic le flécaïnide ou I’ajmaline. Si l’ECG montre un aspect de type 1 au cours du test le patient est considéré comme ayant un syndrome de Brugada « induit ». Nous considérerons donc seulement les patients avec un type 1 spontané ou induit.
Être sûr que le patient est asymptomatique
Pour considérer qu’un patient présentant un syndrome de Brugada est asymptomatique, il faut exclure les symptômes associés à cette pathologie :
Le premier et le plus important est celui d’un arrêt cardio-respiratoire. Il s’agit du symptôme qui augmente le plus le risque de mort subite (récidive) chez un patient porteur de Brugada. Le deuxième symptôme est la syncope. Dans ce cadre, il est important de noter que l’interrogatoire est fondamental pour orienter vers une origine cardiologique : début et fin brusque, plus souvent nocturne (les morts subites au cours de ce syndrome sont le plus souvent nocturnes du fait de l’activation vagale qui aggrave cette pathologie), parfois il peut s’agir de syncope compliquée de crise convulsive (respiration agonique nocturne)…
Ce qui complique le diagnostic est qu’il s’agit souvent de patients jeunes et il a été montré que les patients porteurs de syndrome de Brugada font plus souvent des malaises vagaux que la population générale(2). Ainsi s’il existe un doute, il convient de pousser les investigations notamment avec un tilt-test (pour diagnostiquer une syncope vaso-vagale), de mettre un Holter de longue durée pour enregistrer une arythmie ventriculaire ou éventuellement de réaliser une stimulation ventriculaire programmée (SVP). Les symptômes en rapport avec un syndrome de Brugada sont hautement associés au risque de mort subite chez ces patients.
Valeur de la SVP
La stimulation ventriculaire programmée consiste à stimuler le ventricule droit pour essayer de déclencher une arythmie ventriculaire avec l’idée que les patients porteurs de syndrome de Brugada sont plus susceptibles de déclencher une TV ou une FV. Ceci est vrai puisque qu’on estime que chez ces patients en globalité, on induit une arythmie ventriculaire grave dans 20-30 % des cas ; cependant ce chiffre diminue à 10 % chez les patients asymptomatiques. Ainsi la valeur prédictive positive de cet examen est relativement médiocre de l’ordre de 20 % et la valeur prédictive négative est bonne (98 %) mais n’est pas de 100 %(3).
Il semble donc que le risque de trouble du rythme ventriculaire soit plus élevé chez les patients avec une SVP positive mais que cet examen, seul, ne permette pas de porter l’indication d’implantation d’un DAI par exemple ou de rassurer définitivement le patient sur son risque de mort subite(4).
Autres critères associés à une mort subite
Il faut noter que les patients avec un type 1 spontané ont un risque de mort subite plus élevé que les patients avec un type 1 induit. Les patients symptomatiques sont aussi plus à risque que les patients asymptomatiques. Si le patient présente un type 1 spontané asymptomatique le risque de mort subite annuel est estimé à 0,5 %(5,6). Il s’agit donc d’un risque faible mais qui n’est pas nul.
D’autres facteurs de risque de mort subite ont été décrits :
- allongement du délai pic de l’onde T-fin de l’onde T (marqueur de dispersion de repolarisation)(7) ;
- potentiels tardifs positifs ;
- majoration du segment ST en phase de récupération au cours d’une épreuve d’effort ;
- fragmentation du QRS (figure 2) ;
- QRS larges
- présence d’une repolarisation précoce associée ;
- patient faisant aussi de la FA ;
- prolongation de l’espace PR.
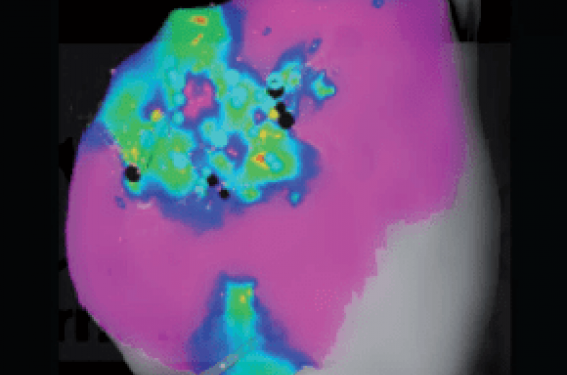
Figure 2. Tirée de l’article Brugada et al.(13) (Circ Arrhythm Electrophysiol 2015 ; 8 : 1 373-81), cette figure montre la présence de potentiels fragmentés en rythme sinusal au niveau de l’infundibulum pulmonaire chez des patients porteurs de syndrome de Brugada. Ces potentiels sont ablatés avec une normalisation de l’électrocardiogramme par la suite.
Cependant tous ces facteurs pris isolément ne sont pas suffisamment puissants pour pouvoir influer sur la décision thérapeutique à prendre chez nos patients asymptomatiques. Ainsi, une prise en compte globale de tous ces facteurs semble nécessaire pour pouvoir stratifier, au cas par cas, les patients présentant un syndrome de Brugada asymptomatique.
Enfin il est à noter que les antécédents familiaux de mort subite ainsi que la présence d’une mutation génétique (gène SCN5A) n’ont pas été retrouvés comme des facteurs associés à un sur-risque de mort subite(8).
Traitement possible chez le patient asymptomatique
Les mesures dans la vie quotidienne : chez un patient porteur d’un syndrome de Brugada, il convient de proposer systématiquement quelques mesures simples visant à prévenir la survenue de trouble du rythme : éviter de prendre des médicaments aggravant ce syndrome (liste à donner au patient ; http//www.brugadadrugs.org), éviter de boire trop d’alcool ou des repas trop lourds (pour éviter une trop forte stimulation vagale), traiter une fièvre et consulter en cas de malaise ou perte de connaissance. Enfin un ECG systématique doit être proposé aux parents du premier degré du patient.
Pour un patient asymptomatique avec un Brugada induit, seules ces mesures doivent être effectuées.
Le cas du patient présentant un syndrome de Brugada de type 1 spontané asymptomatique est plus complexe.
À ce niveau, une discussion doit être engagée avec le patient en l’informant de sa pathologie, des limites des connaissances actuelles, du rapport bénéficerisque des thérapeutiques et éventuellement d’autres examens à effectuer. Il peut être proposé au patient de réaliser une SVP qui, si elle est négative, rassurera un peu plus le patient (même si ce n’est pas du 100 %). Le problème est que si la SVP est positive (10 % des cas), il va être difficile d’en rester là.
• Par la suite, un traitement par hydroxyquinidine (Sérécor®) peut être proposé(9).
Le problème est qu’il s’agit d’un traitement qui doit être bien conduit et qui peut présenter des effets secondaires. Une surveillance rapprochée médicale s’avère donc nécessaire dans ce cas avec un contrôle de la SVP pour vérifier sa négativation(10).
• L’autre option est l’implantation d’un DAI, qui chez un patient asymptomatique, doit être bien réfléchie, notamment car il s’agit souvent de patients jeunes avec des risques de complications plus élevées que dans la population standard ayant un DAI (fracture de sonde, infection, problèmes liés aux changements itératifs de boîtier, etc.)(11). À noter que chez les patients ayant un syndrome de Brugada nécessitant l’implantation d’un DAI, l’utilisation d’un DAI sous-cutanée semble préférable du fait du risque de complications à long terme plus faible.
• Enfin l’ablation dans le syndrome de Brugada semble émerger comme une thérapeutique prometteuse. En effet, il a été montré que ces patients présentent de petites zones cicatricielles, surtout épicardiques au niveau du ventricule droit et que l’ablation de ces zones pourrait permettre de négativer le test à la Flécaïne®, réduire l’inductibilité à la SVP et l’aspect électrocardiographique de Brugada(12,13). Un jour, peut-être pourra-t-on proposer cette intervention préventive chez les patients asymptomatiques.
Que disent les recommandations ?
À l’heure actuelle, les recommandations européennes sont assez claires dans le cas de patients présentant un syndrome de Brugada symptomatique mais restent assez vagues pour les patients asymptomatiques avec type 1 spontané compte tenu des incertitudes scientifiques mentionnées précédemment(8) :
- les mesures dans la vie quotidienne sont à préconiser chez tous les patients porteurs d’un syndrome de Brugada (niveau I) ;
- l’implantation d’un défibrillateur est formellement indiquée (niveau I) chez les patients survivants d’une mort subite ou ayant présenté une TV syncopale ;
- l’implantation d’un défibrillateur devrait être considérée (niveau IIa) chez un patient présentant un Brugada de type 1 avec une syncope ;
- l’implantation d’un défibrillateur pourrait être considérée (niveau IIb) chez un patient avec une SVP positive. Cet item peut donc se référer à un patient asymptomatique avec SVP positive ce qui complique la décision compte tenu des éléments qui ont été mentionnés précédemment.
En pratique
Chez un patient porteur d’un syndrome de Brugada induit asymptomatique, seul les mesures de la vie quotidienne sont à prendre.
Cependant chez le type 1 spontané asymptomatique, la prise en charge est plus complexe compte tenu du risque potentiel de mort subite faible mais non négligeable (0,5 %/an).
La décision de la réalisation d’une SVP et de la prise en charge thérapeutique doit se faire avec le patient en lui expliquant les risques et les bénéfices de chacune des stratégies possibles.
De nombreuses études sont en cours pour essayer de mieux préciser quelle est la meilleure stratégie chez ce type de patients.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :